WikiDer > Damascenone
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК (E) -1- (2,6,6-Триметил-1-циклогекса-1,3-диенил) бут-2-ен-1-он | |
| Идентификаторы | |
3D модель (JSmol) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.041.662 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C13ЧАС18О | |
| Молярная масса | 190.286 г · моль−1 |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Дамаскеноны представляют собой серию тесно связанных химических соединений, которые являются компонентами различных эфирные масла. Дамаскеноны относятся к семейству химических веществ, известных как роза. кетоны, который также включает дамасконы и иононы. бета-Дамасценон вносит основной вклад в аромат роз, несмотря на его очень низкую концентрацию, и является важным ароматическим химическим веществом, используемым в парфюмерии.[1]
Дамаскеноны образуются в результате деградации каротиноиды.[2]
В 2008 г. (E) -β-дамасценон был идентифицирован как первичный одорант в Кентукки бурбон.[3]
Биосинтез
Эта секция может быть слишком техническим для большинства читателей, чтобы понять. Пожалуйста помогите улучшить это к Сделайте это понятным для неспециалистов, не снимая технических деталей. (Май 2016) (Узнайте, как и когда удалить этот шаблон сообщения) |
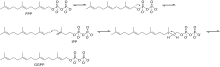
Биосинтез β-дамасценона начинается с фарнезилпирофосфат (FPP) и изопентенилпирофосфат (IPP) реагирует с образованием геранилгеранилпирофосфат (GGPP) Рисунок 1.
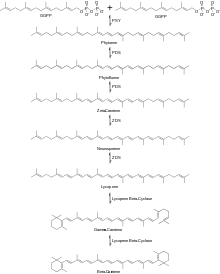
Следующие две молекулы GGPP конденсируются вместе с образованием фитоен за счет удаления дифосфата и протонного сдвига, катализируемого ферментом фитоенсинтаза (PSY). Фитоен затем проходит серию реакций десатурации с использованием фермента фитоен десатураза (PDS) производить фитофлуен тогда ζ-каротин. Было обнаружено, что другие ферменты катализируют эту реакцию, включая CrtI и CrtP.[4]Следующая серия реакций десатурации катализируется ферментом ζ-каротин десатураза (ZDS) к произведенному нейроспорен с последующим ликопин. Другие ферменты, способные катализировать эту реакцию, включают CtrI и CrtQ. Далее ликопин проходит две реакции циклизации с использованием фермента ликопин-β-циклаза первое производство γ-каротин с последующей второй циклизацией, производящей β-каротин как показано на рисунке 2.
Механизм циклизации ликопина до β-каротина показан на схеме 2.
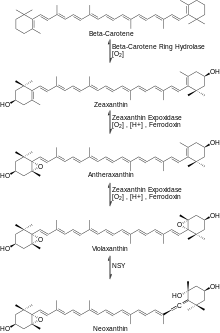
Затем β-каротин вступает в реакцию с O2 и ферментом β-каротиновым кольцом гидроксилазы с образованием зеаксантин.[5]Затем зеаксантин взаимодействует с O2, NADPH (H +) и восстановленным кластером ферредоксина [железо-сера] в присутствии фермента. зеаксантин эпоксидаза (ZE) для производства антераксантина, который аналогичным образом реагирует с образованием виолаксантин. Затем виолаксантин вступает в реакцию с ферментом. неоксантинсинтаза формировать неоксантин основной предшественник β-дамасценона, как показано на рисунке 3.
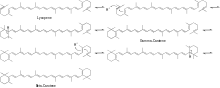
[6]Чтобы получить β-дамасценон из неоксантина, необходимо еще несколько модификаций. Сначала неоксантин подвергается окислительному расщеплению с образованием кетона кузнечика. Затем кетон кузнечика восстанавливается с образованием алленового триола. На этом этапе существует два основных пути, по которым алленовый триол может производить конечный продукт. Алленовый триол может подвергаться реакции дегидратации с образованием либо ацетиленового диола, либо алленового диола. Наконец, последняя реакция дегидратации ацетиленового диола или алленового диола дает конечный продукт β-дамасценон, как показано на рисунке 4.
[7][8] Предлагаемый механизм превращения алленового триола в ацетиленовый диол показан на схеме 3.
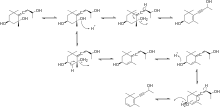
Предлагаемый механизм превращения ацетиленового диола в конечный продукт показан на схеме 4.
Этот механизм известен как Перегруппировка Мейера-Шустера.
Смотрите также
Рекомендации
- ^ Роза (Rosa damascena), Джон С. Леффингуэлл
- ^ Сачихико Исоэ; Шигео Кацумура; Такео Сакан (1973). «Синтез дамасценона и бета-дамаскона и возможный механизм их образования из каротиноидов». Helvetica Chimica Acta. 56 (5): 1514–1516. Дои:10.1002 / hlca.19730560508.
- ^ ЛУИДЖИ ПУАССОН; ПИТЕР ШИБЕРЛЬ (2008). «Характеристика наиболее активных запахов соединений в американском виски из бурбона с помощью анализа разбавления экстракта аромата». Журнал сельскохозяйственной и пищевой химии. 56 (14): 5813–5819. Дои:10.1021 / jf800382m. PMID 18570373.
- ^ Майкл Х. Уолтер; Дитер Штрак (2011). «BCаротиноиды и продукты их расщепления: биосинтез и функции». Nat. Prod. Представитель. 28 (4): 663–692. Дои:10.1039 / c0np00036a. PMID 21321752.
- ^ Цзянь Цзэн; Ченг Ван; Си Чен; Мингли Занг; Цуйхун Юань; Xiatian Wang; Цюн Ван; Мяо Ли; Сяоянь Ли; Лин Чен; Кэсю Ли; Джунли Чанг; Юешэн Ван; Гуансиа Ян; Гуанюань Хэ (2015). «Ликопин-β-циклаза играет важную роль в биосинтезе провитамина А в эндосперме пшеницы». BMC Биология растений. 15 (112): 112. Дои:10.1186 / s12870-015-0514-5. ЧВК 4433027. PMID 25943989.
- ^ Кодзи Миками; Масаси Хосокава (2013). «Биосинтетический путь и польза для здоровья фукоксантина, ксантофилла, специфичного для водорослей, в бурых морских водорослях». Int. J. Mol. Наука. 14 (7): 13763–13781. Дои:10.3390 / ijms140713763. ЧВК 3742216. PMID 23820585.
- ^ Яир Безман; Ицхак Билкис; Питер Винтерхальтер; Петер Флейшманн; Рассел Л. Роузефф; Сюзанна Бальдерманн; Майкл Наим (2005). «Термическое окисление 9'-цис-неоксантина в модельной системе, содержащей пероксиуксусную кислоту, приводит к сильному запаху β-дамасценона». Журнал сельскохозяйственной и пищевой химии. 53 (23): 9199–9206. Дои:10.1021 / jf051330b. PMID 16277423.
- ^ Питер Винтерхальтер; Реджеп Гёк (2013). «TDN и β-Damascenone: два важных метаболита каротиноидов в вине». Продукты расщепления каротиноидов. Серия симпозиумов ACS. 1134. С. 125–137. Дои:10.1021 / bk-2013-1134.ch011. ISBN 978-0-8412-2778-1.