WikiDer > Дэвид Э. Клеммер
Дэвид Э. Клеммер | |
|---|---|
 | |
| Родившийся | 23 февраля 1965 г. |
| Альма-матер | |
| Известен | Спектрометрия ионной подвижности, масс-спектрометрии |
| Награды | Медаль Бимана, Награда ACS Chemical Instrumentation Award |
| Научная карьера | |
| Поля | Аналитическая химия, масс-спектрометрии |
| Учреждения | Университет Индианы Блумингтон |
| Докторант | Питер Б. Арментроут |
| Интернет сайт | www |
Дэвид Э. Клеммер (23 февраля 1965 г., Аламоса, Колорадо) является химиком-аналитиком и заслуженным профессором, заведующим кафедрой химии им. Роберта и Марджори Манн. Университет Индианы в Блумингтон, Индиана, где он возглавляет Clemmer Group.[1] Клеммер разрабатывает новые научные инструменты для масс-спектрометрия подвижности ионов (IMS / MS), включая первый прибор для вложенной ионной подвижности время полета масс-спектрометрии.[2] Он получил ряд наград, в том числе медаль Бимана в 2006 году «за новаторский вклад в интеграцию разделения ионной подвижности с различными технологиями масс-спектрометрии».[3]
ранняя жизнь и образование
Клеммер родился 23 февраля 1965 года в семье художника Эда Клеммера и его жены Мэри Энн, учительницы. Аламоса, Колорадо.[4] Он присутствовал Государственный колледж Адамса, где он изначально специализировался на музыке, а затем перешел в науку.[4] Он получил степень бакалавра наук. по химии с отличием в 1987 году. Университет Юты, получив докторскую степень. по физической химии в 1992 г.[5] Его научным руководителем был Питер Б. Арментроут,[2] с которым он изучал ионы переходных металлов в газовых реакциях.[3]
Карьера
В течение 1992–1993 годов Клеммер работал докторантом в Японии при поддержке Японского общества содействия научным стипендиям в Технологический институт Химэдзи. Он работал с Кенджи Хонма над механизмами переноса электронов.[6] и реакции атомов металлов в возбужденном состоянии и газообразных молекул.[3]С 1993 по 1995 год Клеммер был научным сотрудником докторантуры в Северо-Западный университет, где он работал с Мартином Ф. Джарролдом,[3] изучение сворачивание белка и конформация белка в газовой фазе с использованием таких методов, как Спектрометрия ионной подвижности.[7][8]
В 1995 году Клеммер поступил на химический факультет Университета Индианы.[3] С 2002 по 2006 год он занимал должность заведующего кафедрой химии.[9] Он является профессором и возглавляет кафедру химии Роберта и Марджори Манн, на которую он был назначен в 2002 году.[3][5] Опубликовал более 230 статей.[1]
Среди тех, кто оказал на него влияние, он включает Майкл Т. Бауэрс, Джесси Л. Бошам, Р. Грэм Кукс, Скотт А. Маклаки, Фред Маклафферти, Эван Р. Уильямс, Джозеф А. Лоо, Вики Высоцкий, и Джули А. Лири.[2] Среди его аспирантов Рена А. С. Робинсон, Стивен Валентайн, чероки Хоглунд-Хайзер,[10] и Кэтрин Сребалус Барнс.[11]
Исследование
Клеммер особенно заинтересован в изучении структурных характеристик и конформационной динамики сложных систем с низкой симметрией. Клеммер разрабатывает научные инструменты и методы для исследования биомолекулярная структура и сложные биомолекулярные смеси в газовой фазе с использованием спектрометрии ионной подвижности.[11]
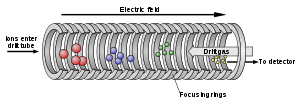
Методы ионной подвижности разделяют ионы на разные группы в зависимости от их способности перемещаться через электрически заряженный буферный газ. Это позволяет дифференцировать сложные смеси способами, которые не могут быть достигнуты только с помощью масс-спектрометрии. Даже незначительные количества соединений можно различить и по-разному исследовать в соответствии с такими характеристиками, как размер, форма и заряд, а также масса.[2]
Клеммер помог установить подвижность ионов как мощный инструмент и область исследований посредством своих «тщательных исследований» и «революционных инструментальных методов».[3] В ранних работах Клеммер и Джаррольд использовали длинные дрейфовые трубки с некластеризованной газовой атмосферой для увеличения разрешающей способности спектрометрии ионной подвижности.[12]Клеммера по методам газофазного разделения для ионная подвижность-масс-спектрометрия (IM-MS) и их применение к структурному анализу интактных белков считается «особенно важной вехой» в применении IM-MS к исследованию биомолекулярных структур.[13][14][15]Клеммер и его коллеги разработали как минимум дюжину различных конфигураций, сочетающих модульные компоненты для ионной подвижности с масс-спектрометрическими приборами.[2][16] К ним относятся сочетание подвижности ионов с Времяпролетная масс-спектрометрия (TOF).[17][18][19]Они также разработали первый инструмент вложенной ионной подвижности. время полета масс-спектрометрии.[2][5]
Такое оборудование позволяет исследователям больше узнать как о структурах, так и о конформационной динамике систем.[20]Клеммер идентифицировал фундаментальные отношения между зарядовыми состояниями и структурами и показал, что одно зарядовое состояние может существовать в более чем одной конформации в газовых состояниях.[3] Такие методы можно использовать для изучения как белков, так и пептидов.[21][3]В ранних работах Клеммер показал, что множественные конформации гемепротеин цитохром с могут быть дифференцированы по их мобильности.[22] Кроме того, подвижность различных хиральных изомеров связана с укладкой их белков.[23] Более современные методы позволяют исследователям отслеживать переходы в конформациях макромолекулярных ионов во время газовой фазы. Короткий импульс ионов вводится в дрейфовую трубку за счет ионизации электрораспылением. Структуры разделяются в зависимости от их подвижности. Подвергая определенные состояния возбуждающим столкновениям, можно создавать новые структуры и отслеживать их посредством различных конформационных изменений. Изменения конформации во время газофазных данных можно затем сопоставить с исходными популяциями структур. Таким образом, исследователи могут понять возможные пути между структурами.[24]
Понимание того, как происходит сворачивание белков в трехмерных молекулах, - одна из постоянных проблем биологии. Белки различной формы часто имеют разную биологическую активность и медицинскую ценность.[5] Работа Клеммера находит применение в науках о жизни для понимания конформации структур в больших белковых комплексах,[5] профилирование протеома плазмы,[13] изучение роли белков и сворачивания белков в нейродегенеративных заболеваниях,[5] выявление возможных маркеров рака в крови, моче или слюне,[4] и повышение эффективности открытия лекарств.[25] Методы ионной подвижности-масс-спектрометрии также позволяют измерять и коррелировать большое количество различных характеристик одновременно в одном анализе. Исследователи могут использовать эти методы для исследования сложных биологических образцов на предмет наличия липидомика, протеомика, гликомика, и метаболомика Информация.[13]
Компании
Клеммер является соучредителем За пределами геномики, компания, занимающаяся системной биологией, и основатель Прогностическая физиология и медицина, биотехнологическая компания, специализирующаяся на персонализированная медицина.[4]
Увлечения
Помимо игры на нескольких инструментах, Клеммер любит бегать марафоны.[2]
Награды и отличия
- 2018, выдающийся вклад Джона Б. Фенна, поделился с Мартином Ф. Джарролдом [26] и Герт фон Хельден,[27] Американское общество масс-спектрометрии[28]
- 2017, научный сотрудник Национальной академии изобретателей.[29]
- 2014–2015, Премия ANACHEM [30]
- 2014 г., заслуженный профессор, Университет Индианы, Блумингтон.[5]
- 2014 г., заслуженный выпускник химии, Университет Юты[9]
- 2012, Американское химическое общество (ACS) Награда за химическое оборудование[31]
- 2011 г., научный сотрудник, Американская ассоциация развития науки (AAAS)[32]
- 2011–2012 гг., Научный сотрудник Японского общества содействия науке (JSPS).
- 2010, выдающийся выпускник штата Адамс[4]
- 2009, Премия Трейси М. Соннеборн, Университет Индианы в Блумингтоне[11]
- 2007, Американское химическое общество (ACS) награда Акрон [33]
- 2006, медаль Бимана, Американское общество масс-спектрометрии[3]
- 2005 г., научный сотрудник, Королевское химическое общество
- 2003–2005, Национальный фонд науки Премия за специальное творчество
- 2002, Pittcon Награда за достижение [34]
- 2002, Назван одним из Популярная наука'Список 10 самых блестящих [10]
- 2002, назначен Робертом и Марджори Манн кафедрой химии Университета Индианы в Блумингтоне.[5]
- 2000–2002, Премия Эли Лилли в области аналитической химии
- 1998–2001 гг., Научный сотрудник, Alfred P. Sloan Research [35]
- 2000, Национальная премия Fresenius, Фи Лямбда ипсилон[36]
- 1999–2000, Американское химическое общество (ACS), Отдел аналитической химии, Премия Артура Ф. Финдейса
- 1999, премия учителя и ученого Камиллы Дрейфус, Фонд Камиллы и Генри Дрейфусов[37]
- 1999, «Новаторы до 35 лет», Обзор технологий MIT[25]
- 1996–2000, Национальный фонд науки Премия за раннюю карьеру
Рекомендации
- ^ а б "Клеммер Груп Проф. Дэвид Э. Клеммер". Университет Индианы Блумингтон. Получено 26 апреля 2017.
- ^ а б c d е ж грамм «Профессор Дэвид Клеммер, Университет Индианы». Waters Наука о возможном. Получено 26 апреля 2017.
- ^ а б c d е ж грамм час я j Bierbaum, Veronica M .; Фред В. Маклафферти (2007). "В центре внимания Дэвида Э. Клеммера, лауреата медали Бимана 2006 г.". Журнал Американского общества масс-спектрометрии. 18 (7): 1161–1162. Дои:10.1016 / j.jasms.2007.05.004. PMID 17555983.
- ^ а б c d е Релиа, Линда (26 августа 2010 г.). «Клеммер превращает науку в искусство». Государственный университет Адамса. Получено 28 апреля 2017.
- ^ а б c d е ж грамм час "Достижения и награды университета: почетный доктор Дэвид Э. Клеммер". Университет Индианы Блумингтон. Получено 28 апреля 2017.
- ^ Хонма, Кендзи; Клеммер, Дэвид Э. (1995). «Важность механизма переноса электрона в реакциях нейтральных атомов переходных металлов». Лазерная химия. 15 (2–4): 209–220. Дои:10.1155/1995/25319.
- ^ Клеммер, Дэвид Э .; Джарролд, Мартин Ф. (июнь 1997 г.). «Измерения подвижности ионов и их приложения к кластерам и биомолекулам». Журнал масс-спектрометрии. 32 (6): 577–592. Дои:10.1002 / (SICI) 1096-9888 (199706) 32: 6 <577 :: AID-JMS530> 3.0.CO; 2-4. S2CID 16681465.
- ^ Клеммер, Дэвид Э .; Хаджинс, Роберт Р .; Джарролд, Мартин Ф. (октябрь 1995 г.). «Конформации голого белка: цитохром с в газовой фазе» (PDF). Журнал Американского химического общества. 117 (40): 10141–10142. Дои:10.1021 / ja00145a037. Получено 1 мая 2017.
- ^ а б «Награда выдающихся выпускников химии 2014 года». Университет Юты. Получено 1 мая 2017.
- ^ а б Хиннефельд, Стив (2002). "'Блестящие 10 ученых благодарны коллегам из IU » (PDF). Hoosier Times. Получено 2 мая 2017.
- ^ а б c Коннелли-Эскин, Синди (20 апреля 2009 г.). «Объявлен лауреат премии Трейси М. Соннеборн и профессор Провоста». IU News Room. Получено 28 апреля 2017.
- ^ Eiceman, G.A .; Карпас, З .; Хилл-младший, H.H. (2014). Спектрометрия ионной подвижности (Третье изд.). Бока-Ратон, Флорида: CRC. С. 30–31. ISBN 9781439859971.
- ^ а б c Маклин, Джон А. (октябрь 2009 г.). "Редукция корреляции массы и подвижности: конформационный ландшафт безводных биомолекул". Журнал Американского общества масс-спектрометрии. 20 (10): 1775–1781. Дои:10.1016 / j.jasms.2009.06.016. PMID 19646898.
- ^ Шелимов, К.Б .; Clemmer, D.E .; Hudgins, R.R .; Джарролд, М.Ф. (1997). "Структура белка в вакууме: газовая фаза конформации BPTI и цитохрома c". Варенье. Chem. Soc. 119 (9): 2240–2248. Дои:10.1021 / ja9619059. S2CID 9163743.
- ^ Ибрагим, Йехиа М .; Бейкер, Эрин С .; Дэниэлсон, Уильям Ф .; Norheim, Randolph V .; Prior, David C .; Андерсон, Гордон А .; Белов, Михаил Е .; Смит, Ричард Д. (февраль 2015 г.). «Разработка нового времяпролетного масс-спектрометра ионной подвижности». Международный журнал масс-спектрометрии. 377: 655–662. Дои:10.1016 / j.ijms.2014.07.034. ЧВК 4501404. PMID 26185483.
- ^ «Группа Клеммер, разработка нового оборудования для ионной мобильности». Университет Индианы. Получено 2 мая 2017.
- ^ Hoaglund, Cherokee S .; Валентин, Стивен Дж .; Sporleder, C. Ray; Рейли, Джеймс П .; Клеммер, Дэвид Э. (1998). "Трехмерная ионная подвижность / TOFMS-анализ биомолекул, распыленных электрораспылением" (PDF). Анальный. Chem. 70 (11): 2236–2242. Дои:10.1021 / ac980059c. PMID 9624897. Получено 1 мая 2017.
- ^ Хендерсон, Шейла С .; Валентин, Стивен Дж .; Counterman, Anne E .; Клеммер, Дэвид Э. (1999). «ESI / ионная ловушка / ионная подвижность / времяпролетная масс-спектрометрия для быстрого и чувствительного анализа биомолекулярных смесей» (PDF). Анальный. Chem. 71 (2): 291–301. Дои:10.1021 / ac9809175. PMID 9949724. Получено 1 мая 2017.
- ^ Мён, Сонни; Ли, Ён Джин; Мун, Мён Хи; Тараска, Джон; Соуэлл, Рена; Кенигер, Сторми; Hilderbrand, Amy E .; Валентин, Стивен Дж .; Шербас, Люси; Чербас, Петр; Кауфманн, Томас С .; Миллер, Дэвид Ф .; Мехреф, Йехиа; Новотный, Милош В .; Юинг, Майкл А .; Sporleder, C. Ray; Клеммер, Дэвид Э. (октябрь 2003 г.). «Разработка высокочувствительных методов спектрометрии подвижности ионов с ионной ловушкой: времяпролетные методы: высокопроизводительное разделение пептидов, происходящих из белкового экстракта, с помощью нано-LC-IMS-TOF». Аналитическая химия. 75 (19): 5137–5145. Дои:10.1021 / ac030107f. PMID 14708788. Получено 1 мая 2017.
- ^ Ланукара, Франческо; Холман, Стивен У .; Грей, Кристофер Дж .; Айерс, Клэр Э. (21 марта 2014 г.). «Возможности масс-спектрометрии ионной подвижности для структурной характеристики и изучения конформационной динамики». Химия природы. 6 (4): 281–294. Дои:10.1038 / nchem.1889. PMID 24651194. S2CID 2512242.
- ^ Гросс, Майкл Л .; Чен, Годун; Праманик, Бирендра Н. (2012). Масс-спектрометрия белков и пептидов в открытии лекарств. Хобокен, штат Нью-Джерси: Wiley. С. 202–203. ISBN 978-0-470-25817-0.
- ^ Hoaglund-Hyzer, Cherokee S .; Counterman, Anne E .; Клеммер, Дэвид Э. (1999). «Безводные белковые ионы» (PDF). Chem. Rev. 99 (10): 3037–3079. Дои:10.1021 / cr980139g. PMID 11749510. Получено 1 мая 2017.
- ^ Шварцбург, Александр А. (2008). Спектрометрия дифференциальной подвижности ионов: нелинейный перенос ионов и основы FAIMS. Бока-Ратон, Флорида: CRC Press. С. 25–26.
- ^ «Встреча Питтсбургского общества спектроскопии в январе 2013 г.». Общество спектроскопии Питтсбурга. Получено 2 мая 2017.
- ^ а б «Дэвид Клеммер, 34 университета Индианы». Новаторы до 35 лет: 1999. Обзор технологий MIT. Получено 28 апреля 2017.
- ^ "MFJ Research Group".
- ^ "Герт фон Хельден Групп".
- ^ "Отличный вклад ASMS Джона Б. Фенна".
- ^ "Страница стипендиатов Национальной академии изобретателей".
- ^ «Награды АНАХЕМ».
- ^ «Премия DAC в области химического приборостроения». Американское химическое общество (ACS). Отделение аналитической химии ACS. Получено 26 апреля 2017.
- ^ «Рекордные 10 преподавателей получили звание стипендиата AAAS, крупнейшего в мире научного общества». Внутри IU. 1 декабря 2011 г.
- ^ «Премия Акрон Секция».
- ^ «Питткон 2002».
- ^ "Стипендии Sloan Research".
- ^ "Национальная премия Фрезениуса". Северо-Западный университет. Получено 1 мая 2017.
- ^ "Программа награждения учителей и ученых Камиллы Дрейфус" (PDF). Фонд Камиллы Дрейфус. Получено 28 апреля 2017.
внешняя ссылка
- http://www.indiana.edu/~clemmer/home.htm
- Дэвид Э. Клеммер публикации, проиндексированные Google ученый