WikiDer > EML4-ALK-положительный рак легкого
| EML4-ALK-положительный рак легкого | |
|---|---|
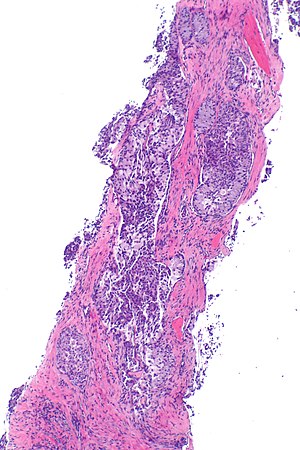 | |
| Микрофотография показывает ALK-положительную аденокарциному легкого. H&E пятно. | |
| Специальность | Онкология |
EML4-ALK-положительный рак легкого является основным злокачественный опухоль легкого чей клетки содержат характерную аномальную конфигурацию ДНК где иглокожие, связанные с микротрубочками, подобные белку 4 (EML4) ген сливается с киназа анапластической лимфомы (ALK) ген. Это ненормальное слияние генов приводит к производству белок (EML4-ALK), который во многих случаях способствует развитию и поддержанию злокачественного поведения рак клетки.[1]
Преобразование EML4-ALK Впервые гибридный ген был обнаружен при немелкоклеточной карциноме легкого (НМРЛ) в 2007 году.[2]
Признаки и симптомы
Признаки и симптомы этого варианта рака легких, по-видимому, имитируют симптомы основного основного типа клеток.[нужна цитата]
Диагностика
Классификация
Большинство карцином легких, содержащих EML4-ALK слияние генов аденокарциномы.
Некоторые исследования показывают, что папиллярная аденокарцинома и аденокарцинома из перстневых клеток[3] варианты с большей вероятностью несут этот слитый ген, чем другие гистологические варианты.
Скрининг
Скрининг на ALK-положительный рак легких в настоящее время является стандартом лечения в США и Канаде. Скрининг можно проводить с иммуноокрашиванием, РЫБЫ, или секвенирование следующего поколения (NGS).[нужна цитата]
Уход
Кризотиниб это таргетная терапия (одобренная FDA в 2011 году), производимая Pfizer и продаваемая под торговой маркой Xalkori и Crizalk, которая нацелена на гибридный ген EML4 / ALK.[нужна цитата]
Церитиниб - это таргетная терапия второго поколения (одобрено FDA в 2014 году), производимая Novartis и продаваемая под торговой маркой Zykadia, которая также нацелена на гибридный ген EML4, но как лекарство второго поколения имеет меньшую молекулу, которая обеспечивает лучшее проникновение в кровяной мозг. Барьер (BBB) по сравнению с кризотинибом и более эффективен для защиты центральной нервной системы (ЦНС).[нужна цитата]
Алектиниб еще одна таргетная терапия второго поколения, одобренная (для этого) Японией в 2014 г.[4] и по США FDA в 2015 году.[5], производятся Genentech и продаются под торговой маркой Alecensa.
Бригатиниб таргетная терапия второго поколения (одобрено FDA в 2017 году), производимая Takeda и продаваемая под торговой маркой Alunbrig.
Энсартиниб - это таргетная терапия второго поколения (пробный препарат X-396), производимая XCovery.[нужна цитата]
Лорлатиниб - это таргетная терапия третьего поколения (ожидает одобрения FDA в рамках пробного препарата PF-6463922), производимая Pfizer.[нужна цитата]
TPX-0005 - это испытательный препарат нового поколения для таргетной терапии.[нужна цитата]
Прогноз
Лечение кризотинибом достигает 60% Скорость отклика.[6] Однако кризотиниб не показал улучшения общей выживаемости по сравнению с химиотерапией.[7] Это может быть связано с тем, что процент перекрестного перехода на кризотиниб у пациентов, первоначально получавших химиотерапию, составил 70%.[8] Кроме того, пациенты с отрицательным результатом на слияние EML4 / ALK имели ответ на кризотиниб до 35%.[9]
Эпидемиология
EML4-ALK слияния генов происходят почти исключительно при карциномах, возникающих у некурящих.[10][11] Около 4% немелкоклеточных карцином легких связаны с гибридным геном тирозинкиназы EML4-ALK.[12] 4–6% аденокарцином легких связаны с геном слияния.[6]
EML4-ALK мутация редко встречается в сочетании с К-РАН или же EGFR мутации.
Рекомендации
- ^ Soda M, Choi YL, Enomoto M и др. (Август 2007 г.). «Идентификация трансформирующего слитого гена EML4-ALK при немелкоклеточном раке легкого». Природа. 448 (7153): 561–6. Bibcode:2007Натура.448..561S. Дои:10.1038 / природа05945. PMID 17625570. S2CID 2172543.
- ^ Sasaki T, Rodig SJ, Chirieac LR, Jänne PA (июль 2010 г.). «Биология и лечение немелкоклеточного рака легкого EML4-ALK». Евро. J. Рак. 46 (10): 1773–80. Дои:10.1016 / j.ejca.2010.04.002. ЧВК 2888755. PMID 20418096.
- ^ Ко Й, Ким Д. В., Ким Т. М. и др. (Май 2011 г.). «Клинико-патологические характеристики и исходы пациентов с анапластической лимфомой, прогрессирующей аденокарциномой легких: предложение по эффективной стратегии скрининга этих опухолей». J Торак Онкол. 6 (5): 905–12. Дои:10.1097 / JTO.0b013e3182111461. PMID 21358343. S2CID 38377715.
- ^ Япония стала первой страной, одобрившей алектиниб компании Рош для людей с конкретной формой рака легких на поздней стадии.
- ^ Новая пероральная терапия для лечения ALK-положительного рака легких. Декабрь 2015
- ^ а б Bayliss, R; Цой, Дж (март 2016 г.). «Молекулярные механизмы, лежащие в основе рака, вызванного EML4-ALK, и их ответ на целевые препараты». Клеточные и молекулярные науки о жизни. 73 (6): 1209–1224. Дои:10.1007 / s00018-015-2117-6. ЧВК 4761370. PMID 26755435.
- ^ https://www.accessdata.fda.gov/drugsatfda_docs/label/2017/202570s019lbl.pdf
- ^ Соломон, Бенджамин Дж .; Мок, Тони; Ким, Донг-Ван; Ву И-Лонг; Накагава, Кадзухико; Мехайл, Тарек; Фелип, Энрикета; Каппуццо, Федерико; Паолини, Иоланда; Усари, Тициана; Айер, Шривидья; Райзман, Арлин; Wilner, Keith D .; Турси, Дженнифер; Блэкхолл, Фиона; ПРОФИЛЬ 1014 Следователи (2014). «Кризотиниб первой линии в сравнении с химиотерапией при ALK-положительном раке легкого». Медицинский журнал Новой Англии. 371 (23): 2167–2177. Дои:10.1056 / NEJMoa1408440. HDL:2434/426878. PMID 25470694.
- ^ https://www.accessdata.fda.gov/cdrh_docs/pdf11/P110012B.pdf
- ^ Шоу А.Т., Йип Б.И., Мино-Кенудсон М. и др. (Сентябрь 2009 г.). «Клинические особенности и исходы у пациентов с немелкоклеточным раком легкого, несущих EML4-ALK». Журнал клинической онкологии. 27 (26): 4247–4253. Дои:10.1200 / JCO.2009.22.6993. ЧВК 2744268. PMID 19667264.
- ^ Мартелли М.П., Соцци Г., Эрнандес Л. и др. (Февраль 2009 г.). «Перестройка EML4-ALK при немелкоклеточном раке легкого и неопухолевых тканях легкого». Являюсь. Дж. Патол. 174 (2): 661–70. Дои:10.2353 / ajpath.2009.080755. ЧВК 2630573. PMID 19147828.
- ^ Кумар, В; Аббас АК; Астер JC (2013). «Глава 5». Базовая патология Роббинса (9-е изд.). Elsevier Saunders. п. 212. ISBN 978-1-4377-1781-5.
