WikiDer > Гексаметилдисилоксан
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Гексаметилдисилоксан | |
| Другие имена Бис (триметилсилил) эфир Бис (триметилсилил) оксид | |
| Идентификаторы | |
3D модель (JSmol) | |
| Сокращения | HMDSO, (TMS)2О |
| 1736258 | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.003.176 |
| Номер ЕС |
|
| MeSH | Гексаметилдисилоксан |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1993 |
| |
| |
| Характеристики | |
| C6ЧАС18ОSi2 | |
| Молярная масса | 162.379 г · моль−1 |
| Внешность | Бесцветная жидкость |
| Плотность | 0,764 г см−3 |
| Температура плавления | -59 ° С (-74 ° F, 214 К) |
| Точка кипения | От 100 до 101 ° C (от 212 до 214 ° F, от 373 до 374 K) |
| 930.7±33.7 ppb (23 ° С) [1] | |
| Давление газа | 43 гПа (20 ° C) [2] |
| 1.377 | |
| Опасности | |
| Главный опасности | Легковоспламеняющаяся жидкость и пар Вызывает серьезное раздражение глаз |
Классификация ЕС (DSD) (устарело) | |
| R-фразы (устарело) | R11 |
| S-фразы (устарело) | S16 |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | -1 (1) ° С |
| Родственные соединения | |
Родственные соединения | Дисилоксан Тетраметилсилан |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
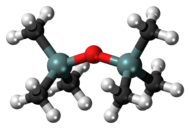
Гексаметилдисилоксан (HMDSO) является кремнийорганическое соединение с формулой O [Si (CH3)3]2. Эта летучая бесцветная жидкость используется как растворитель и как реагент в органический синтез. Он подготовлен гидролиз из триметилсилилхлорид. Молекула является прототипом дисилоксан и напоминает подразделение полидиметилсилоксан.
Синтез и реакции
Гексаметилдисилоксан можно получить путем добавления триметилсилилхлорид к очищенной воде:
- 2 меня3SiCl + H2O → 2 HCl + O [Si (CH3)3]2
Он также является результатом гидролиза силилэфиров и других силил-защищенных функциональных групп. HMDSO можно превратить обратно в хлорид реакцией с Me.2SiCl2.[3]
Гексаметилдисилоксан в основном используется как источник триметилсилил функциональная группа (-Si (CH3)3) в органический синтез. Например, в присутствии кислоты катализатор, он превращает спирты и карбоновые кислоты в силиловые эфиры и силиловые эфиры соответственно.[4]
Он реагирует с оксидом рения (VII) с образованием силоксид:[5]
- Re2О7 + O [Si (CH3)3]2 → 2 O3ReOSi (CH3)3
Ниша использует
HMDSO используется в качестве внутреннего стандарта для калибровки химический сдвиг в1ЧАС ЯМР-спектроскопия. С ним легче обращаться, поскольку он менее летуч, чем обычный стандартный тетраметилсилан но по-прежнему отображает только синглет около 0 ppm.
HMDSO имеет еще более слабую сольватирующую способность, чем алканы. Поэтому иногда его используют для кристаллизоваться высоколипофильные соединения.
Он используется в жидкие повязки (спрей на пластыри), например, спрей кавилон, для защиты поврежденной кожи от раздражения другими биологическими жидкостями. Он также используется для смягчения и удаления остатков клея, оставленных медицинской лентой и повязками, без дальнейшего раздражения кожи.
HMDSO изучается для создания диэлектрических материалов с низким k для полупроводниковой промышленности компанией PECVD (плазменное химическое осаждение из паровой фазы).
HMDSO использовался в качестве репортерной молекулы для измерения напряжения кислорода в тканях (pO2). HMDSO является высокогидрофобным и демонстрирует высокую растворимость газа и, следовательно, сильную реакцию скорости релаксации спиновой решетки ядерного магнитного резонанса (R1) на изменения pO2. Молекулярная симметрия обеспечивает единственный сигнал ЯМР. После прямой инъекции в ткани его использовали для создания карт динамики оксигенации опухолей и мышц в отношении дыхания гипероксическим газом.[6]
Рекомендации
- ^ Сударшанан Варапратх; Сесил Л. Фрай; Джерри Хэмелинк (1996). «Растворимость перметилсилоксанов (силиконов) в воде». Экологическая токсикология и химия. 15 (8): 1263–1265. Дои:10.1002 / и т.д.5620150803.
- ^ Запись CAS RN 107-46-0 в базе данных веществ GESTIS Институт охраны труда и здоровья, по состоянию на 11 марта 2015 г.
- ^ Röshe, L .; John, P .; Рейтмайер, Р. «Органические соединения кремния» Энциклопедия промышленной химии Ульмана. Джон Уайли и сыновья: Сан-Франциско, 2003. Дои:10.1002 / 14356007.a24_021.
- ^ Pfeifer, J. «Гексаметилдисилоксан» в Энциклопедия реагентов для органического синтеза (Ред: Л. Пакетт) 2004, J. Wiley & Sons, Нью-Йорк. Дои:10.1002 / 047084289X.
- ^ Schmidt, M .; Schmidbaur, H., "Trimethylsilyl perrhenate", Inorg. Synth. 1967, 9, 149–151. Дои:10.1002 / 9780470132401.ch40
- ^ Кодибагкар В.Д., Цуй В., Мерритт М.Э., Мейсон Р.П. Новый подход ЯМР 1H к количественной оксиметрии тканей с использованием гексаметилдисилоксана. Magn Reson Med 2006; 55: 743–748 и Кодибагкар В.Д., Ван Х, Пачеко-Торрес Дж., Гулака П., Мейсон Р.П. Протонная визуализация силоксанов для картирования уровней оксигенации тканей (ПИСТОЛЕТ): инструмент для количественной оксиметрии тканей. ЯМР Биомед 2008; 21: 899-907.
