WikiDer > Гексанитробензол
 | |
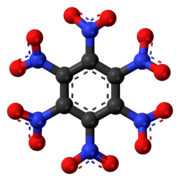 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Гексанитробензол | |
| Другие имена 1,2,3,4,5,6-гексанитробензол | |
| Идентификаторы | |
3D модель (JSmol) | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Характеристики | |
| C6N6О12 | |
| Молярная масса | 348,10 г / моль |
| Внешность | Желтые или коричневые порошкообразные кристаллы |
| Плотность | 1.985 грамм/см3 |
| Температура плавления | От 256 до 264 ° C (от 493 до 507 ° F; от 529 до 537 K) |
| Взрывоопасные данные | |
| Чувствительность к ударам | Никто |
| Чувствительность к трению | Никто |
| Скорость детонации | 9,340 РС[1] |
| RE фактор | 1.8 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Гексанитробензол, также известный как HNB, является высокимплотность взрывной сложный с химическая формула C6N6О12, полученный окисляющий в амин группа пентанитроанилин с пероксид водорода в серная кислота.
Характеристики
У HNB есть нежелательное свойство: он умеренно чувствителен к свету и поэтому его трудно использовать безопасно. В настоящее время он не используется в производстве взрывчатых веществ, хотя он используется в качестве химического вещества-прекурсора в одном из методов производства ТАТБ, другое взрывчатое вещество.
HNB экспериментально использовался в качестве источника газа для взрывоопасных газодинамический лазер.[2] В этом приложении HNB и тетранитрометан предпочтительнее более обычных взрывчатых веществ, поскольку продукты взрыва CO2 и н2 являются достаточно простой смесью для моделирования газодинамических процессов и очень похожи на обычную газодинамическую лазерную среду. Вода и водородные продукты многих других взрывчатых веществ могут мешать колебательным состояниям CO.2 в этом типе лазера.
Подготовка
Во время Великой Отечественной войны в Германии предложили метод синтеза гексанитробензола, который предполагалось производить в полупромышленном масштабе по следующей схеме:
- C6ЧАС3(НЕТ2)3 → С6ЧАС3(NHOH)3 (частичное сокращение)
- C6ЧАС3(NHOH)3 → С6(НЕТ2)3(NHOH)3 (нитрование)
- C6(НЕТ2)3(NHOH)3 → С6(НЕТ2)6 (окисление)
Полное нитрование бензола практически невозможно, так как нитрогруппы деактивация групп для дальнейшего нитрования.
Дополнительные свойства
- Чепмен-Давление детонации жуже: 43 ГПа
- Плотность кристаллов: 2,01
Смотрите также
Примечания
- ^ Точное определение парных потенциалов для CшЧАСИксNуОz система молекул: полуэмпирический метод, Тиль и др., 1995
- ^ Газодинамический лазер на конденсированных взрывчатых веществах, Патент США 4099142
Рекомендации
- Теплота образования и химический состав
- Синтез и характеристика производных галогенов и нитрофенилазидов как высокоэнергетических материалов., PhD Thesis, Adam, D; 2001 г.
- Р. Л. Аткинс; Р. А. Холлинз; У. С. Уилсон (1986). «Синтез полинитросоединений. Гексазамещенные бензолы». J. Org. Chem. 51 (17): 3261–3266. Дои:10.1021 / jo00367a003.
- А. Т. Нильсен; Р. Л. Аткинс; У. П. Норрис (1979). «Окисление поли (нитро) анилинов до поли (нитро) бензолов. Синтез гексанитробензола и пентанитробензола». J. Org. Chem. 44 (7): 1181–1182. Дои:10.1021 / jo01321a041.
- З. А. Акопян; Ю. Т. Стручков; В. Г. Дашевский (1966). «Кристаллическая и молекулярная структура гексанитробензола». Журнал структурной химии. 7 (3): 385–392. Дои:10.1007 / BF00744430. S2CID 96053767.