WikiDer > Сальвинорин - Википедия
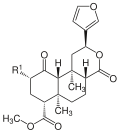
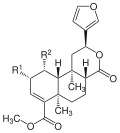
Сальвинорины представляют собой группу природных химических соединений и их структурные аналоги. Несколько сальвиноринов были выделены из Сальвия дивинорум. Они классифицируются как дитерпеноид фуранолактоны. Сальвинорин А галлюциноген с диссоциативным действием.
Было выделено и охарактеризовано несколько сальвиноринов.
| Имя | Структура | р1 | р2 | Химическая формула | Молярная масса | Количество CAS | PubChem |
|---|---|---|---|---|---|---|---|
| Сальвинорин А | –OCOCH3 | − | C23ЧАС28О8 | 432,46 г · моль−1 | 83729-01-5 | CID 128563 из PubChem | |
| Сальвинорин Б | -ОЙ | − | C21ЧАС26О7 | 390,43 г · моль−1 | 92545-30-7 | CID 11440685 из PubChem | |
| Сальвинорин С | –OCOCH3 | –OCOCH3 | C25ЧАС30О9 | 475,29 г · моль−1 | 385785-99-9 | – | |
| Сальвинорин Д | –OCOCH3 | -ОЙ | C23ЧАС28О8 | 432,47 г · моль−1 | 540770-13-6 | – | |
| Сальвинорин E | -ОЙ | –OCOCH3 | C23ЧАС28О8 | 432,47 г · моль−1 | 540770-14-7 | – | |
| Сальвинорин Ф | -ОЙ | -ЧАС | C21ЧАС26О6 | 374,43 г · моль−1 | 540770-15-8 | – | |
| Сальвинорин Г | = O | –OCOCH3 | C23ЧАС26О8 | 430,45 г · моль−1 | 866622-54-0 | – | |
| Сальвинорин H | -ОЙ | -ОЙ | C21ЧАС26О7 | 390,43 г · моль−1 | 872004-62-1 | – | |
| Сальвинорин I | – | – | C21ЧАС28О7 | 392,45 г · моль−1 | 917951-71-4 | – | |
| 17α-Сальвинорин J | 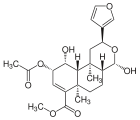 | – | – | C23ЧАС30О8 | 434,49 г · моль−1 | 1157894-83-1 | – |
| 17β-сальвинорин J | 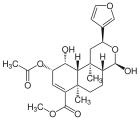 | – | – | C23ЧАС30О8 | 434,49 г · моль−1 | 1157894-85-3 | – |
Связанные соединения
В поисках полезной биологической активности несколько синтетических и полусинтетический аналоги были подготовлены к учебе. Полусинтетические аналоги включают этоксиметиловый эфир сальвинорина B и метоксиметиловый эфир сальвинорина B. Полностью синтетические аналоги включают геркинорин.
Несколько производные может быть удобно получен из сальвинорина B. Большинство производных являются селективными. каппа опиоид агонисты как с сальвинорином А, хотя некоторые из них даже более эффективны, с наиболее мощным соединением 2-этоксиметил сальвинорин B в десять раз сильнее, чем сальвинорин А. Некоторые производные, такие как геркинорин, снижают действие каппа-опиоидов и вместо этого действуют как мю опиоид агонисты.[1][2][3][4]
22-тиоцианато-сальвинорин А примечателен своим функциональная избирательность.[5] 2-метоксиметил сальвинорин B в семь раз более эффективен, чем сальвинорин А в отношении KOPr в анализах GTP-γS.[6]
Многие другие терпеноиды были выделены из Сальвия дивинорум, включая классы дивинаторинов и сальвиницинов. Ни одно из этих соединений не показало значительного (субмикромолярного) сродства к каппа-опиоидным рецепторам, и нет никаких доказательств того, что они способствуют психоактивности растения.[7][8]
Рекомендации
- ^ Манро Т.А.; Дункан К.К.; Xu W; Ван Ю; Лю-Чен LY; Карлезон WA; Коэн BM; Беген С (2008). «Стандартные защитные группы создают мощные и селективные κ-опиоиды: алкоксиметиловые эфиры сальвинорина B». Биоорганическая и медицинская химия. 16 (3): 1279–86. Дои:10.1016 / j.bmc.2007.10.067. ЧВК 2568987. PMID 17981041.
- ^ Holden KG; Tidgewell K; Marquam A; Ротман РБ; Navarro H; Присинзано Т.Э. (2007). «Синтетические исследования дитерпенов неоклеродана из Сальвия дивинорум: освоение 1 позиции ». Письма по биоорганической и медицинской химии. 17 (22): 6111–5. Дои:10.1016 / j.bmcl.2007.09.050. ЧВК 2111044. PMID 17904842.
- ^ Lee DY; Он М; Лю-Чен LY; Ван Ю; Li JG; Xu W; Ma Z; Карлезон WA; Коэн Б. (2006). «Синтез и фармакологические исследования in vitro новых C (4) -модифицированных аналогов сальвинорина A». Письма по биоорганической и медицинской химии. 16 (21): 5498–502. Дои:10.1016 / j.bmcl.2006.08.051. PMID 16945525.
- ^ Беген С; Ричардс MR; Li JG; Ван Ю; Xu W; Лю-Чен LY; Карлезон WA; Коэн Б.М. (2006). «Синтез и оценка in vitro аналогов сальвинорина A: влияние конфигурации на C (2) и замещение на C (18)». Письма по биоорганической и медицинской химии. 16 (17): 4679–85. Дои:10.1016 / j.bmcl.2006.05.093. PMID 16777411.
- ^ Уайт К., Робинсон Дж. Э., Чжу Х. и др. (2014). «Агонист k-опиоидных рецепторов, связанный с G-белком, RB-64 является анальгетиком с уникальным спектром активности in vivo». J. Pharmacol. Exp. Ther. 352 (1): 98–109. Дои:10.1124 / jpet.114.216820. ЧВК 4279099. PMID 25320048.
- ^ Wang, Y .; Chen, Y .; Xu, W .; Ли, Д .; Ma, Z; Rawls, S .; Cowan, A .; Лю-Чен, Л. (2008). «2-метоксиметил-сальвинорин B является мощным агонистом каппа-опиоидных рецепторов с более длительным действием in vivo, чем сальвинорин А.» Журнал фармакологии и экспериментальной терапии. 324 (3): 1073–1083. Дои:10.1124 / jpet.107.132142. ЧВК 2519046. PMID 18089845.
- ^ Бигхэм АК; Манро Т.А.; Rizzacasa MA; Робинс-Браун Р.М. (2003). "Дивинаторины A-C, новые дитерпеноиды неоклеродана из контролируемого шалфея Сальвия дивинорум". Журнал натуральных продуктов. 66 (9): 1242–4. CiteSeerX 10.1.1.693.6690. Дои:10.1021 / np030313i. PMID 14510607.
- ^ Манро Т.А.; Rizzacasa MA (2003). "Сальвинорины D-F, новые дитерпеноиды неоклеродана из Сальвия дивинорум, и улучшенный метод выделения сальвинорина А ». Журнал натуральных продуктов. 66 (5): 703–5. Дои:10.1021 / np0205699. PMID 12762813.