WikiDer > Тест Эймса
В Тест Эймса широко используемый метод, который использует бактерии чтобы проверить, может ли данное химическое вещество вызывать мутации в ДНК тестового организма. Более формально это биологический анализ оценить мутагенный потенциал химических соединений.[1] Положительный тест указывает на то, что химическое вещество является мутагенным и поэтому может действовать как канцероген, потому что рак часто связан с мутация. Тест служит быстрым и удобным анализом для оценки канцерогенного потенциала соединения, поскольку стандартные анализы канцерогенов на мышах и крысах требуют много времени (на выполнение требуется от двух до трех лет) и дороги. Однако известны ложноположительные и ложноотрицательные результаты.[2]
Процедура была описана в серии статей в начале 1970-х гг. Брюс Эймс и его группа на Калифорнийский университет в Беркли.[3][4][5][6]
Общая процедура
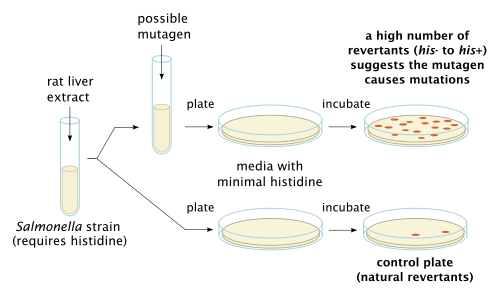
В тесте Эймса используются несколько штаммов бактерии. Сальмонелла тифимуриум которые несут мутации в генах, участвующих в гистидин синтез. Эти штаммы ауксотрофный мутанты, т.е. они нуждаются в гистидине для роста, но не могут его производить. Метод проверяет способность тестируемого вещества создавать мутации, которые приводят к возврату к «прототрофному» состоянию, так что клетки могут расти на среде без гистидина.
Штаммы тестера специально сконструированы для обнаружения либо сдвиг рамки (например, штаммы ТА-1537 и ТА-1538) или точка (например, штамм TA-1531) мутации в генах, необходимых для синтеза гистидина, так что мутагены, действующие через различные механизмы, могут быть идентифицированы. Некоторые соединения весьма специфичны, вызывая реверсию всего у одного или двух штаммов.[4] Штаммы-тестеры также несут мутации в генах, ответственных за липополисахарид синтез, делая клеточная стенка бактерий более проницаемых,[5] и в система эксцизионной репарации чтобы сделать тест более чувствительным.[6]
У более крупных организмов, таких как млекопитающие, есть метаболические процессы, которые потенциально могут превратить химическое вещество, считающееся не мутагенным, в то, что является мутагенным, или то, которое считается мутагенным, в другое.[7] Следовательно, чтобы более эффективно проверить мутагенность химического соединения по отношению к более крупным организмам, можно добавить ферменты печени крысы в попытке воспроизвести влияние метаболических процессов на соединение, тестируемое в тесте Эймса. Необязательно добавляют экстракт печени крысы для имитации эффекта метаболизм, так как некоторые соединения, например бензо [а] пирен, сами по себе не мутагены, а продукты их метаболизма.[3]
Бактерии распространяются на агар пластинка с небольшим количеством гистидина. Это небольшое количество гистидина в питательной среде позволяет бактериям расти в течение начального времени и иметь возможность мутировать. Когда гистидин истощается, выживут только те бактерии, которые мутировали, чтобы получить способность производить собственный гистидин. Планшет инкубируют 48 часов. Мутагенность вещества пропорциональна количеству наблюдаемых колоний.
Тест Эймса и канцерогены
Мутагены, идентифицированные с помощью теста Эймса, также являются возможными канцерогенами, и ранние исследования Эймса показали, что с помощью этого теста можно идентифицировать 90% известных канцерогенов.[8] Однако более поздние исследования показали идентификацию 50–70% известных канцерогенов.[нужна цитата] Тест был использован для идентификации ряда соединений, ранее использовавшихся в коммерческих продуктах, как потенциальных канцерогенов.[9] Примеры включают трис (2,3-дибромпропил) фосфат, который использовался в качестве антипирена в пластике и текстиле, таком как детская одежда для сна,[10] и фурилфурамид который использовался в качестве антибактериальной добавки к пище в Японии в 1960-х и 1970-х годах. Фактически, фурилфурамид ранее проходил испытания на животных, но более тщательные испытания после его выявления в тесте Эймса показали, что он канцерогенный.[11] Их положительные тесты привели к тому, что эти химические вещества были изъяты из использования в потребительских товарах.
Один интересный результат теста Эймса состоит в том, что кривая доза-ответ при различных концентрациях химического вещества почти всегда линейна,[8] что указывает на отсутствие пороговой концентрации для мутагенеза. Следовательно, это предполагает, что, как и в случае с радиацией, может нет безопасного порога на химические мутагены или канцерогены.[12][13] Однако некоторые предположили, что организмы могут переносить низкие уровни мутагенов из-за защитных механизмов, таких как Ремонт ДНК, и, таким образом, может существовать порог для определенных химических мутагенов.[14] Сам Брюс Эймс возражал против линейной экстраполяции зависимости доза-ответ от высокой дозы, используемой в тестах на канцерогенез в системах животных, на более низкую дозу химических веществ, обычно встречающихся при воздействии на человека, поскольку результаты могут быть ложноположительными из-за митогенный реакция, вызванная искусственно высокой дозой химикатов, используемых в таких тестах.[15][16] Он также предостерег от «истерии по поводу крошечных следов химикатов, которые могут или не могут вызывать рак», что «полностью устраняет основные риски, о которых вам следует знать».[17]
Тест Эймса часто используется в качестве одного из начальных скринингов для потенциальных лекарств для отсеивания возможных канцерогенов, и это один из восьми тестов, требуемых в соответствии с Закон о пестицидах (США) и один из шести тестов, требуемых в соответствии с Закон о контроле за токсичными веществами (СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ).[18]
Ограничения
Сальмонелла тифимуриум Прокариот, следовательно, не идеальная модель для человека. Печень крысы S9 фракция используется для имитации метаболических условий у млекопитающих, чтобы можно было оценить мутагенный потенциал метаболитов, образованных родительской молекулой в печеночной системе; однако существуют различия в метаболизме между людьми и крысами, которые могут влиять на мутагенность исследуемых химических веществ.[19] Следовательно, тест можно улучшить, используя фракцию S9 печени человека; его использование ранее ограничивалось его доступностью, но теперь оно доступно на коммерческой основе и, следовательно, может быть более целесообразным.[20] Адаптированный in vitro Модель была сделана для эукариотических клеток, например дрожжей.
Мутагены, идентифицированные в тесте Эймса, не обязательно должны быть канцерогенными, и необходимы дальнейшие тесты на любой потенциальный канцероген, идентифицированный в тесте. Лекарства, содержащие нитратную составляющую, иногда оказываются положительными на Эймса, когда они действительно безопасны. Нитратные соединения могут образовывать оксид азота, важная сигнальная молекула, которая может дать ложноположительный результат. Нитроглицерин является положительным примером Эймса, который все еще используется в лечении сегодня. Однако содержание нитратов в пищевых продуктах может быть восстановлено бактериальным действием до нитритов, которые, как известно, генерируют канцерогены, реагируя с аминами и амидами. Чтобы опровергнуть положительный результат теста Эймса, необходимы длительные токсикологические исследования и исследования результатов с такими соединениями.
Метод флуктуации

Первоначально тест Эймса был разработан с использованием чашек с агаром (метод включения чашек), как описано выше. С тех пор была разработана альтернатива выполнению теста Эймса, известная как «метод флуктуации». Этот метод аналогичен по концепции методу на основе агара, при котором бактерии добавляются в реакционную смесь с небольшим количеством гистидин, что позволяет бактериям расти и мутировать, возвращаясь к синтезу собственного гистидина. Включая индикатор pH, частота мутации подсчитывается в микропланшеты как количество лунок, изменивших цвет (вызванных падением pH из-за метаболических процессов размножающихся бактерий). Как и в случае с традиционным тестом Эймса, образец сравнивается с естественной фоновой скоростью обратной мутации, чтобы установить генотоксичность вещества. Метод флуктуации выполняется полностью в жидкой культуре и оценивается путем подсчета количества лунок, которые становятся желтыми от пурпурных в 96-луночных или 384-луночных микропланшетах.
В методе 96-луночного планшета частота мутации рассчитывается как количество лунок из 96, которые изменили цвет. Чашки инкубируют до пяти дней, при этом каждый день подсчитывают мутировавшие (желтые) колонии и сравнивают с фоновой скоростью обратной мутации с использованием установленных таблиц значимости для определения значимых различий между фоновой скоростью мутации и таковой для испытуемых. образцы.
В более упрощенном методе микрофлуктуации 384-луночного планшета частота мутации рассчитывается как количество лунок из 48, которые изменили цвет после 2 дней инкубации. Тестируемый образец анализируется при шести уровнях доз с одновременным нулевым (фоновым) контролем и положительным контролем, которые помещаются в один 384-луночный планшет. Анализ проводится в трех экземплярах для обеспечения статистической надежности. В нем используются тестируемые штаммы, рекомендованные Директивой ОЭСР 471 (ауксотрофы гистидина и ауксотрофы триптофана).
Метод флуктуации сравним с традиционным методом наливных планшетов с точки зрения чувствительности и точности, однако он имеет ряд преимуществ: для него требуется меньше исследуемого образца, он имеет простую колориметрическую конечную точку, подсчитывая количество положительных лунок из возможных. 96 или 48 лунок занимает гораздо меньше времени, чем подсчет отдельных колоний на чашке с агаром. Доступно несколько коммерческих комплектов. В большинстве наборов есть расходные компоненты, готовые к использованию, в том числе лиофилизированные бактерии, а тесты можно проводить с помощью многоканальных пипеток. Метод флуктуации также позволяет тестировать большие объемы водных образцов (до 75% об. / Об.), Повышая чувствительность и расширяя его применение для низкоуровневых мутагенов окружающей среды.[21]
Рекомендации
- ^ Мортельманс К., Зейгер Э. (ноябрь 2000 г.). «Анализ мутагенности Ames Salmonella / микросом». Мутационные исследования. 455 (1–2): 29–60. Дои:10.1016 / S0027-5107 (00) 00064-6. PMID 11113466.
- ^ Чарнли Джи (2002). «Тест Эймса». Энциклопедия общественного здоровья. eNotes.com. Архивировано из оригинал 4 февраля 2009 г.. Получено 2014-05-02.
- ^ а б Эймс Б.Н., Дерстон В.Е., Ямасаки Э., Ли Ф.Д. (август 1973 г.). «Канцерогены - это мутагены: простая тест-система, объединяющая гомогенаты печени для активации и бактерии для обнаружения». Труды Национальной академии наук Соединенных Штатов Америки. 70 (8): 2281–5. Дои:10.1073 / пнас.70.8.2281. ЧВК 433718. PMID 4151811.
- ^ а б Эймс Б.Н., Гурни Э.Г., Миллер Д.А., Бартч Х. (ноябрь 1972 г.). «Канцерогены как мутагены сдвига рамки считывания: метаболиты и производные 2-ацетиламинофлуорена и других канцерогенов ароматических аминов». Труды Национальной академии наук Соединенных Штатов Америки. 69 (11): 3128–32. Дои:10.1073 / pnas.69.11.3128. ЧВК 389719. PMID 4564203.
- ^ а б Эймс Б.Н., Ли Ф.Д., Дерстон В.Е. (март 1973 г.). «Улучшенная бактериальная тест-система для обнаружения и классификации мутагенов и канцерогенов». Труды Национальной академии наук Соединенных Штатов Америки. 70 (3): 782–6. Дои:10.1073 / пнас.70.3.782. ЧВК 433358. PMID 4577135.
- ^ а б Макканн Дж., Спингарн Н.Э., Кобори Дж., Эймс Б.Н. (март 1975 г.). «Обнаружение канцерогенов как мутагенов: штаммы бактериальных тестеров с плазмидами R-фактора». Труды Национальной академии наук Соединенных Штатов Америки. 72 (3): 979–83. Дои:10.1073 / pnas.72.3.979. ЧВК 432447. PMID 165497.
- ^ Хартвелл Л., Голдберг М., Худ Л., Рейнольдс А., Сильвер Л. (2011). Генетика: от генов к геномам (4-е изд.). Нью-Йорк: Макгроу-Хилл. ISBN 978-0-07-352526-6. OCLC 317623365.
- ^ а б Макканн Дж., Чой Э., Ямасаки Э., Эймс Б.Н. (декабрь 1975 г.). «Обнаружение канцерогенов как мутагенов в тесте на сальмонеллу / микросомы: анализ 300 химических веществ». Труды Национальной академии наук Соединенных Штатов Америки. 72 (12): 5135–9. Дои:10.1073 / пнас.72.12.5135. ЧВК 388891. PMID 1061098.
- ^ Эймс Б.Н. (Май 1979 г.). «Выявление химических веществ в окружающей среде, вызывающих мутации и рак» (PDF). Наука. 204 (4393): 587–93. Дои:10.1126 / science.373122. JSTOR 1748159. PMID 373122.
- ^ Привал MJ, McCoy EC, Gutter B, Rosendranz HS (январь 1977 г.). «Трис (2,3-дибромпропил) фосфат: мутагенность широко применяемого антипирена». Наука. 195 (4273): 76–8. Дои:10.1126 / science.318761. PMID 318761.
- ^ Хаяцу, Хирока (1991), Мутагены в продуктах питания: обнаружение и профилактика, CRC Press, стр. 286 стр., ISBN 978-0-8493-5877-7
- ^ Тисдейл А. (2011). Генотоксические примеси: стратегии идентификации и контроля. Вили-Блэквелл. ISBN 978-0-470-49919-1.
- ^ Тубиана М (сентябрь 1992 г.). «Канцерогенный эффект от воздействия малых доз канцерогенов». Британский журнал промышленной медицины. 49 (9): 601–5. Дои:10.1136 / oem.49.9.601. ЧВК 1039303. PMID 1390264.
- ^ Дженкинс Г.Дж., Доак С.Х., Джонсон Г.Е., Квик Э., Уотерс Э.М., Парри Дж. М. (ноябрь 2005 г.). «Существуют ли пороговые значения доза-ответ для генотоксичных алкилирующих агентов?». Мутагенез. 20 (6): 389–98. Дои:10.1093 / mutage / gei054. PMID 16135536.
- ^ Forman D (август 1991 г.). «Эймс, тест Эймса и причины рака». BMJ. 303 (6800): 428–9. Дои:10.1136 / bmj.303.6800.428. ЧВК 1670593. PMID 1912830.
- ^ Эймс Б.Н., Голд Л.С. (октябрь 1990 г.). «Химический канцерогенез: слишком много канцерогенов для грызунов». Труды Национальной академии наук Соединенных Штатов Америки. 87 (19): 7772–6. Дои:10.1073 / пнас.87.19.7772. ЧВК 54830. PMID 2217209.
- ^ Твомбли Р. (сентябрь 2001 г.). «Федеральный доклад о канцерогенности представляет новый список номинантов». Журнал Национального института рака. 93 (18): 1372. Дои:10.1093 / jnci / 93.18.1372. PMID 11562386.
- ^ Фермер ПБ, Уокер Дж. М. (2006). Молекулярная основа рака. Издательство Кригер. ISBN 978-0-7099-1044-2.
- ^ Хакура А., Сузуки С., Сато Т. (январь 1999 г.). «Преимущество использования S9 печени человека в тесте Эймса». Мутационные исследования. 438 (1): 29–36. Дои:10.1016 / с 1383-5718 (98) 00159-4. PMID 9858674.
- ^ Хакура А, Сузуки С, Сато Т (2004). «Улучшение теста Эймса с использованием препарата S9 печени человека». В Yan Z, Caldwell G (ред.). Оптимизация в открытии лекарств: методы in vitro. Методы фармакологии и токсикологии. Humana Press. ISBN 978-1-58829-332-9.
- ^ Bridges BA (ноябрь 1980 г.). «Флуктуационный тест». Архив токсикологии. 46 (1–2): 41–4. Дои:10.1007 / BF00361244. PMID 7235997. S2CID 23769437.
дальнейшее чтение
- Филлипсон, Кэролайн Э .; Иоаннидес, Костас (1 марта 1989 г.). «Метаболическое действие полициклических ароматических углеводородов на мутагены в тесте Эймса различными видами животных, включая человека». Мутационные исследования / Фундаментальные и молекулярные механизмы мутагенеза. 211 (1): 147–151. Дои:10.1016/0027-5107(89)90115-2. ISSN 0027-5107. PMID 2493576.
- Маккиннелл Р.Г. (06.11.2015). Понимание, профилактика и борьба с раком человека: исторические труды и жизнь Элизабет Каверт Миллер и Джеймса А. Миллера. БРИЛЛ. ISBN 9789004286801.
- Claxton LD, Umbuzeiro GD, DeMarini DM (ноябрь 2010 г.). «Анализ мутагенности сальмонелл: стетоскоп генетической токсикологии для 21 века». Перспективы гигиены окружающей среды. 118 (11): 1515–22. Дои:10.1289 / ehp.1002336. ЧВК 2974687. PMID 20682480.