WikiDer > Ацетат цинка
 | |
| Имена | |
|---|---|
| Название ИЮПАК Ацетат цинка | |
| Другие имена Уксусная кислота, цинковая соль Уксусная кислота, соль цинка (II) Дикарбометоксицинк Диацетат цинка | |
| Идентификаторы | |
3D модель (JSmol) |
|
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.008.338 |
| Номер E | E650 (усилитель вкуса) |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Характеристики | |
| Zn (CH3COO)2(ЧАС2O)2 (дигидрат) | |
| Молярная масса | 219,50 г / моль (дигидрат) 183,48 г / моль (безводный) |
| Внешность | Белое твердое вещество (все формы) |
| Плотность | 1,735 г / см3 (дигидрат) |
| Температура плавления | Разлагается при 237 ° C (459 ° F; 510 K) (дигидрат теряет воду при 100 ° C) |
| Точка кипения | разлагается |
| 43 г / 100 мл (20 ° C, дигидрат) | |
| Растворимость | 1,5 г / 100 мл (метанол) |
| −101.0·10−6 см3/ моль (+2 H2O) | |
| Структура | |
| октаэдрический (дигидрат) | |
| четырехгранный | |
| Фармакология | |
| A16AX05 (ВОЗ) | |
| Опасности | |
| Главный опасности | умеренно токсичный |
| R-фразы (устарело) | R22 R36 R50 / 53 |
| S-фразы (устарело) | S26 S60 S61 |
| Родственные соединения | |
Другой анионы | Хлорид цинка |
Другой катионы | Ацетат меди (II) |
Родственные соединения | Основной ацетат бериллия |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Ацетат цинка это соль с формула Zn (CH3CO2)2, который обычно встречается как дигидрат Zn (CH3CO2)2· 2H2О. И гидрат, и безводный формы представляют собой бесцветные твердые вещества, которые обычно используются в химическом синтезе и в качестве пищевых добавок. Ацетаты цинка получают под действием уксусная кислота на карбонат цинка или же цинк металл. При использовании в качестве пищевая добавка, он имеет Номер E E650.
Использует
Диетические и лечебные применения
Ацетат цинка использовался в леденцы для лечения насморка.[1] Ацетат цинка также можно использовать для лечения дефицита цинка.[2] В качестве ежедневной пероральной добавки он используется для подавления абсорбции меди организмом в рамках лечения Болезнь Вильсона.[3] Ацетат цинка также продается как вяжущее средство в форме мази, лосьона для местного применения или в сочетании с антибиотиком, таким как эритромицин для местного лечения прыщей.[4] Обычно он продается как мазь от зуда для местного применения.
Промышленное применение
Промышленные применения включают консервирование древесины, производство других солей цинка, полимеров, производство ацетат этила, как краситель едкий, и аналитический реагент. Он используется на коммерческих атомных электростанциях в качестве ингибитора гальванического покрытия на трубопроводах первичной воды.
Основные свойства и конструкции
В безводном ацетате цинка цинк координирован с четырьмя атомами кислорода, образуя тетраэдрическое окружение, затем эти тетраэдрические многогранники соединяются между собой ацетатными лигандами с образованием ряда полимерных структур.[5][6][7] Напротив, большинство диацетатов металлов содержат металлы в октаэдрической координации с бидентатными ацетатными группами.
В дигидрате ацетата цинка цинк является октаэдрическим, в котором обе ацетатные группы являются бидентатными.[8][9]
Основной ацетат цинка
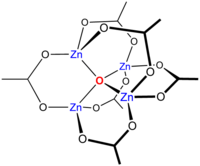
Нагрев Zn (CH3CO2)2 в вакууме приводит к потере уксусный ангидрид, оставляя остаток основного ацетата цинка с формулой Zn4O (CH3CO2)6. Этот кластерное соединение имеет четырехгранный структура, показанная ниже. Этот вид очень похож на соответствующий бериллий соединение, хотя оно немного расширено с расстояниями Zn-O ~ 1,97 против ~ 1,63 Å для Быть4O (OAc)6.[10]
Смотрите также
- Основной ацетат бериллия - изоструктурный
Рекомендации
- ^ «Цинк - информационный бюллетень для специалистов в области здравоохранения». Управление диетических добавок Национального института здоровья США. 11 февраля 2016 г.. Получено 15 ноября, 2018.
- ^ Вегмюллер, Рита; Тай, Фабиан; Зедер, Кристоф; Брнич, Марица; Харрелл, Ричард Ф. (2014). «Поглощение цинка молодыми взрослыми из дополнительного цитрата цинка сопоставимо с таковым из глюконата цинка и выше, чем из оксида цинка». Журнал питания. 144 (2): 132–136. Дои:10.3945 / jn.113.181487. ЧВК 3901420. PMID 24259556.
- ^ «Болезнь Вильсона». NIDDK. Июль 2014 г. В архиве из оригинала на 2016-10-04. Получено 15 ноября, 2018.
- ^ Schachner, L .; Eaglstein, W .; Kittles, C .; Мерц, П. (1990). «Актуальная терапия эритромицином и цинком от прыщей». Журнал Американской академии дерматологии. 22 (2, ч. 1): 253–60. Дои:10.1016 / 0190-9622 (90) 70034-ф. PMID 2138176.
- ^ Clegg, W .; Литтл, И. Р .; Страуган, Б. П. (15 декабря 1986 г.). «Моноклинный безводный ацетат цинка (II)». Acta Crystallographica Раздел C. 42 (12): 1701–1703. Дои:10.1107 / S010827018609087X.
- ^ Хэ, Хуншань (15 ноября 2006 г.). «Новый моноклинный полиморф безводного ацетата цинка». Acta Crystallographica Раздел E. 62 (12): m3291 – m3292. Дои:10.1107 / S1600536806046678.
- ^ Capilla, A. V .; Аранда, Р. А. (1979). "Безводный ацетат цинка (II) (CH3-COO)2Zn ». Связь с кристаллической структурой. 8: 795–797.
- ^ van Niekerk, J. N .; Schoening, F. R. L .; Талбот, Дж. Х. (10 сентября 1953 г.). «Кристаллическая структура дигидрата ацетата цинка, Zn (CH3COO) 2.2H2O». Acta Crystallographica. 6 (8): 720–723. Дои:10.1107 / S0365110X53002015.
- ^ Ишиока, Т .; Мурата, А .; Kitagawa, Y .; Накамура, К. Т. (15 августа 1997 г.). «Дигидрат ацетата цинка (II)». Acta Crystallographica Раздел C. 53 (8): 1029–1031. Дои:10.1107 / S0108270197004484.
- ^ Koyama, H .; Сайто, Ю. (1954). «Кристаллическая структура оксиацетата цинка, Zn4O (CH3COO)6". Бык. Chem. Soc. Jpn. 27 (2): 112–114. Дои:10.1246 / bcsj.27.112.