WikiDer > Йодид кадмия
 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Иодид кадмия (II) | |
| Другие имена Дииодид кадмия | |
| Идентификаторы | |
3D модель (JSmol) | |
| ChemSpider | |
| ECHA InfoCard | 100.029.294 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| CdI2 | |
| Молярная масса | 366,22 г / моль |
| Внешность | кристаллы от белого до бледно-желтого |
| Плотность | 5,640 г / см3, твердый |
| Температура плавления | 387 ° С (729 ° F, 660 К) |
| Точка кипения | 742 ° С (1368 ° F, 1015 К) |
| 787 г / л (0 ° С) 847 г / л (20 ° С) 1250 г / л (100 ° С) | |
| Растворимость | растворим в этиловый спирт, ацетон, эфир и аммиак |
| -117.2·10−6 см3/ моль | |
| Структура | |
| Тригональный, hP3, космическая группа п3м1, №164 | |
| восьмигранный | |
| Опасности | |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| H301, H331, H351, H373, H400, H410 | |
| P260, P280, P301 + 330 + 331, P310, P304 + 340, P311, P403 + 233 | |
| NFPA 704 (огненный алмаз) | |
| NIOSH (Пределы воздействия на здоровье в США): | |
PEL (Допустимо) | [1910.1027] TWA 0,005 мг / м3 (как Cd)[1] |
REL (Рекомендуемые) | Ca[1] |
IDLH (Непосредственная опасность) | Ca [9 мг / м3 (как Cd)][1] |
| Родственные соединения | |
Другой анионы | фторид кадмия хлорид кадмия бромид кадмия |
Другой катионы | йодид цинка иодид ртути (II) |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Йодид кадмия, CdI2, представляет собой химическое соединение кадмий и йод. Он примечателен своим Кристальная структура, что характерно для соединений вида MX2 с сильным поляризация последствия.
Подготовка
Иодид кадмия получают путем добавления металлического кадмия или его оксида, гидроксида или карбоната к йодистоводородная кислота.
Также соединение можно получить путем нагревания кадмия с йодом.
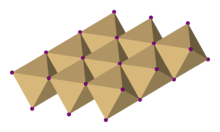
Кристальная структура
В йодиде кадмия йодид анионы образуют гексагональную плотноупакованную структуру, в то время как кадмий катионы заполните все октаэдрические узлы чередующимися слоями. Полученная структура представляет собой слоистую решетку. Эта же базовая структура встречается во многих других соли и минералы. Йодид кадмия в основном ионно связанный но с частичным ковалентный персонаж.[2]
Кристаллическая структура иодида кадмия является прототипом, на котором можно рассматривать кристаллические структуры многих других соединений. Соединения с любой из следующих характеристик имеют тенденцию принимать CdI2 структура:[нужна цитата]
- Йодиды умеренно поляризационных катионы; бромиды и хлориды сильно поляризующих катионов
- Гидроксиды дикатионов, то есть соединений с общей формулой M (OH)2
- Сульфиды, селениды и теллуриды (халькогениды) тетракатов, т.е. соединений общей формулы MX2, где X = S, Se, Te
Рекомендации
- ^ а б c Карманный справочник NIOSH по химической опасности. "#0087". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. С. 1211–1212. ISBN 978-0-08-037941-8.

