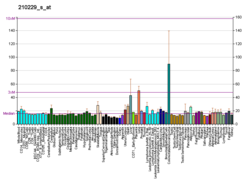
WikiDer > Колониестимулирующий фактор гранулоцитов-макрофагов
| Колониестимулирующий фактор гранулоцитов-макрофагов | |||||||||
|---|---|---|---|---|---|---|---|---|---|
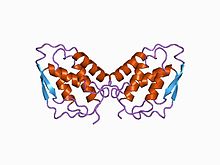 трехмерная структура рекомбинантный колониестимулирующий фактор гранулоцитов-макрофагов человека (rhGM_CSF) | |||||||||
| Идентификаторы | |||||||||
| Символ | GM_CSF | ||||||||
| Pfam | PF01109 | ||||||||
| Pfam клан | CL0053 | ||||||||
| ИнтерПро | IPR000773 | ||||||||
| PROSITE | PDOC00584 | ||||||||
| SCOP2 | 2gmf / Объем / СУПФАМ | ||||||||
| |||||||||
 | |
| Клинические данные | |
|---|---|
| Код УВД | |
| Идентификаторы | |
| |
| Количество CAS | |
| DrugBank | |
| ChemSpider |
|
| Химические и физические данные | |
| Формула | C639ЧАС1006N168О196S8 |
| Молярная масса | 14434.54 г · моль−1 |
| | |
Колониестимулирующий фактор гранулоцитов-макрофагов (GM-CSF), также известный как колониестимулирующий фактор 2 (CSF2), это мономерный гликопротеин секретно макрофаги, Т-клетки, тучные клетки, естественные клетки-киллеры, эндотелиальные клетки и фибробласты который функционирует как цитокин. В фармацевтический аналоги встречающегося в природе GM-CSF называются сарграмостим и молграмостим.
В отличие от колониестимулирующий фактор гранулоцитов, который специально продвигает нейтрофил пролиферации и созревания GM-CSF влияет на большее количество типов клеток, особенно на макрофаги и эозинофилы.[5]
Функция
GM-CSF - это мономерный гликопротеин который функционирует как цитокин - это лейкоцит фактор роста.[6] GM-CSF стимулирует стволовые клетки производить гранулоциты (нейтрофилы, эозинофилы, и базофилы) и моноциты. Моноциты выходят из кровообращения и мигрируют в ткань, после чего созревают в макрофаги и дендритные клетки. Таким образом, это часть невосприимчивый/воспалительный каскад, в результате чего активация небольшого количества макрофагов может быстро привести к увеличению их числа, что имеет решающее значение для борьбы с инфекционное заболевание.
GM-CSF также оказывает некоторое влияние на зрелые клетки иммунной системы. К ним относятся, например, усиление миграции нейтрофилов и изменение рецепторов, экспрессируемых на поверхности клеток.[7]
Сигналы GM-CSF через преобразователь сигналов и активатор транскрипции, STAT5.[8] В макрофагах также было показано, что он передает сигнал через STAT3. Цитокин активирует макрофаги, препятствуя выживанию грибов. Он вызывает депривацию свободного внутриклеточного цинка и увеличивает производство активные формы кислорода что приводит к грибковому голоданию по цинку и токсичности.[9] Таким образом, GM-CSF способствует развитию иммунной системы и способствует защите от инфекций.
GM-CSF также играет роль в эмбриональном развитии, функционируя как эмбриокин продуцируется репродуктивным трактом.[10]
Генетика
Ген человека локализован в непосредственной близости от интерлейкин 3 ген в Т помощник связанный с типом 2 кластер генов цитокинов в области хромосомы 5q31, который, как известно, связан с интерстициальными делециями в 5q- синдром и острый миелолейкоз. GM-CSF и IL-3 разделены изолирующим элементом и, таким образом, регулируются независимо.[11] Другие гены в кластере включают гены, кодирующие интерлейкины 4, 5, и 13.[12]
Гликозилирование
Колониестимулирующий фактор гранулоцитов-макрофагов человека гликозилирован в зрелой форме.
История
GM-CSF был впервые клонирован в 1985 году, и вскоре после этого были изготовлены три потенциальных лекарственных продукта с использованием рекомбинантная ДНК технологии: молграмостим был сделан в кишечная палочка и не гликозилирован, сарграмостим был произведен в дрожжах, имеет лейцин вместо пролина в положении 23 и несколько гликозилирован, и Regramostim был произведен в клетках яичников китайского хомячка (СНО) и имеет большее гликозилирование, чем сарграмостим. Степень гликозилирования влияет на то, как организм взаимодействует с лекарством и как лекарство взаимодействует с организмом.[13]
В это время, Институт генетики, Inc. работал над молграмостимом,[14] Иммунекс работал над сарграмостим (Лейкин),[15] и Sandoz работал над реграмостимом.[16]
Молграмостим был в конечном итоге совместно разработан и продан компаниями Novartis и Schering-Plough под торговым названием Leucomax для использования в восстановлении уровня лейкоцитов после химиотерапии, а в 2002 году Novartis продала свои права компании Schering-Plough.[17][18]
Сарграмостим был одобрен FDA США в 1991 году для ускорения восстановления лейкоцитов после аутологичного трансплантация костного мозга под торговым наименованием Leukine, и прошел через несколько рук, в результате Genzyme[19] который впоследствии был приобретен Санофи. Leukine в настоящее время принадлежит Partner Therapeutics (PTx).
Imlygic был одобрен FDA США в октябре 2015 года.[20] и в декабре 2015 года EMA в качестве онколитической виротерапии, коммерциализированной Amgen Inc. вирус онколитического герпеса, названный Талимоген лахерпарепвец, был генетически сконструирован для экспрессии человеческого GM-CSF с использованием аппарата опухолевых клеток.[21]
Направления исследований
GM-CSF содержится в больших количествах в суставах с ревматоидный артрит и блокируя GM-CSF как биологическая мишень может уменьшить воспаление или повреждение. Некоторые препараты (например, отилимаб) разрабатываются для блокировать GM-CSF.[22] У пациентов в критическом состоянии GM-CSF был испытан в качестве терапии иммуносупрессии критических заболеваний и показал многообещающее восстановление. моноцит[23] и нейтрофил[24] функции, хотя влияние на исходы для пациентов в настоящее время неясно и требует более крупных исследований.
Смотрите также
- КОЕ-ГМ
- Рецептор колониестимулирующего фактора гранулоцитов-макрофагов
- Филграстим (Нейпоген, а колониестимулирующий фактор гранулоцитов (G-CSF) аналог)
- Пегфилграстим (Неуласта, а ПЭГилированный форма филграстим)
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000164400 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000018916 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ «Ссылка на Mouse PubMed:». Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Корень РК, Дейл округ Колумбия (март 1999 г.). «Гранулоцитарный колониестимулирующий фактор и гранулоцитарно-макрофагальный колониестимулирующий фактор: сравнения и потенциал для использования в лечении инфекций у пациентов без нейтропении». Журнал инфекционных болезней. 179 Suppl 2 (Suppl 2): S342–52. Дои:10.1086/513857. PMID 10081506.
- ^ Франсиско-Крус А., Агилар-Сантелизес М., Рамос-Эспиноса О, Мата-Эспиноса Д., Маркина-Кастильо Б., Барриос-Паян Дж., Эрнандес-Пандо Р. (январь 2014 г.). «Гранулоцитарно-макрофагальный колониестимулирующий фактор: не просто еще один гемопоэтический фактор роста». Медицинская онкология. 31 (1): 774. Дои:10.1007 / s12032-013-0774-6. PMID 24264600. S2CID 24452892.
- ^ Gasson JC (март 1991 г.). «Молекулярная физиология гранулоцитарно-макрофагального колониестимулирующего фактора». Кровь. 77 (6): 1131–45. Дои:10.1182 / blood.V77.6.1131.1131. PMID 2001448.
- ^ Voehringer D (октябрь 2012 г.). «Модуляция базофилов цитокиновой инструкцией». Европейский журнал иммунологии. 42 (10): 2544–50. Дои:10.1002 / eji.201142318. PMID 23042651.
- ^ Субраманиан Виньеш К., Ландеро Фигероа Дж. А., Поролло А., Карузо Дж. А., Дипе Г. С. (октябрь 2013 г.). «Гранулоцитарный макрофаг-колониестимулирующий фактор, индуцированный секвестрацией Zn, увеличивает супероксид макрофага и ограничивает выживание внутриклеточных патогенов». Иммунитет. 39 (4): 697–710. Дои:10.1016 / j.immuni.2013.09.006. ЧВК 3841917. PMID 24138881.
- ^ Хансен П.Дж., Доббс КБ, Деникол А.С. (сентябрь 2014 г.). «Программирование предимплантационного эмбриона с помощью фактора 2, стимулирующего колонию эмбриокинов». Наука о воспроизводстве животных. 149 (1–2): 59–66. Дои:10.1016 / j.anireprosci.2014.05.017. PMID 24954585.
- ^ Bowers SR, Mirabella F, Calero-Nieto FJ, Valeaux S, Hadjur S., Baxter EW, Merkenschlager M, Cockerill PN (апрель 2009 г.). «Консервативный инсулятор, который рекрутирует CTCF и когезин, существует между тесно связанными, но дивергентно регулируемыми генами интерлейкина-3 и генов фактора, стимулирующего колонию гранулоцитов-макрофагов». Молекулярная и клеточная биология. 29 (7): 1682–93. Дои:10.1128 / MCB.01411-08. ЧВК 2655614. PMID 19158269.
- ^ «Ген Entrez: колониестимулирующий фактор 2 CSF2 (гранулоцит-макрофаг)».
- ^ Армитаж Дж. О. (декабрь 1998 г.). «Новые области применения рекомбинантного человеческого фактора, стимулирующего колонии гранулоцитов-макрофагов» (PDF). Кровь. 92 (12): 4491–508. Дои:10.1182 / кровь.V92.12.4491. PMID 9845514.
- ^ «Молграмостим». AdisInsight. Получено 3 апреля 2018.
- ^ Персонал (май 2008 г.). «Назад в будущее: скоро появится оригинальный жидкий лейкин®» (PDF). Обзор онкологического бизнеса. Архивировано из оригинал (PDF) на 2016-08-25. Получено 2016-08-29.
- ^ Хусейн А.М., Росс М., Вреденбург Дж., Мейзенберг Б., Харс В., Гилберт С., Петрос В. П., Конильо Д., Курцберг Дж., Рубин П. (ноябрь 1995 г.). «Эффекты гранулоцитарно-макрофагального колониестимулирующего фактора, продуцируемого в клетках яичников китайского хомячка (реграмостим), Escherichia coli (молграмостим) и дрожжах (сарграмостим) на праймирование клеток-предшественников периферической крови для использования с аутологичным костным мозгом после высокодозной химиотерапии». Европейский журнал гематологии. 55 (5): 348–56. Дои:10.1111 / j.1600-0609.1995.tb00713.x. PMID 7493686. S2CID 25424116.
- ^ «Пресс-релиз: Novartis Oncology уделяет особое внимание ключевым факторам роста». Novartis через SEC Edgar. 30 октября 2002 г.
- ^ «Научные выводы и основания для внесения поправок в сводку характеристик продукта, представленную EMEA» (PDF). EMA CPMP. 27 июня 2000 г.
- ^ «Завод Bayer Healthcare Pharmaceuticals, округ Снохомиш, штат Вашингтон». Pharmaceutical-technology.com. Получено 12 ноября 2011.
- ^ Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. «ИМЛИГИК (талимоген лахерпарепвек)». fda.gov. Получено 17 декабря 2019.
- ^ Андтбака, Роберт Х. И .; Kaufman, Howard L .; Колличио, Фрэнсис; Аматруда, Томас; Зензер, Нил; Чесни, Джейсон; Delman, Keith A .; Spitler, Lynn E .; Пузанов, Игорь; Agarwala, Sanjiv S .; Милхем, Мохаммед; Кранмер, Ли; Курти, Брендан; Льюис, Карл; Росс, Меррик; Гатри, Трой; Linette, Gerald P .; Дэниелс, Грегори А .; Харрингтон, Кевин; Миддлтон, Марк Р .; Miller, Wilson H .; Загер, Джонатан С .; Йе, Инин; Яо, Бин; Ли, Ай; Долман, Сьюзен; Вандервальде, Ари; Гансерт, Дженнифер; Гроб, Роберт С. (2015-09-01). «Талимоген Лахерпарепвек увеличивает стойкость ответа у пациентов с запущенной меланомой». Журнал клинической онкологии. 33 (25): 2780–2788. Дои:10.1200 / JCO.2014.58.3377. ISSN 1527-7755. PMID 26014293.
- ^ Deiß A, Brecht I, Haarmann A, Buttmann M (март 2013 г.). «Лечение рассеянного склероза моноклональными антителами: обновление 2013 года». Экспертный обзор нейротерапии. 13 (3): 313–35. Дои:10.1586 / ern.13.17. PMID 23448220. S2CID 169334.
- ^ Майзель, Кристиан; Schefold, Joerg C .; Пшовски, Рене; Бауманн, Тихо; Хетцгер, Катрин; Грегор, Ян; Вебер-Карстенс, Штеффен; Хаспер, Дитрих; Кех, Дидье (01.10.2009). «Гранулоцитарно-макрофагальный колониестимулирующий фактор для устранения связанной с сепсисом иммуносупрессии: двойное слепое рандомизированное плацебо-контролируемое многоцентровое исследование». Американский журнал респираторной медицины и реанимации. 180 (7): 640–648. Дои:10.1164 / rccm.200903-0363OC. ISSN 1535-4970. PMID 19590022.
- ^ Пиндер, Эмма М .; Рострон, Энтони Дж .; Hellyer, Thomas P .; Рушо-Спарагано, Мария-Элен; Скотт, Джонатан; Macfarlane, James G .; Вискомб, Сара; Widdrington, John D .; Рой, Алистер И. (31.07.2018). «Рандомизированное контролируемое исследование GM-CSF у пациентов в критическом состоянии с нарушенным фагоцитозом нейтрофилов». Грудная клетка. 73 (10): thoraxjnl – 2017–211323. Дои:10.1136 / thoraxjnl-2017-211323. ISSN 1468-3296. ЧВК 6166597. PMID 30064991.
внешняя ссылка
- Официальный сайт гентаура
- Официальный сайт Leukine
- Гранулоциты-макрофаги + колониестимулирующий фактор + фактор в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Обзор всей структурной информации, доступной в PDB за UniProt: P04141 (Гранулоцитарно-макрофагальный колониестимулирующий фактор) на PDBe-KB.