WikiDer > Фрагментация Гроба
В химия, а Фрагментация Гроба является реакция элиминации что нарушает нейтральный алифатический цепочка на три фрагмента: положительный ион охватывая атомы 1 и 2 ("электрофуга"), ненасыщенный нейтральный фрагмент, охватывающий позиции 3 и 4, а отрицательный ион ("нуклеофуга"), составляющие остальную часть цепочки.[1][2][3]
Например, положительный ион может быть карбений, карбоний или же ион ацилия; нейтральный фрагмент мог быть алкен, алкин, или же я добываю; а отрицательный фрагмент может быть тозил или же гидроксил ион:
Реакция названа в честь швейцарского химика. Кирилл А. Гроб.
С другой стороны, атом 1 может начинаться как анион, и в этом случае он становится нейтральным, а не превращается из нейтрального в катионный.
История
Ранним примером фрагментации является обезвоживание из ди (терт-бутил) метанол уступающий 2-метил-2-бутен и изобутен, реакция, описанная в 1933 г. Фрэнк К. Уитмор.[4] Эта реакция протекает с образованием вторичного карбокатион за которым следует реакция перегруппировки к более стабильному третичному карбокатиону и устранению т-бутил катион:
Альберт Эшенмозер в 1952 г. исследовал катализируемую основаниями фрагментацию некоторых бета-гидроксикетоны:[5]
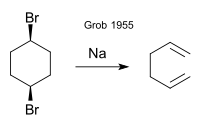
Оригинальная работа Grob (1955) касается формирования 1,5-гексадиен из СНГ- или же транс-1,4-дибромциклогексан по натрий металл:[1]
Согласно рецензентам Прантц и Мулцер (2010), название Grob fragmentation было выбрано «в более или менее вопиющем пренебрежении к более ранним вкладам».[6]
Механизм реакции
В механизм реакции варьируется в зависимости от реагента и условий реакции, при этом фрагментация происходит в согласованная реакция или происходить в два этапа с карбокатионный промежуточное звено, когда нуклеофуга уходит первым, или происходящее в два этапа с анионным промежуточным звеном, когда электрофуга уходит первой. Карбанионный путь более распространен и ему способствует стабильность образующегося катиона и способность нуклеофуги к уходящей группе. В случае циклических субстратов предпочтительная геометрия удаления - это сигма-связь, которая вытесняет уходящая группа быть противником, аналогично конформационный ориентации в механизме E2 реакции элиминации.
Примеры
Тапсигаргин из кетона Виланда – Мишера
Пример дробления типа Гроба в органический синтез это расширение Кетон Виланда-Мишера к тапсигаргин:[7]
В этой реакции снижение кетона 1 с борогидрид натрия дает алкоголь 2, который функционализирован мезилат 3 с мезилхлорид в пиридин. Тогда уменьшение Enone к аллиловый спирт 4 с три-терт-бутоксиалюминийгидрид в тетрагидрофуран с последующим гидроборирование с боран в THF дает боран 5 (для ясности отображается только один заместитель). Фрагментация Гроба на 6 происходит с метоксид натрия в метанол в рефлюкс. А метоксид группа атакует бор атом дает борат сложные фрагменты. Поскольку каждый атом бора может содержать три молекулы субстрата (R), конечным побочным продуктом бора является триметилборат
Другой пример - реакция фрагментации эпоксидного спирта как часть Общий синтез таксола Холтона.
аза-гробская фрагментация
3-аза-Гроба фрагментация это вариация, которая имеет место, когда электрофуга и нуклеофуга расположены в позициях 1 и 5 на вторичном или третичном амин цепь с азотом в положении 3.[8][9] Продукты реакции - электрофугальный фрагмент, я добываю, и нуклеофугальный фрагмент (такой как алкоголь).
Фрагментация 3-аза-Grob может происходить с несколькими различными нуклеофугами. В механизм реакции сообщалось, что оно начинается с восстановления амида, защищенного простым эфиром, с образованием вторичного спирта. Затем происходит согласованная стадия фрагментации с образованием продуктов реакции.
Было обнаружено, что объем реакции охватывает THF и тетрагидротиофен защитные группы с использованием различных гидридных агентов.[10]
Смотрите также
Рекомендации
- ^ а б Grob, C.A .; Бауманн, В. (1955). "Die 1,4-Eliminierung unter Fragmentierung". Helvetica Chimica Acta (на немецком). 38 (3): 594–610. Дои:10.1002 / hlca.19550380306.
- ^ Weyerstahl, P .; Маршалл, Х. (1991). «Реакции фрагментации». В Трост, Барри М.; Флеминг, Ян (ред.). Манипуляции с гетероатомом. Комплексный органический синтез: селективность, стратегия и эффективность в современной органической химии. 6 (1-е изд.). Амстердам: Pergamon Press. С. 1044–1065. ISBN 978-0-08-035929-8. Cite использует устаревший параметр
| editorlink1 =(помощь) - ^ Курти, Ласло; Чако, Барбара (2007). Стратегические применения названных реакций в органическом синтезе: предпосылки и подробные механизмы - 250 названных реакций. Амстердам: Эльзевир. ISBN 978-0-12-429785-2.
- ^ Уитмор, Фрэнк С.; Стали, Э. Э. (1933). «Общая основа внутримолекулярных перегруппировок. II. Дегидратация ди-терт-бутилкарбинол и превращение образующихся ноненов в триметилэтилен и изобутилен ». Журнал Американского химического общества. 55 (10): 4153–4157. Дои:10.1021 / ja01337a042.
- ^ Эшенмозер, А.; Фрей, А. (1952). "Uber die Spaltung des Mesylesters von 2-Methyl-2-oxymethyl-cyclopentanon mit Basen". Helvetica Chimica Acta (на немецком). 35 (5): 1660–1666. Дои:10.1002 / hlca.19520350532.
- ^ Пранц, Катрин; Мульцер, Иоганн (2010). "Синтетические применения карбонильной фрагментации Grob". Химические обзоры. 110 (6): 3741–3766. Дои:10.1021 / cr900386h. PMID 20163188.
- ^ Ley, S. V .; Антонелло, А .; Бальскус, Э. П .; Бут, Д. Т .; Christensen, S. B .; Cleator, E .; Золото, H .; Hogenauer, K .; Hunger, U .; Myers, R.M .; Оливер, С. Ф .; Simic, O .; Smith, M.D .; Sohoel, H .; Вулфорд, А. Дж. А. (2004). «Синтез тапсигаргинов». Труды Национальной академии наук. 101 (33): 12073–12078. Bibcode:2004ПНАС..10112073Л. Дои:10.1073 / pnas.0403300101. ЧВК 514437. PMID 15226504.
- ^ Ван, Джех-Дженг; Ху, Ван-Пин; Чунг, Хун-Вэй; Ван, Ли-Фанг; Сюй, Мэй-Хуэй (1998). "Новое и оригинальное расщепление амидной связи N-метоксиметилпирроло [2,1-c] [1,4] бензодиазепин-5,11-дионы путем восстановления гидрида посредством 3-аза-фрагментации Гроба ». Тетраэдр. 54 (43): 13149–13154. Дои:10.1016 / S0040-4020 (98) 00795-9.
- ^ Ван, Дже-Дженг; Ху, Ван-Пин (1999). "Новая 3-аза-гробовая фрагментация в восстановлении гидрида эфир-защищенных ароматических лактамов". Журнал органической химии. 64 (15): 5725–5727. Дои:10.1021 / jo990549k. PMID 11674651.
- ^ Ху, Ван-Пин; Ван, Дже-Дженг; Цай, Пей-Цзин (2000). "Новые примеры фрагментации 3-Аза-Гроба". Журнал органической химии. 65 (13): 4208–4209. Дои:10.1021 / jo000252i. PMID 10866646.