WikiDer > Метил трифторметансульфонат
 | |
 | |
| Имена | |
|---|---|
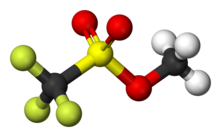
| Название ИЮПАК Метил трифторметансульфонат | |
| Другие имена Трифторметансульфоновая кислота, метиловый эфир Трифликовая кислота, метиловый эфир, метилтрифлат | |
| Идентификаторы | |
3D модель (JSmol) | |
| ChemSpider | |
| ECHA InfoCard | 100.005.793 |
PubChem CID | |
| UNII | |
| |
| |
| Свойства | |
| C2ЧАС3F3О3S | |
| Молярная масса | 164.10 г · моль−1 |
| Внешность | Бесцветная жидкость |
| Плотность | 1,496 г / мл |
| Температура плавления | -64 ° С (-83 ° F, 209 К) |
| Точка кипения | 100 ° С (212 ° F, 373 К) |
| Гидролизует | |
| Опасности | |
| Основной опасности | Коррозионный |
| R-фразы (устарело) | R10-R34 |
| S-фразы (устарело) | S26-S36 / 37/39-S45 |
| точка возгорания | 38 ° С (100 ° F, 311 К) |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Метил трифторметансульфонат, также обычно называемый метилтрифлат и сокращенно MeOTf, это органическое соединение с формула CF3ТАК2ОСН3. Это бесцветная жидкость, которая находит применение в органической химии в качестве сильнодействующего вещества. метилирование агент.[1] Соединение тесно связано с метилфторсульфонат (ФСО2ОСН3). Хотя сообщений о смертельных исходах среди людей еще не поступало, в то время как несколько случаев были зарегистрированы для метилфторсульфоната (LC50 (крыса, 1 час) = 5 частей на миллион) ожидается, что метилтрифлат будет иметь аналогичную токсичность на основании имеющихся данных.[1]
Синтез
Метилтрифлат коммерчески доступен, однако его также можно получить в лаборатории путем обработки диметилсульфат с трифликовой кислотой.[2]
- CF3ТАК2ОН + (СН3O)2ТАК2 → CF3ТАК2ОСН3 + CH3OSO2ОЙ
Реактивность
Соединение интенсивно гидролизуется при контакте с водой:
- CF3ТАК2ОСН3 + H2O → CF3ТАК2ОН + СН3ОЙ
Метилирование
Один из рейтингов метилирующих агентов: (CH3)3О+ > CF3ТАК2ОСН3 ≈ FSO2ОСН3 > (CH3)2ТАК4 > CH3я.[2] Метилтрифлат будет алкилировать многие функциональные группы, которые являются очень бедными нуклеофилами, такие как альдегиды, амиды, и нитрилы. Не метилирует бензол и объемные 2,6-ди-терт-бутилпиридин.[1] Его способность метилировать N-гетероциклы эксплуатируются в определенных снятие защиты схемы.[3]
Катионная полимеризация
Метилтрифлат инициирует живая катионная полимеризация из лактид[4] и другие лактоны, включая β-пропиолактон, ε-капролактон и гликолид.[5]
Циклические карбонаты, подобные триметиленкарбонат и неопентиленкарбонат (5,5-диметил-1,3-диоксан-2-он) можно полимеризовать до соответствующих поликарбонатов.[6] 2-алкил-2-оксазолины, например 2-этил-2-оксазолин, также полимеризуются до поли (2-алкилоксазолина) s.[7]
Смотрите также
использованная литература
- ^ а б c Роджер У. Олдер; Джастин Г. Э. Филлипс; Лицзюнь Хуан; Сюэфэй Хуан (2005). «Метилтрифторметансульфонат». Энциклопедия реагентов для органического синтеза. Дои:10.1002 / 047084289X.rm266m.pub2. ISBN 0471936235.
- ^ а б Стэнг, Питер Дж .; Ханак, Майкл; Субраманиан, Л. Р. (1982). «Перфторалкансульфоновые эфиры: методы получения и применения в органической химии». Синтез. 1982 (2): 85–126. Дои:10.1055 / с-1982-29711. ISSN 0039-7881.
- ^ Альберт И. Мейерс; Марк Э. Фланаган (1998). «2,2'-Диметокси-6-формилбифенил». Органический синтез.; Коллективный объем, 9, п. 258
- ^ Рангель, Ирма; Рикар, Мишель; Рикар, Ален (1994). «Полимеризация L-лактида и ε-капролактона в присутствии метилтрифторметансульфоната». Макромолекулярная химия и физика. 195 (9): 3095–3101. Дои:10.1002 / macp.1994.021950908.
- ^ Jonté, J. Michael; Дансинг, Рут; Кричелдорф, Ханс Р. (1985). «Полилактоны. 4. Катионная полимеризация лактонов с помощью алкилсульфонатов». Журнал макромолекулярной науки: Часть A - Химия. 22 (4): 495–514. Дои:10.1080/00222338508056616. ISSN 0022-233X.
- ^ Kricheldorf, Hans R .; Веген-Шульц, Беттина; Йенсен, Йорг (1998). «Катионная полимеризация алифатических циклокарбонатов». Макромолекулярные симпозиумы. 132 (1): 421–430. Дои:10.1002 / masy.19981320139.
- ^ Гласснер, Матиас; D’hooge, Dagmar R .; Янг Пак, Джин; Van Steenberge, Paul H.M .; Monnery, Bryn D .; Рейнер, Мария-Франсуаза; Хугенбум, Ричард (2015). «Систематическое исследование алкилсульфонатных инициаторов катионной полимеризации с раскрытием цикла 2-оксазолинов с выявлением оптимальных комбинаций мономеров и инициаторов». Европейский Полимерный Журнал. 65: 298–304. Дои:10.1016 / j.eurpolymj.2015.01.019. HDL:1854 / LU-5924229.
