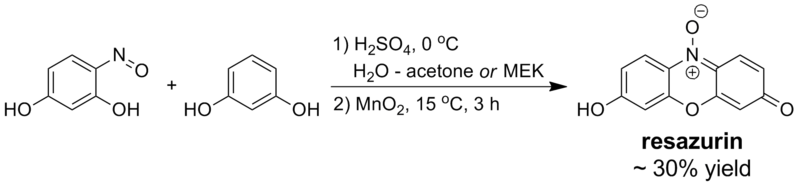WikiDer > Ресазурин
 | |
| Имена | |
|---|---|
| Название ИЮПАК 7-гидрокси-10-оксидофеноксазин-10-иум-3-он | |
| Другие имена Alamar Blue, Vybrant, UptiBlue, диазорезорцин, азорезорцин, резазоин, резазурин | |
| Идентификаторы | |
| |
3D модель (JSmol) | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.008.171 |
PubChem CID | |
| UNII | |
| |
| Характеристики | |
| C12ЧАС7NО4 | |
| Молярная масса | 229.191 г · моль−1 |
| растворимый | |
| Опасности | |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| H315, H319, H335 | |
| P261, P305 + 351 + 338 | |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Ресазурин (7-Гидрокси-3ЧАС-феноксазин-3-он 10-оксид) представляет собой феноксазин краситель это слабо флуоресцентный, нетоксичный, проницаемые для клеток и чувствительные к окислительно-восстановительному потенциалу.[2][3] Ресазурин имеет синий к фиолетовый цвет (в pH > 6.5) и используется в микробиологический, сотовый, и ферментативный анализы, потому что это может быть необратимо уменьшенный к розовый-цветный и очень флуоресцентный резоруфин (7-Гидрокси-3ЧАС-феноксазин-3-он). При примерно нейтральном pH резоруфин можно определить визуально по его розовому цвету или по флуориметрия, с максимумом возбуждения 530-570 нм и максимумом испускания 580-590 нм[4].
Когда раствор, содержащий резоруфин, подвергается восстановительным условиям (Eчас <-110 мВ), почти весь резоруфин обратимо восстанавливается до прозрачный нефлуоресцентный дигидрорезоруфин (син. гидрорезоруфин) и раствор становится прозрачным ( окислительно-восстановительный потенциал пары резоруфин / дигидрорезоруфин составляет -51 мВ по сравнению с стандартный водородный электрод при pH 7,0). Когда Eчас этого же раствора увеличивается, дигидрорезоруфин снова окисляется до резоруфина, и эту обратимую реакцию можно использовать для мониторинга, если окислительно-восстановительный потенциал питательная среда остается на достаточно низком уровне для анаэробные организмы.
| Ресазурин (индикатор pH) | ||
| ниже pH 6,5 | выше pH 6.5 | |
| 6.5 | ⇌ | 6.5 |
Раствор резазурина имеет одно из самых высоких значений из известных Крефта. двуцветность индекс.[5] Это означает, что он имеет большое изменение воспринимаемого цвета. оттенок когда толщина или концентрация наблюдаемого образца увеличивается или уменьшается.
Обычно резазурин коммерчески доступен в виде натрий соль.
Приложения для определения жизнеспособности клеток
Резазурин превращается в резоруфин под действием аэробного дыхания метаболически активных клеток, и его можно использовать как индикатор жизнеспособности клеток. Впервые он был использован для количественного определения содержания бактерий в молоке Пешем и Зиммертом в 1929 году.[6] Его можно использовать для обнаружения наличия жизнеспособных клеток в культурах клеток млекопитающих.[7] Первоначально он был коммерчески представлен под торговой маркой Alamar Blue (Trek Diagnostic Systems, Inc), а теперь также доступен под другими названиями, такими как AB assay, Vybrant (Молекулярные зонды) и UptiBlue (Интерхим).
Анализы на основе резазурина показывают отличную корреляцию с эталонными анализами жизнеспособности, такими как формазананализы на основе (МТТ/ XTT) и методы на основе тритированного тимидина.[8] Низкая токсичность делает его пригодным для более длительных исследований, его применяли для животных клеток, бактерий и грибов. [8] за анализы клеточной культуры такие как подсчет клеток, выживаемость клеток и распространение клеток.[9].
Чтобы заменить стандартный анализ живых / мертвых, резазурин также можно объединить с хемилюминесцентными анализами, такими как анализы цитокинов, анализы каспазы для измерения апоптоза или анализы репортеров для измерения экспрессии гена или белка.[8]
Необратимая реакция резазурина на резоруфин пропорционально аэробному дыханию.[10]
Ресазурин как колориметрический анализ жизнеспособности клеток
Резазурин применяют как флуоресцентный анализ жизнеспособности клеток - Ресазурин не флуоресцирует при воздействии зеленого света
Ресазурин как флуоресцентный анализ жизнеспособности клеток - Ресоруфин флуоресцирует при воздействии зеленого света
Другие приложения
Резазурин эффективно снижает митохондрии, что делает полезным также оценивать митохондриальный метаболический Мероприятия.
Обычно при наличии НАДФН-дегидрогеназа или же НАДН-дегидрогеназа как фермент, НАДФН или же НАДН является восстановителем, превращающим резазурин в резоруфин. Следовательно, систему резазурин / диафораза / NADPH можно использовать для определения уровня NADH, NADPH или диафоразы, а также любой биохимической или ферментной активности, которая участвует в биохимической реакции, генерирующей NADH или NADPH.[11][12][13][14][15]
Резазурин можно использовать для анализа L-глутамат, достигая чувствительности 2,0 пмоль на лунку в 96-луночном планшете.[16]
Резазурин также можно использовать для измерения аэробного биоразложения органических веществ, обнаруженных в сточных водах.[17]
Резазурин используется для измерения количества аэробного дыхания в ручьях.[18] Поскольку большая часть аэробного дыхания происходит в русле потока, превращение резазурина в резоруфин также является мерой количества обмена между столбом воды и слоем потока.
Синтез
Резазурин получают путем катализируемой кислотой конденсации между резорцин и 4-нитрозорезорцин с последующим окислением промежуточного продукта оксид марганца (IV):
Обработка сырого продукта реакции избытком карбонат натрия дает натриевую соль резазурина, которая обычно является коммерческой формой красителя. Проведение стадии конденсации в спиртах возможно, но приводит к более низким выходам продукта; в чистой воде или уксусной кислоте реакция протекает неудовлетворительно.[19]
Связанные красители
10-ацетил-3,7-дигидроксифеноксазин (также известный как Amplex Red), структурно связанный с резазурином, реагирует с H2О2 в стехиометрии 1: 1 для получения того же побочного продукта резоруфина (используется во многих анализах, например пероксидаза хрена (HRP), или NADH, NADPH с помощью ферментов).[20][21]
7-этоксирезоруфин, представляет собой соединение, используемое в качестве субстрата при измерении цитохром P450 (CYP1A1) индукции с использованием этоксирезоруфин-O-деэтилаза (EROD) аналитическая система в клеточной культуре и образцах окружающей среды, произведенная в ответ на воздействие арильные углеводороды. Соединение катализируется ферментом с образованием того же флуоресцентного продукта, резоруфина.[нужна цитата]
1,3-дихлор-7-гидрокси-9,9-диметилакридин-2 (9ЧАС)-один (Краситель DDAO), флуоресцентный краситель, используемый для мечения олигонуклеотидов.[нужна цитата]
Рекомендации
- ^ «Ресазурин | C12H7NO4 | ChemSpider».
- ^ Bueno, C .; Villegas, M. L .; Бертолотти, S.G .; Previtali, C.M .; Neumann, M. G .; Энсинас, М. В. (2002). «Взаимодействие в возбужденном состоянии резазурина и резоруфина с водными растворами аминосина. Фотофизика и фотохимическая реакция». Фотохимия и фотобиология. 76 (4): 385–90. Дои:10.1562 / 0031-8655 (2002) 0760385TESIOR2.0.CO2. PMID 12405144.
- ^ Хаггерти, Рой; Марти, Евгения; Аргерих, Альба; Шиллер, Даниэль фон; Гримм, Нэнси Б. (2009). «Ресазурин как« умный »индикатор для количественной оценки метаболически активного временного накопления в речных экосистемах». Журнал геофизических исследований: биогеонауки. 114 (G3). Дои:10.1029 / 2008JG000942. HDL:10261/38263. ISSN 2156-2202.
- ^ Чен, Дж. Л., Стил, Т. У., и Стаки, Д. К. (2015). Моделирование и применение быстрого флуоресцентного анализа биотоксичности при анаэробном пищеварении. Наука об окружающей среде и технологии, 49 (22), 13463-13471.http://pubs.acs.org/doi/10.1021/acs.est.5b03050
- ^ Крефт, Само; Крефт, Марко (2009). «Количественная оценка дихроматизма: характеристика цвета прозрачных материалов». Журнал Оптического общества Америки A. 26 (7): 1576–81. Bibcode:2009JOSAA..26.1576K. Дои:10.1364 / JOSAA.26.001576. PMID 19568292.
- ^ Pesch, K. L .; Зиммерт, У. (1929). «Комбинированные тесты на лактозу и галактозу с помощью ферментативных реакций». Milchw. Форш. 8: 551.
- ^ Аноопкумар-Дуки, S; Кэри, JB; Конере, Т; О'Салливан, Э; Ван Пелт, ФН; Оллшир, А (2005). «Ресазуриновый анализ радиационного ответа в культивируемых клетках». Британский журнал радиологии. 78 (934): 945–7. Дои:10.1259 / bjr / 54004230. PMID 16177019.
- ^ а б c Анализ жизнеспособных клеток UptiBlue техническое руководство
- ^ Курин, Елена; Атанасов, Атанас; Донат, Оливер; Хейсс, Эльке; Дирш, Верена; Надь, Милан (2012). «Изучение синергии ингибирующего потенциала полифенолов красного вина на пролиферацию гладкомышечных клеток сосудов». Planta Medica. 78 (8): 772–8. Дои:10.1055 / с-0031-1298440. PMID 22499559.
- ^ Гонсалес-Пинсон, Рикардо; Хаггерти, Рой; Мирольд, Дэвид Д. (2012). «Измерение аэробного дыхания в речных экосистемах с помощью системы резазурин-резоруфин» (PDF). Журнал геофизических исследований. 117 (G3): G00N06. Bibcode:2012JGRG..117.0N06G. Дои:10.1029 / 2012JG001965.
- ^ Шахангян, С .; Ash, K. O .; Роллинз, Д. Э. (1984). «Ферментативный метод анализа формиата в плазме человека». Журнал аналитической токсикологии. 8 (6): 273–6. Дои:10.1093 / jat / 8.6.273. PMID 6549198.
- ^ Hanson, NQ; Фрейер, EF (1983). «Влияние белка на определение общего количества желчных кислот в сыворотке». Клиническая химия. 29 (1): 171–5. Дои:10.1093 / Clinchem / 29.1.171. PMID 6571720.
- ^ Де Йонг, Дональд У .; Вудлиф, Уильям Г. (1977). «Флуориметрический анализ дегидрогеназ табачного листа с резазурином». Biochimica et Biophysica Acta (BBA) - Энзимология. 484 (2): 249–59. Дои:10.1016 / 0005-2744 (77) 90081-Х. PMID 20957.
- ^ Барнс, Стивен; Спенни, Джерри Г. (1980). «Стехиометрия nadh-оксидоредуктазы реакции для определения дегидрогеназы». Clinica Chimica Acta. 107 (3): 149–54. Дои:10.1016/0009-8981(80)90442-8. PMID 6893684.
- ^ Winartasaputra, H; Маллет, В.Н. Куан, СС; Гильбо, GG (1980). «Флуорометрическое и колориметрическое ферментативное определение триглицеридов (триацилглицеринов) в сыворотке крови». Клиническая химия. 26 (5): 613–7. Дои:10.1093 / Clinchem / 26.5.613. PMID 6894889.
- ^ Чепмен, Джастин; Чжоу, Минцзе (1999). «Микропланшетные флуориметрические методы для ферментативного определения l-глутамата: применение для измерения l-глутамата в образцах пищевых продуктов». Analytica Chimica Acta. 402 (1–2): 47–52. Дои:10.1016 / S0003-2670 (99) 00533-4.
- ^ Jouanneau, S .; Recoules, L .; Дюран, М.Дж .; Букабаче, А .; Picot, V .; Primault, Y .; Lakel, A .; Сенгелин, М .; Barillon, B .; Туанд, Г. (2014). «Методы оценки биохимической потребности в кислороде (БПК): обзор». Водные исследования. 49: 62–82. Дои:10.1016 / j.watres.2013.10.066. PMID 24316182.
- ^ Хаггерти, Рой; Марти, Евгения; Аргерих, Альба; Фон Шиллер, Даниэль; Гримм, Нэнси Б. (2009). «Ресазурин как« умный »индикатор для количественной оценки метаболически активного временного накопления в речных экосистемах». Журнал геофизических исследований. 114 (G3): G03014. Bibcode:2009JGRG..114.3014H. Дои:10.1029 / 2008JG000942. HDL:10261/38263.
- ^ A США 2376283 A, Фрэнк Шорт Уоллес и Питер Оксли, «Красители, подходящие для использования в качестве индикаторов», опубликовано 1945-05-15, передано Boots Pure Drug Co Ltd.
- ^ Чжоу М., Диву З., Панчук-Волошина Н. и др. Стабильное нефлуоресцентное производное резоруфина для флуорометрического определения следовых количеств перекиси водорода: приложения для определения активности НАДФН-оксидазы фагоцитов и других оксидаз. Анальная биохимия 253 162-168 (1997)
- ^ «10-Ацетил-3,7-дигидроксифеноксазин (CAS 119171-73-2) | Cayman Chemical».