WikiDer > Дефицит мевалонаткиназы
| Дефицит мевалонаткиназы | |
|---|---|
| Другие имена | Мевалоновая ацидурия[1] и Синдром гипер иммуноглобина D (HIDS) |
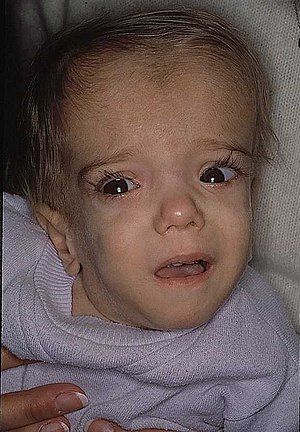 | |
| Пациент с дефицитом мевалонаткиназы в возрасте 21 месяца с характерными черепно-лицевыми особенностями. | |
| Специальность | Гематология, неврология, иммунология, медицинская генетика, эндокринология |
Дефицит мевалонаткиназы (MKD), является аутосомный рецессивный [2] нарушение обмена веществ что нарушает биосинтез из холестерин и изопреноиды.[3]
Для него характерен повышенный уровень иммуноглобина D в крови.Мевалонаткиназа (MVK) - фермент, участвующий в биосинтезе холестеринов и изопреноидов, и он необходим для превращения мевалоната в мевалонат-5-фосфат в присутствии Mg2 +. MKD возникает из-за мутации в гене, кодирующем мевалонаткиназу, что приводит к снижению или недостаточной активности этого фермента. Из-за этого недостатка Мевалонатная кислота Тяжесть МКД зависит от уровня этого дефицита, при этом синдром гипериммуноглобулинемии D (впервые описанный как HIDS в 1984 г.) менее тяжелый, но более распространенный, а мевалоновая ацидурия (MVA ); более тяжелая, но более редкая форма.
Генетика
Дефицит мевалонаткиназы передается по наследству аутосомно-рецессивный Это означает, что ребенок должен унаследовать дефектную копию гена от обоих родителей, чтобы пострадать.[2] Это пример потери функции мутация. Ген, кодирующий мевалонаткиназу, состоит из 10 экзоны в локусе 12q14.[4] Охарактеризовано около 63 патологических вариантов последовательности гена.[нужна цитата] Наиболее распространенными из них являются V377I, I268T, H20P / N и P167L, присутствующие у 70% больных.[4]
Иммуноглобин D
Иммуноглобулин D (IgD) - это белок, вырабатываемый определенным типом белых кровяных телец. Есть пять классов Иммуноглобин как IgG, IgA и IgM, IgE и IgD. Они играют важную роль в иммунной системе. Функция IgD до сих пор не ясна.
Существует связь между MKD и интерлейкином 1beta (IL-Iβ). Существует повышенная секреция IL-1β, а дефицит мевалонаткиназы в MKD, скорее всего, опосредован дефектным белком. пренилирование (Пренилирование относится к добавлению гидрофобных остатков к белкам)] и нестериновые изопреноиды, такие как фарнезилпирофосфат (FPP) или геранилгеранилпирофосфат (GGPP) связаны с целевым белком, который влияет на активность и местоположение клетки. На модели человеческого моноцитарного МКД было обнаружено, что дефицит GGPP приводит к избыточной продукции IL-1β и дефектному пренилированию RhoA. Это вызывает повышенный уровень Rac1 и PKB, который влияет на GTPases и B7-Glycoproteins. Ранее было установлено, что Rac1Путь / PI3K / PKB был связан с патогенезом MKD. Инактивация RhoA действует как индуктор транскрипции мРНК IL-1β независимо от активности NLRP3 или каспазы-1. Из-за дефектного RhoA образуется дефектный митохондрии (удлиненные и неустойчивые) в клетке. Если митохондрия повреждена, она очищается в клетке за счет механизма аутофагия. Но в МКД нарушается клиренс дефектных митохондрий из цитозоля. В результате митохондриальная ДНК начинает накапливаться в цитозоле, который связывает и активирует NLRP3, который отвечает за выработку IL-1β. Активация может быть прямой или косвенной. Его также можно активировать активные формы кислорода (ROS).[5] Известно, что моноциты и макрофаги также производят более высокие уровни фактора некроза опухоли альфа (TNF-α), интерлейкин 6 (Ил-6) Кроме как ИЛ-Iβ [5] Во время приступов лихорадки (лихорадки) и во время приступов С - реактивный белок (CRP) также увеличивается.[4] СРБ выделяется печенью, что вызывает воспаление [13].
Синдром гипер-IgD
Гипериммуноглобулинемия D с возвратной лихорадкой это синдром периодической лихорадки первоначально описанный в 1984 г. терапевт Йос ван дер Меер,[6] затем в Лейденский университет Медицинский центр. В мире описано не более 300 случаев. В настоящее время он признан аллельным вариантом MKD.[7]
Признаки и симптомы
HIDS является одним из многих синдромы периодической лихорадки. Для него характерны приступы высокая температура, артралгия, поражения кожи в том числе циклические язвы во рту, и понос. Особенности лаборатории включают острофазовый ответ (повышенный CRP и СОЭ) и заметно приподнят IgD (и часто IgA), хотя описаны случаи с нормальным IgD.[8]
В основном это описано в Нидерланды и Франция, хотя в международный регистр включен ряд случаев из других стран.[8]
В дифференциальный диагноз включает в себя лихорадка неизвестного происхождения, семейная средиземноморская лихорадка (FMF) и семейная лихорадка Хиберниан (или ассоциированный с приемом TNFα периодический синдром / TRAPS).[8]
Причина
Практически у всех людей с синдромом есть мутации в ген за мевалонаткиназа, который является частью Путь HMG-CoA редуктазы, важный сотовый метаболический путь.[9][10] В самом деле, подобные приступы лихорадки (но с нормальным уровнем IgD) были описаны у пациентов с мевалоновой ацидурией. врожденная ошибка обмена веществ теперь рассматривается как тяжелая форма HIDS.[8]
Патофизиология
Неизвестно, каким образом мутации мевалонаткиназы вызывают приступы лихорадки, хотя предполагается, что другие продукты пути биосинтеза холестерина, пренилирование цепи (геранилгераниол и фарнезол) может сыграть роль.[8]
Диагностика
Дефицит мевалонаткиназы вызывает накопление мевалоновая кислота в мочав результате недостаточной активности фермента мевалонаткиназа[11] (АТФ: мевалонат-5-фосфотрансфераза; EC 2.7.1.36).
Расстройство было впервые описано в 1985 году.[12]
Классифицируется как врожденная ошибка обмена веществ, дефицит мевалонаткиназы обычно приводит к отставание в развитии, гипотония, анемия, гепатоспленомегалия, различный дисморфический Особенности, умственная отсталость, общий неспособность процветать и несколько других функций.

Уход
МКД не лечится. Но воспаление и другие эффекты можно до некоторой степени уменьшить.
- Препараты, нацеленные на ИЛ-1, можно использовать для уменьшения эффектов расстройства. Анакинра является антагонистом рецепторов ИЛ-1. Анакинра связывает рецептор IL-1, предотвращая действие как IL-1α, так и IL-1β, и было доказано, что она снижает клиническое и биохимическое воспаление при МКД. Он может эффективно снизить частоту, а также тяжесть воспалительных атак при ежедневном использовании. Недостатки при использовании этого препарата - возникновение болезненной реакции в месте инъекции и, поскольку в ближайшем будущем прием препарата будет прекращен, у вас начнутся приступы лихорадки. (Обследован у больного 12 лет).
- Канакинумаб представляет собой моноклональное антитело длительного действия, направленное против IL-1β, которое, как было показано, эффективно снижает как частоту, так и тяжесть заболевания у пациентов, страдающих легкой и тяжелой МКБ, в отчетах о случаях и в серии наблюдательных случаев. Он снижает физиологические эффекты, но биохимический параметр все еще остается повышенным (Galeotti et al. Продемонстрировали, что он более эффективен, чем анакинра - 6 пациентов, страдающих МКД).
- Анти-TNF-терапия может быть эффективной при МКБ, но эффект в основном частичный, и неэффективность терапии и клиническое ухудшение часто описываются у пациентов, находящихся на лечении. инфликсимаб или этанерцепт.[5] Благоприятный эффект человеческого моноклонального антитела против TNFα адалимумаба был отмечен у небольшого числа пациентов с МКД.
- Большинству пациентов с МКБ помогает терапия анти-ИЛ-1. Однако также может возникнуть заболевание, резистентное к IL-1. Пример. тоцилизумаб (гуманизированное моноклональное антитело против рецептора интерлейкина-6 (ИЛ-6)). Этот препарат используется, когда пациенты не реагируют на Анакинру. (Shendi et al. Лечили молодую женщину, у которой Анакинра был неэффективен с тоцилизумаб). Было обнаружено, что он эффективен в снижении биохимического и клинического воспаления [30]. Stoffels et al. наблюдали снижение частоты и тяжести воспалительных атак, хотя после нескольких месяцев лечения у одного из этих двух пациентов постоянно проявлялись легкие воспалительные симптомы в отсутствие биохимических маркеров воспаления.
- Благотворное влияние трансплантация гемопоэтических стволовых клеток может использоваться при тяжелых состояниях недостаточности мевалонаткиназы (улучшение церебральной миелинизация на МРТ после трансплантация аллогенных стволовых клеток наблюдалось у одной девушки). Но трансплантация печени не повлияла на приступы лихорадки у этого пациента.[5]
Лечение HIDS
Канакинумаб одобрен для лечения HIDS и доказал свою эффективность.[13][14] Иммунодепрессанты этанерцепт[15] и Анакинра[16] также показали свою эффективность. Статины лекарства могут снижать уровень мевалоната и в настоящее время исследуются. В недавнем сообщении об одном случае бисфосфонаты были выделены как потенциальный терапевтический вариант.[17]
Эпидемиология
В мире менее 1 человека из 1 000 000 имеют HIDS [5]. 200 человек во всем мире действительно страдают от МКД.[4]
Дополнительные изображения
Смотрите также
Рекомендации
- ^ Онлайн-менделевское наследование в человеке (OMIM): 251170
- ^ а б «Дефицит мевалонаткиназы».
- ^ Манчини Дж., Филип Н., Шаброл Б., Диври П., Роллан М. О., Пинсар Н. (май – июнь 1993 г.). «Мевалоновая ацидурия у 3 братьев и сестер: новая узнаваемая метаболическая энцефалопатия». Педиатр. Neurol. 9 (3): 243–246. Дои:10.1016 / 0887-8994 (93) 90095-Т. PMID 8352861.
- ^ а б c d «Дефицит мевалонаткиназы».
- ^ а б c d Малдерс-Мандерс, CM; Саймон, А (2015). «Синдром гипер-IgD / дефицит мевалонаткиназы: что нового?». Семин Иммунопатол. 37 (4): 371–6. Дои:10.1007 / s00281-015-0492-6. ЧВК 4491100. PMID 25990874.
- ^ ван дер Меер JW, Vossen JM, Radl J, et al. (Май 1984 г.). «Гипериммуноглобулинемия D и периодическая лихорадка: новый синдром». Ланцет. 1 (8386): 1087–90. Дои:10.1016 / S0140-6736 (84) 92505-4. PMID 6144826.
- ^ «Запись OMIM - * 251170 - МЕВАЛОНАТНАЯ КИНАЗА; MVK». omim.org.
- ^ а б c d е Дрент Дж. П., Ван дер Меер Дж. В. (декабрь 2001 г.). «Наследственная периодическая лихорадка». N. Engl. J. Med. 345 (24): 1748–57. Дои:10.1056 / NEJMra010200. PMID 11742050.
- ^ Дрент Дж. П., Куиссет Л., Грато Дж. И др. (Июнь 1999 г.). «Мутации в гене, кодирующем мевалонаткиназу, вызывают гипер-IgD и синдром периодической лихорадки. Международная исследовательская группа по гипер-IgD». Nat. Genet. 22 (2): 178–81. Дои:10.1038/9696. PMID 10369262.
- ^ Хаутен С.М., Куис В., Дюран М. и др. (Июнь 1999 г.). «Мутации в MVK, кодирующем мевалонаткиназу, вызывают гипериммуноглобулинемию D и синдром периодической лихорадки». Nat. Genet. 22 (2): 175–7. Дои:10.1038/9691. PMID 10369261.
- ^ Бретон Мартинес-младший, Кановас Мартинес А., Касана Перес С., Эскрипа Алепус Дж., Хименес Васкес Ф. (октябрь 2007 г.). «Мевалоновая ацидурия: сообщение о двух случаях». J. Inherit. Метаб. Дис. 30 (5): 829. Дои:10.1007 / s10545-007-0618-7. PMID 17578678.
- ^ Berger R, Smit GP, Schierbeek H, Bijsterveld K, le Coultre R (октябрь 1985 г.). «Мевалоновая ацидурия: врожденная ошибка биосинтеза холестерина?». Clin. Чим. Acta. 152 (1–2): 219–222. Дои:10.1016/0009-8981(85)90195-0. PMID 4053401.
- ^ Aróstegui, JI; Антон, J .; Calvo, I .; Роблес, А .; Speziale, A .; Joubert, Y .; Junge, G .; Ягуэ, Дж. (01.01.2015). «Долгосрочная эффективность и безопасность канакинумаба при активном гипер-IgD-синдроме (HIDS): результаты открытого исследования». Детская ревматология. 13 (1): O58. Дои:10.1186 / 1546-0096-13-S1-O58. ISSN 1546-0096. ЧВК 4596954.
- ^ Козлова, А .; Мамзерова, Е .; Машан, А .; Щербина, А. (01.06.2014). «AB0918 Эффективность и безопасность лечения детей с ловушками и шкурами с помощью блокатора IL1 (CANAKINUMAB)». Анналы ревматических болезней. 73 (Приложение 2): 1103–1104. Дои:10.1136 / annrheumdis-2014-eular.3697. ISSN 0003-4967.
- ^ Такада, Кадзуки; Аксентиевич Ивона; Махадеван, Виджаябхану; Дин, Джейн А .; Келли, Ричард I .; Кастнер, Дэниел Л. (01.09.2003). «Благоприятный предварительный опыт применения этанерцепта у двух пациентов с гипериммуноглобулинемией D и синдромом периодической лихорадки». Артрит и ревматизм. 48 (9): 2645–2651. Дои:10.1002 / арт.11218. ISSN 0004-3591. PMID 13130485.
- ^ Риганте Д., Ансуини В., Бертони Б. и др. (Ноябрь 2006 г.). «Лечение анакинрой при гипериммуноглобулинемии D / синдроме периодической лихорадки». Ревматол. Int. 27 (1): 97–100. Дои:10.1007 / s00296-006-0164-x. PMID 16871408.
- ^ Кантарини, L; Витале, А; Magnotti, F; Lucherini, O.M .; Caso, F; Frediani, B; Галеацци, М; Риганте, Д. (2013). «Еженедельный пероральный прием алендроната при дефиците мевалонаткиназы». Журнал редких заболеваний Orphanet. 8: 196. Дои:10.1186/1750-1172-8-196. ЧВК 3880037. PMID 24360083.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
| Классификация |
|---|


