WikiDer > Плазомицин
 | |
| Клинические данные | |
|---|---|
| Произношение | pla "zoe mye 'sin |
| Торговые наименования | Земдри |
| Другие имена | АЧН-490, 6 '- (гидроксилэтил) -1- (HABA) -сисомицин |
| AHFS/Drugs.com | Монография |
| MedlinePlus | a618037 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Внутривенное вливание |
| Класс препарата | Аминогликозид |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| Лиганд PDB | |
| Химические и физические данные | |
| Формула | C25ЧАС48N6О10 |
| Молярная масса | 592.691 г · моль−1 |
| 3D модель (JSmol) | |
| |
| |
Плазомицин, продается под торговой маркой Земдри, является аминогликозидный антибиотик используется для лечения сложных инфекция мочеиспускательного канала.[1] С 2019 года это рекомендуется только для тех, для кого альтернативы не подходят.[1] Это дается инъекция в вену.[1]
Общие побочные эффекты включают: проблемы с почками, понос, тошнота и изменения артериального давления.[1] Другие серьезные побочные эффекты включают: потеря слуха, Clostridium difficile-ассоциированная диарея, анафилаксияи мышечная слабость.[1] Использование во время беременности может нанести вред ребенку.[1] Плазомицин снижает способность бактерий вырабатывать белок.[1]
Плазомицин был одобрен для медицинского применения в США в 2018 году.[2][3] Это на Список основных лекарственных средств Всемирной организации здравоохранения.[4]
Медицинское использование
Плазомицин одобрен США. Управление по контролю за продуктами и лекарствами (FDA) для взрослых с осложненными инфекциями мочевыводящих путей, включая пиелонефрит, вызванный кишечная палочка, Клебсиелла пневмонии, Протей мирабилис, или же Энтеробактерные клоакиу пациентов, у которых есть ограниченные альтернативные варианты лечения или их нет. Земдри - это внутривенная инфузия, вводимая один раз в день.[5][6][7][8] FDA отклонило одобрение для лечения инфекций кровотока из-за отсутствия продемонстрированной эффективности.[2]
Сообщается, что плазомицин демонстрирует in vitro синергетическая активность в сочетании с даптомицин или же цефтобипрол против метициллин-устойчивый Золотистый стафилококк, устойчивый к ванкомицину S. aureus и против Синегнойная палочка в сочетании с цефепим, дорипенем, имипенем или же пиперациллин / тазобактам.[9] Он также демонстрирует мощный in vitro активность по сравнению с устойчивостью к карбапенемам Acinetobacter baumannii.[10] Плазомицин не уступает меропенему.[11][12]
История
Препарат разработан биотехнологической компанией Achaogen. В 2012 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США предоставило быстрый трек обозначение для разработки и регуляторной экспертизы плазомицина.[13] FDA одобрило плазомицин для взрослых с осложненными ИМП и ограниченными альтернативными вариантами лечения или отсутствием их в 2018 году.[5] Achaogen не смогла найти устойчивый рынок для этого препарата и несколько месяцев спустя объявила о банкротстве.[14] Универсальная версия производится Cipla USA.[15]
Синтез
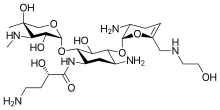
Это получено из сисомицин присоединением заместителя гидроксиаминомасляной кислоты в положении 1 и заместителя гидроксиэтила в положении 6 '.[16][9]
Имена
Плазомицин - это международное непатентованное название (ГОСТИНИЦА).[17]
Рекомендации
- ^ а б c d е ж грамм "Монография по сульфату плазомицина для профессионалов". Drugs.com. Американское общество фармацевтов систем здравоохранения. Получено 10 октября 2019.
- ^ а б «Лекарственные препараты, одобренные FDA: Zemdri». НАС. Управление по контролю за продуктами и лекарствами. Получено 28 июн 2018.
- ^ «Пакет одобрения лекарственных средств: Земдри (плазомицин)». НАС. Управление по контролю за продуктами и лекарствами. 5 июля 2018 г.. Получено 25 декабря 2019.
- ^ Всемирная организация здоровья (2019). Типовой список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г.. Женева: Всемирная организация здравоохранения. HDL:10665/325771. WHO / MVP / EMP / IAU / 2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ а б «Земдри (плазомицин) - плазомицин для инъекций». DailyMed. 30 июля 2020 г.. Получено 11 октября 2020.
- ^ «плазомицин (Rx)». Medscape. Получено 14 сентября 2019.
- ^ Brown T (3 мая 2018 г.). «Группа FDA рекомендует плазомицин для лечения ИМП, но не БСИ». Medscape. Получено 14 сентября 2019.
- ^ «BioCentury - FDA одобряет плазомицин для лечения ИМП, но не инфекций крови». www.biocentury.com. Получено 28 июн 2018.
- ^ а б Жанель Г.Г., Лоусон С.Д., Зеленицкий С.И. и др. (Апрель 2012 г.). «Сравнение аминогликозида плазомицина нового поколения с гентамицином, тобрамицином и амикацином». Экспертная оценка противоинфекционной терапии. 10 (4): 459–73. Дои:10.1586 / eri.12.25. PMID 22512755. S2CID 31496981.
- ^ Гарсиа-Сальгеро С., Родригес-Авиаль I, Пиказо Дж. Дж. И др. (Октябрь 2015 г.). "Может ли плазомицин один или в комбинации быть терапевтическим вариантом против устойчивых к карбапенемам" Acinetobacter baumannii?" (PDF). Противомикробные агенты Chemother. 59 (10): 5959–66. Дои:10.1128 / AAC.00873-15. ЧВК 4576036. PMID 26169398. Получено 27 апреля 2016.
- ^ Номер клинического исследования NCT02486627 для «Исследования плазмомицина по сравнению с меропенемом для лечения осложненной инфекции мочевыводящих путей (cUTI), включая острый пиелонефрит (AP) (EPIC)» на ClinicalTrials.gov
- ^ Wagenlehner FM, Cloutier DJ, Комиренко А.С. и др. (21 февраля 2019 г.). «Плазомицин для лечения осложненных инфекций мочевыводящих путей один раз в день». Медицинский журнал Новой Англии. 380 (8): 729–740. Дои:10.1056 / nejmoa1801467. ISSN 0028-4793. PMID 30786187. Сложить резюме – Центр исследований и политики в области инфекционных заболеваний (21 февраля 2019 г.).
- ^ «Achaogen объявляет о присвоении плазомицина статуса QIDP FDA» (Пресс-релиз). Achaogen, Inc. 8 января 2015 г.. Получено 27 апреля 2016 - через GlobeNewswire.
- ^ Джейкобс А. (25 декабря 2019 г.). «Кризис антибиотиков нависает над банкротством производителей лекарств». Нью-Йорк Таймс.
- ^ "Универсальная доступность Земдри". Drugs.com. Получено 26 декабря 2019.
- ^ Агген Дж. Б., Армстронг Е. С., Голдблюм А. А. и др. (Ноябрь 2010 г.). «Синтез и спектр неогликозида ACHN-490» (PDF). Противомикробные агенты Chemother. 54 (11): 4636–4642. Дои:10.1128 / AAC.00572-10. ЧВК 2976124. PMID 20805391.
- ^ «Международные непатентованные наименования фармацевтических субстанций (МНН). Рекомендуемые МНН: Список 68». Информация ВОЗ о лекарствах. Всемирная организация здоровья. 26 (3): 314. Сентябрь 2012 г.. Получено 27 апреля 2016.
дальнейшее чтение
- «Информационная информация FDA для заседания Консультативного комитета по противомикробным препаратам 2 мая 2018 г.» (PDF). НАС. Управление по контролю за продуктами и лекарствами. 2 мая 2018. Получено 14 сентября 2019.
- «Информационная информация по ахаогену для заседания Консультативного комитета по противомикробным препаратам 2 мая 2018 г.» (PDF). НАС. Управление по контролю за продуктами и лекарствами. 2 мая 2018. Получено 14 сентября 2019.
- «Исправления в информационном бюллетене по ахаогену для заседания Консультативного комитета по противомикробным препаратам 2 мая 2018 г.» (PDF). НАС. Управление по контролю за продуктами и лекарствами. 2 мая 2018. Получено 14 сентября 2019.
внешняя ссылка
- «Плазомицин». Портал информации о наркотиках. Национальная медицинская библиотека США.
- «Сульфат плазомицина». Портал информации о наркотиках. Национальная медицинская библиотека США.