WikiDer > Тиофен
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Тиофен | |||
| Другие имена Тиофуран Тиациклопентадиен Тиоле | |||
| Идентификаторы | |||
3D модель (JSmol) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.392 | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| |||
| |||
| Характеристики | |||
| C4ЧАС4S | |||
| Молярная масса | 84,14 г / моль | ||
| Внешность | бесцветная жидкость | ||
| Плотность | 1,051 г / мл, жидкость | ||
| Температура плавления | -38 ° С (-36 ° F, 235 К) | ||
| Точка кипения | 84 ° С (183 ° F, 357 К) | ||
| -57.38·10−6 см3/ моль | |||
| 1.5287 | |||
| Вязкость | 0,8712 сп при 0,2 ° C 0,6432 сп при 22,4 ° C | ||
| Опасности | |||
| Паспорт безопасности | Внешний паспорт безопасности материалов, Внешний паспорт безопасности материалов | ||
Классификация ЕС (DSD) (устарело) | нет в списке | ||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | -1 ° С (30 ° F, 272 К) | ||
| Родственные соединения | |||
Связанный тиоэфиры | Тетрагидротиофен Диэтилсульфид | ||
Родственные соединения | Фуран Селенофен Пиррол | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
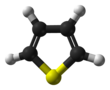
Тиофен это гетероциклическое соединение с формулой C4ЧАС4S. Состоящий из плоского пятичленного кольца, он ароматный о чем свидетельствует его обширная реакции замещения. Это бесцветная жидкость с бензол-подобный запах. В большинстве своих реакций он напоминает бензол. Соединения, аналогичные тиофену, включают: фуран (C4ЧАС4O) селенофен (C4ЧАС4Se) и пиррол (C4ЧАС4NH), каждый из которых зависит от гетероатом в ринге.
Изоляция и возникновение
Тиофен был обнаружен в качестве примеси в бензоле.[1] Было замечено, что изатин (ан индол) образует синий краситель если он смешан с серная кислота и сырой бензол. Долгое время считалось, что образование синего индофенина является реакцией самого бензола. Виктор Мейер смог выделить тиофен как фактическое вещество, ответственное за эту реакцию.[2]
Тиофен и особенно его производные встречаются в нефть, иногда в концентрациях до 1–3%. Тиофеновое содержание масло и каменный уголь удаляется через гидрообессеривание (HDS) процесс. В HDS жидкое или газообразное сырье проходит через форму дисульфид молибдена катализатор под давлением H2. Тиофены подвергаются гидрогенолизу с образованием углеводороды и сероводород. Таким образом, сам тиофен превращается в бутан и H2S. Более распространены и проблематичны в нефти бензотиофен и дибензотиофен.
На марсе
Производные тиофена были обнаружены на уровне наномолей в марсианских отложениях почвы возрастом 3,5 миллиарда лет (формация Мюррей, холмы Парамп) с помощью марсохода. Любопытство в кратере Гейла (Марс) с 2012 по 2017 год.[3] Это важная веха в выполнении миссии Марсианская научная лаборатория (MSL) в долгом и неуловимом квесте органическая материя на красной планете. Нагрев при высокой температуре (от 500 ° до 820 ° C) образцов озерного аргиллита Анализ проб на Марсе (SAM) инструмент разрешен газовая хроматография-масс-спектрометрия (ГХ-МС) анализ выделяемых газов и обнаружение ароматических и алифатических молекул, включая несколько тиофеновых соединений.[4] Наличие связей углерод-сера в макромолекулах могло способствовать сохранению органического вещества на очень долгое время. По оценкам, ~ 5% органических молекул, проанализированных СЭМ инструмент содержит органическую серу. Происхождение и способ образования этих молекул до сих пор неизвестны. биотический или же абиотический,[5] но их открытие поставило загадочный вопрос о тиофеновых соединениях как о возможных древних биоподпись на Марсе. Детальный анализ изотопов углерода (δ13C) на уровне следа марсианских вездеходов следующего поколения, таких как Розалинд Франклин,[6] необходимо будет определить, обогащены ли такие органические молекулы легким углеродом (12В) как живые микроорганизмы, обычно обитающие на Земле.
Синтез и производство
Отражая свою высокую стабильность, тиофены возникают в результате многих реакций с участием источников серы и углеводородов, особенно ненасыщенных. Первый синтез тиофена Мейером, описанный в том же году, когда он сделал свое открытие, включает ацетилен и элементарную серу. Тиофены обычно получают реакцией 1,4-дикетоны, диэфиры или дикарбоксилаты с сульфидирующими реагентами, такими как P4S10 например, в Синтез тиофена Пааль-Кнорра. Специализированные тиофены можно синтезировать аналогичным образом, используя Реактив Лавессона в качестве сульфидирующего агента или через Реакция Гевальда, который включает конденсацию двух сложные эфиры в присутствии элементарной серы. Другой метод - это Циклизация Фольхарда – Эрдмана.
Во всем мире тиофен производится в скромных масштабах - около 2000 метрических тонн в год. Производство включает парофазную реакцию источника серы, обычно сероуглерод, и источник C-4, обычно бутанол. Эти реагенты контактируют с оксидом катализатор при 500–550 ° С.[7]
Свойства и структура
При комнатной температуре тиофен представляет собой бесцветную жидкость с умеренно приятным запахом, напоминающим запах бензол, с которым тиофен имеет некоторые общие черты. Высокая реакционная способность тиофена по отношению к сульфированию является основой для отделения тиофена от бензола, которые трудно отделить от бензола. дистилляция из-за схожих точек кипения (разница в 4 ° C при атмосферном давлении). Подобно бензолу тиофен образует азеотроп с этанолом.
Молекула плоская; валентный угол у серы составляет около 93 °, угол C – C – S составляет около 109 °, а два других атома углерода имеют валентный угол около 114 °.[8] Связи C – C с атомами углерода, примыкающими к сере, составляют около 1,34Åдлина связи C – S составляет около 1,70 Å, а длина другой связи C – C составляет около 1,41 Å.[8]
Реактивность
Тиофен считается ароматическим, хотя теоретические расчеты показывают, что степень ароматичности меньше, чем у бензола. «Электронные пары» на сере значительно делокализованный в пи электрон система. Вследствие своей ароматичности тиофен не проявляет свойств, наблюдаемых у обычных сульфиды. Например, атом серы сопротивляется алкилированию и окислению.
Окисление
Окисление может происходить как по сере с образованием тиофена. S-оксид, а также по 2,3-двойной связи, давая тиофен 2,3-эпоксид с последующим Смена NIH перестановка.[9] Окисление тиофена трифторопераксусная кислота также демонстрирует оба пути реакции. Основной путь формирует S-оксид как промежуточный продукт, который подвергается последующему Дильс-Альдер-тип димеризация и дальнейшее окисление с образованием смеси сульфоксид и сульфон продукты с комбинированной доходностью 83% (на основе ЯМР свидетельство):[10][11]
На второстепенном пути реакции Прилежаев эпоксидирование[12] приводит к образованию тиофен-2,3-эпоксида, который быстро перестраивает к изомер тиофен-2-он.[10] Эксперименты по отлову[13] продемонстрировать, что этот путь не побочная реакция от S-оксид промежуточный, в то время как изотопная маркировка с дейтерий подтвердить, что 1,2-гидридный сдвиг происходит и, таким образом, вовлекается катионный промежуточный продукт.[10] Если реакционная смесь не безводный, этот второстепенный путь реакции подавляется, поскольку вода выступает в качестве конкурирующей основы.[10]
Окисление тиофенов может иметь отношение к метаболической активации различных тиофенсодержащих препаратов, таких как тиениловая кислота и исследуемый противоопухолевый препарат OSI-930.[14][15][16][17]
Алкилирование
Хотя атом серы относительно инертен, фланкирующие углеродные центры, положения 2 и 5, очень восприимчивы к атаке со стороны электрофилы. Галогены дают сначала производные 2-галогена, а затем - 2,5-дигалогентиофены; пергалогенирование легко осуществляется с образованием C4Икс4S (X = Cl, Br, I).[18] Броминаты тиофена 107 раз быстрее, чем бензол.[7]
Хлорметилирование и хлорэтилирование легко протекают по 2,5-положениям. Восстановление хлорметильного продукта дает 2-метилтиофен. Гидролиз с последующей дегидратацией хлорэтильных соединений дает 2-винилтиофен.[19][20]
Обессеривание никелем Ренея
Обессеривание тиофена с помощью Никель Ренея дает бутан. В сочетании с простой 2,5-дифункциональностью тиофена десульфуризация обеспечивает путь к 1,4-дизамещенным бутанам.
Полимеризация
Полимер, образованный путем связывания тиофена через его 2,5 положения, называется политиофен. Полимеризация проводится окислением электрохимическими методами (электрополимеризация) или реагенты для переноса электрона. Показано идеализированное уравнение:
- п С4ЧАС4S → (C4ЧАС2S)п + 2n H+ + 2n e−
Сам политиофен имеет плохие технологические свойства и поэтому мало изучен. Более подходящими являются полимеры, полученные из тиофенов, замещенных в положениях 3, 3 и 4, такие как ЭДОТ (этилендиокситиофен). Политиофены становятся электропроводными при частичном окислении, то есть они приобретают некоторые из характеристик, обычно наблюдаемых в металлах.[21]
Координационная химия
Тиофен проявляет слабый сульфидный характер, но он действительно служит пи-лигандом, образующим фортепианные табуреты например Cr (η5-C4ЧАС4S) (CO)3.[22]
Производные тиофена
- Некоторые тиофены
3,4-этилендиокситиофен (EDOT) является предшественником коммерческого антистатика и электрохромные дисплеи.
Тиенил
При депротонировании тиофен превращается в тиенильную группу C4ЧАС3S−. Хотя аниона как такового не существует, литийорганический производные. Таким образом, реакция тиофена с бутиллитий дает 2-литиотиофен, также называемый 2-тиениллитием. Этот реагент реагирует с электрофилами с образованием тиенильных производных, таких как тиол.[23] Окисление тиениллития дает 2,2'-дитиенил, (C4ЧАС3S)2. Тиениллитий используется для получения более высокого порядка. смешанные купраты.[24] Сочетание эквивалентов тиениланиона дает дитиенил, аналог бифенила.
Тиофены с конденсированными кольцами
Слияние тиофена с бензольным кольцом дает бензотиофен. Слияние с двумя бензольными кольцами дает либо дибензотиофен (ДБТ) или нафтотиофен. Слияние пары тиофеновых колец дает изомеры тиенотиофен.
Использует
Тиофены - важные гетероциклические соединения, которые широко используются в качестве строительных блоков во многих агрохимикатах и фармацевтических препаратах.[7] Бензольное кольцо биологически активного соединения часто можно заменить тиофеном без потери активности.[25] Это видно на таких примерах, как НПВП лорноксикам, тиофеновый аналог пироксикам, и суфентанил, тиофеновый аналог фентанил.
Рекомендации
- ^ Мейер, Виктор (1883). "Ueber den Begleiter des Benzols im Steinkohlenteer" [О веществе, которое сопровождает бензол в каменноугольной смоле]. Berichte der Deutschen Chemischen Gesellschaft. 16: 1465–1478. Дои:10.1002 / cber.188301601324.
- ^ Уорд К., Самптер (1944). «Химия Исатина». Химические обзоры. 34 (3): 393–434. Дои:10.1021 / cr60109a003.
- ^ Воозен, Пол (2018). «Марсоход НАСА поражает Марс органической землей». Наука. Дои:10.1126 / science.aau3992. ISSN 0036-8075.
- ^ Eigenbrode, Jennifer L .; Вызывает, Роджер Э .; Стил, Эндрю; Фрейсине, Кэролайн; Миллан, Маэва; Наварро-Гонсалес, Рафаэль; Саттер, Брэд; Макадам, Эми С.; Франц, Хизер Б .; Glavin, Daniel P .; Арчер, Пол Д .; Mahaffy, Paul R .; Конрад, Памела Г.; Hurowitz, Joel A .; Гротцингер, Джон П .; Гупта, Санджив; Мин, Дуг У .; Самнер, Dawn Y .; Сопа, Кирилл; Малеспин, Чарльз; Бух, Арно; Колл, Патрис (2018). "Органическое вещество сохранилось в аргиллитах возрастом 3 миллиарда лет в кратере Гейла на Марсе" (PDF). Наука. 360 (6393): 1096–1101. Bibcode:2018Научный ... 360.1096E. Дои:10.1126 / science.aas9185. ISSN 0036-8075. PMID 29880683. S2CID 46983230.
- ^ Хайнц, Джейкоб; Шульце-Макух, Дирк (2020). «Тиофены на Марсе: биотическое или абиотическое происхождение?». Астробиология. 20 (4): 552–561. Bibcode:2020AsBio..20..552H. Дои:10.1089 / аст.2019.2139. PMID 32091933.
- ^ «Марсоход Curiosity обнаружил на Марсе органические молекулы. Вот почему они интересны».. CNN. 6 марта 2020.
- ^ а б c Суонстон, Джонатан (2006). «Тиофен». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a26_793.pub2. ISBN 3527306730..
- ^ а б Кембриджская структурная база данных
- ^ Treiber, A., Dansette, P.M., Amri, H.E., Girault, J.-P., Ginderow, D., Mornon, J.-P., Mansuy, D .; Дансетта; Эль-Амри; Жиро; Гиндеров; Морнон; Мансуй (1997). «Химическое и биологическое окисление тиофена: получение и полная характеристика тиофена. S-оксид Димеры и доказательства тиофена S-Оксид как промежуточное звено в метаболизме тиофена в естественных условиях и in vitro". Варенье. Chem. Soc. 119 (7): 1565–1571. Дои:10.1021 / ja962466g.CS1 maint: несколько имен: список авторов (связь)
- ^ а б c d Трейбер, Александр (2002). "Механизм ароматического гидроксилирования тиофена кислотно-катализируемым надкислотным окислением". J. Org. Chem. 67 (21): 7261–7266. Дои:10.1021 / jo0202177. PMID 12375952.
- ^ Кастер, Кеннет С.; Рао, А. Сомасекар; Мохан, Х. Рама; McGrath, Nicholas A .; Бричачек, Мэтью (2012). «Трифторперуксусная кислота». Энциклопедия реагентов для органического синтеза. Энциклопедия реагентов для органического синтеза e-EROS. Дои:10.1002 / 047084289X.rt254.pub2. ISBN 978-0471936237.
- ^ Хаген, Тимоти Дж. (2007). «Прилежаевская реакция». Ин Ли, Джи Джек; Кори, Э. Дж. (ред.). Назовите реакции преобразований функциональных групп.. Джон Уайли и сыновья. С. 274–281. ISBN 9780470176504.
- ^ Анслин, Эрик В.; Догерти, Деннис А. (2006). «8.8 Разные эксперименты для изучения механизмов». Современная физико-органическая химия. Книги университетских наук. С. 471–482. ISBN 9781891389313.
- ^ Mansuy, D., Valadon, P., Erdelmeier, I., López García, P., Amar, C., Girault, J.P., and Dansette, P.M. (1991). «Тиофен S-оксиды как новые реактивные метаболиты: образование путем цитохром-P450-зависимого окисления и реакции с нуклеофилами ». Варенье. Chem. Soc. 113 (20): 7825–7826. Дои:10.1021 / ja00020a089.CS1 maint: несколько имен: список авторов (связь)
- ^ Радемахер П. М., Вудс К. М., Хуанг К., Шкларц Г. Д., Нельсон С. Д.; Лес; Хуанг; Szklarz; Нельсон (2012). «Дифференциальное окисление двух тиофен-содержащих региоизомеров до реактивных метаболитов цитохромом P450 2C9». Chem. Res. Токсикол. 25 (4): 895–903. Дои:10.1021 / tx200519d. ЧВК 3339269. PMID 22329513.CS1 maint: несколько имен: список авторов (связь)
- ^ Mansuy D., Dansette P.M .; Дансетт (2011). «Сульфеновые кислоты как реактивные промежуточные соединения в метаболизме ксенобиотиков». Архивы биохимии и биофизики. 507 (1): 174–185. Дои:10.1016 / j.abb.2010.09.015. PMID 20869346.
- ^ Дансетт, П.М., Рози, Дж., Дебернарди, Дж., Берто Дж., Мэнсуи Д.; Рози; Дебернарди; Берто; Мансуй (2012). «Метаболическая активация прасугрела: природа двух конкурентных путей, приводящих к открытию его тиофенового кольца». Chem. Res. Toxicol. 25 (5): 1058–1065. Дои:10.1021 / тx3000279. PMID 22482514.CS1 maint: несколько имен: список авторов (связь)
- ^ Генри Ю. Лью и К. Р. Ноллер (1963). «2-Йодолтиофен». Органический синтез.; Коллективный объем, 4, п. 545
- ^ У. С. Эмерсон и Т. М. Патрик младший (1963). «2-винилтиофен». Органический синтез.; Коллективный объем, 4, п. 980
- ^ К. Б. Виберг и Г. Ф. МакШейн (1955). «2-хлорметилтиофен». Органический синтез.; Коллективный объем, 3, п. 1
- ^ Дж. Ронкали (1992). «Конъюгированные поли (тиофены): синтез, функционализация и применение». Chem. Ред. 92 (4): 711–738. Дои:10.1021 / cr00012a009.
- ^ Раухфус, Т. Б., "Координационная химия тиофенов", Progress in Inorganic Chemistry, 1991, том 39, стр. 259-311. ISBN 978-0-471-54489-0
- ^ Э. Джонс и И. М. Муди (1988). «2-Тиофентиол». Органический синтез.; Коллективный объем, 6, п. 979
- ^ Липшуц, Брюс Х.; Моретти, Роберт; Ворона, Роберт (1990). «Смешанные эпоксидные отверстия, индуцированные цианокупратом высшего порядка: 1-бензилокси-4-пентен-2-ол». Орг. Синтезатор. 69: 80. Дои:10.15227 / orgsyn.069.0080.
- ^ Даниэль Ледничер (1999). Органическая химия синтеза лекарств. 6. Нью-Йорк: Wiley Interscience. п. 187. ISBN 0-471-24510-0.
внешняя ссылка
- Международная карта химической безопасности 1190
- Чисхолм, Хью, изд. (1911). . Британская энциклопедия. 26 (11-е изд.). Издательство Кембриджского университета.