WikiDer > Трехокись серы - Википедия
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC Триоксид серы | |||
| Систематическое название ИЮПАК Сульфонилиденоксидан | |||
| Другие имена Серный ангидрид, оксид серы (VI) | |||
| Идентификаторы | |||
3D модель (JSmol) |
| ||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.361 | ||
| Номер ЕС |
| ||
| 1448 | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | ООН 1829 | ||
| |||
| |||
| Характеристики | |||
| ТАК3 | |||
| Молярная масса | 80.066 г / моль | ||
| Внешность | Кристаллическое твердое вещество от бесцветного до белого цвета, которое будет дымить на воздухе.[1] Бесцветная жидкость и газ.[2] | ||
| Запах | Варьируется. Пар едкий; как диоксид серы.[3] Туман без запаха.[2] | ||
| Плотность | 1.92 г / см3, жидкость | ||
| Температура плавления | 16,9 ° С (62,4 ° F, 290,0 К) | ||
| Точка кипения | 45 ° С (113 ° F, 318 К) | ||
| Реагирует дать серная кислота | |||
| Термохимия | |||
Стандартный моляр энтропия (S | 256.77 JK−1моль−1 | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −395.7 кДж / моль | ||
| Опасности | |||
| Главный опасности | Сильная коррозия | ||
| Паспорт безопасности | ICSC 1202 | ||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасность | ||
| H314, H335 | |||
| P261, P280, P305 + 351 + 338, P310[4] | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | Негорючий | ||
| Смертельная доза или концентрация (LD, LC): | |||
LC50 (средняя концентрация) | крыса, 4 375 ч. мг / м3[нужна цитата] | ||
| Родственные соединения | |||
Другой катионы | Триоксид селена Триоксид теллура | ||
| Окись серы Диоксид серы | |||
Родственные соединения | Серная кислота | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Триоксид серы (альтернативное написание триоксид серы) - химическое соединение формулы SO3, с относительно узким диапазоном жидкости. В газообразной форме этот вид представляет собой значительный загрязнитель, являясь основным предшественником кислотный дождь.[5]
Он готовится в промышленных масштабах как предшественник серная кислота, и также известен как серная ангидрид.
В совершенно сухом аппарате пары триоксида серы невидимы, а жидкость прозрачна. Однако он обильно дымит даже в относительно сухой атмосфере (его использовали в качестве дымового агента) из-за образования тумана серной кислоты. Этот пар не имеет запаха, но чрезвычайно агрессивен.[2]
Молекулярная структура и связь
Газообразный SO3 это тригонально плоский молекула D3ч симметрия, как предсказано Теория VSEPR. ТАК3 принадлежит D3ч точечная группа.
С точки зрения формализма счета электронов, атом серы имеет степень окисления +6 и официальное обвинение из 0. Структура Льюиса состоит из S = O двойная связь и два S – O дативные облигации без использования d-орбиталей.[6]
Электрический дипольный момент газообразного триоксида серы равна нулю. Это является следствием угла 120 ° между связями S-O.
Химические реакции
ТАК3 это ангидрид из H2ТАК4. Таким образом, происходит следующая реакция:
Реакция протекает как быстро, так и экзотермически, слишком бурно, чтобы ее можно было использовать в крупномасштабном производстве. При температуре 340 ° C или выше серная кислота, триоксид серы и вода сосуществуют в значительных равновесных концентрациях.[нужна цитата]
Триоксид серы также окисляет дихлорид серы приносить полезные реагент, тионилхлорид.
- ТАК3 + SCl2 → SOCl2 + ТАК2
ТАК3 сильный Кислота Льюиса легко образующие кристаллические комплексы с пиридин, диоксан, и триметиламин. Эти аддукты можно использовать в качестве сульфирующих агентов.[8]
Подготовка
В атмосфере
Прямое окисление диоксида серы до триоксида серы на воздухе:
- ТАК2 + 1⁄2О2 = ТАК3 ΔH = -198,4
действительно происходит, но реакция идет очень медленно.
В лаборатории
Триоксид серы можно получить в лаборатории двухступенчатым способом. пиролиз из бисульфат натрия. Пиросульфат натрия промежуточный продукт:[9]
- Обезвоживание при 315 ° C:
- 2 NaHSO4 → Na2S2О7 + H2О
- Растрескивание при 460 ° C:
- Na2S2О7 → Na2ТАК4 + ТАК3
Напротив, KHSO4 не подвергается такой же реакции.[9]
Его также можно приготовить, добавив концентрированный серная кислота к пятиокись фосфора.[10]
В промышленности
Промышленно SO3 сделано контактный процесс. Диоксид серы, что, в свою очередь, происходит за счет сжигания сера или же железный пирит (сульфидная железная руда). После очистки электростатическим осаждением SO2 затем окисляется атмосферным кислород при температуре от 400 до 600 ° C над катализатором. Типичный катализатор состоит из пятиокись ванадия (V2О5) активируется с помощью оксид калия K2О на кизельгур или же кремнезем поддерживать. Платина также работает очень хорошо, но слишком дорого и гораздо легче отравляется (становится неэффективным) примесями.[11]
Большая часть триоксида серы, полученного таким образом, превращается в серная кислота не путем прямого добавления воды, с которой образуется тонкий туман, а путем поглощения концентрированной серной кислотой и разбавления водой полученного олеум.[нужна цитата]
Когда-то он производился промышленным способом путем нагрева. сульфат кальция с кремнезем.
Приложения
Триоксид серы является важным реагентом в сульфирование реакции. Эти процессы позволяют получать моющие средства, красители и фармацевтические препараты. Триоксид серы образуется на месте из серной кислоты или используется в виде раствора в кислоте.
Структура твердого SO3
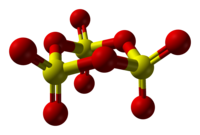

Природа твердого SO3 сложный, потому что структурные изменения вызваны следами воды.[12]
При конденсации газа абсолютно чистый SO3 конденсируется в тример, который часто называют γ-ТАК3. Эта молекулярная форма представляет собой бесцветное твердое вещество с температурой плавления 16,8 ° C. Он принимает циклическую структуру, описываемую как [S (= O)2(μ-O)]3.[13]
Если так3 конденсируется выше 27 ° C, затем α-ТАК3 формы, которая имеет температуру плавления 62,3 ° C. α-ТАК3 имеет волокнистый вид. Конструктивно это полимер [S (= O)2(μ-O)]п. Каждый конец полимера оканчивается группами ОН. β-ТАК3, как и альфа-форма, является волокнистым, но с разной молекулярной массой, состоит из полимера с гидроксильными группами, но плавится при 32,5 ° C. И гамма, и бета-формы являются метастабильными, в конечном итоге они превращаются в стабильную альфа-форму, если оставить их на некоторое время. Это преобразование вызвано следами воды.[14]
Относительное давление паров твердого SO3 альфа <бета <гамма при одинаковых температурах, что указывает на их относительные молекулярная масса. Жидкий триоксид серы имеет давление пара, соответствующее гамма-форме. Таким образом нагревая кристалл α-ТАК3 до точки плавления приводит к внезапному увеличению давления пара, которое может быть достаточно сильным, чтобы разбить стеклянный сосуд, в котором он нагревается. Этот эффект известен как «альфа-взрыв».[14]
ТАК3 агрессивно гигроскопичный. Теплоты гидратации достаточно, чтобы смеси SO3 дерево или хлопок могут воспламениться. В таких случаях SO3 обезвоживает эти углеводы.[14]
Безопасность
Помимо того, что триоксид серы является сильным окислителем, он может вызвать серьезные ожоги как при вдыхании, так и при проглатывании, поскольку он очень агрессивен и гигроскопичен по своей природе. ТАК3 с ним следует обращаться с особой осторожностью, поскольку он бурно реагирует с водой и выделяет высококоррозионную серную кислоту. Его также следует хранить вдали от органических материалов из-за сильной дегидратирующей природы триоксида серы и его способности бурно реагировать с такими материалами.
Источники
Смотрите также
Рекомендации
- ^ "ТРИОКСИД СЕРЫ CAMEO Chemicals NOAA". Cameochemicals.noaa.gov.
- ^ а б c Лернер, Л. (2011). Маломасштабный синтез лабораторных реагентов с моделированием реакций. CRC Press. п. 10. ISBN 9781439813133. LCCN 2010038460.
- ^ «Вещество: триоксид серы - Learn Chemistry Wiki». Rsc.org.
- ^ «Триоксид серы 227692» (PDF). SO3. Архивировано из оригинал на 2020-09-01. Получено 1 сентября 2020.
- ^ Томас Лоэртинг; Клаус Р. Лидл (2000). «К устранению расхождений между теорией и экспериментом: константа скорости атмосферной конверсии SO3 к H2ТАК4". Труды Национальной академии наук Соединенных Штатов Америки. 97 (16): 8874–8878. Bibcode:2000PNAS ... 97.8874L. Дои:10.1073 / пнас.97.16.8874. ЧВК 16788. PMID 10922048.
- ^ Теренс П. Каннингем, Дэвид Л. Купер, Джозеф Геррат, Питер Б. Карадаков и Марио Раймонди (1997). «Химическая связь в оксофторидах сверхкоординированной серы». Журнал химического общества, транзакции Фарадея. 93 (13): 2247–2254. Дои:10.1039 / A700708F.CS1 maint: несколько имен: список авторов (связь)
- ^ «Производство серной кислоты и суперфосфата» (PDF). Химические процессы в Новой Зеландии.
- ^ Коттон, Ф. Альберт; Уилкинсон, Джеффри; Мурильо, Карлос А .; Бохманн, Манфред (1999), Продвинутая неорганическая химия (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 0-471-19957-5
- ^ а б К.Дж. де Фриз; П.Дж. Геллингс (май 1969 г.). «Термическое разложение пиросульфата калия и натрия». Журнал неорганической и ядерной химии. 31 (5): 1307–1313. Дои:10.1016/0022-1902(69)80241-1.
- ^ «Как сделать триоксид серы - YouTube». www.youtube.com. Получено 1 сентября 2020.
- ^ Герман Мюллер "Серная кислота и триоксид серы" в Энциклопедия промышленной химии Ульмана, Wiley-VCH, Weinheim. 2000 г. Дои:10.1002 / 14356007.a25_635
- ^ Холлеман, Арнольд Фредерик; Виберг, Эгон (2001), Виберг, Нильс (ред.), Неорганическая химия, переведенный Иглсоном, Мэри; Брюэр, Уильям, Сан-Диего / Берлин: Academic Press / De Gruyter, ISBN 0-12-352651-5
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ а б c Индекс химических веществ и лекарств Мерк, 9 изд. монография 8775


