WikiDer > Бромид железа (III)
 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Бромид железа (III) | |
| Другие имена Бромид железа Трибромид железа трибромойрон | |
| Идентификаторы | |
3D модель (JSmol) | |
| ChemSpider | |
| ECHA InfoCard | 100.030.069 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| FeBr3 | |
| Молярная масса | 295,56 г моль−1 |
| Внешность | коричневое твердое вещество |
| Запах | без запаха |
| Плотность | 4,50 г см−3 |
| Температура плавления | 200 ° С (392 ° F, 473 К) (разлагается) |
| Структура | |
| Тригональный, 24 грн. | |
| Р-3, №148 | |
| Опасности | |
| Главный опасности | разъедающий |
| R-фразы (устарело) | R36 / 37/38 |
| S-фразы (устарело) | S26 S37 / 39 |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Бромид железа (III) это химическое соединение с формула FeBr3. Это красно-коричневое соединение без запаха, также известное как бромид железа, используется в качестве Кислота Льюиса катализатор в галогенирование из ароматические соединения. Он растворяется в воде с образованием кислых растворов.
Структура, синтез и основные свойства
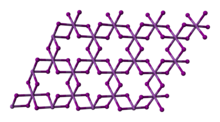
FeBr3 образует полимерную структуру с шестикоординатной, восьмигранный Fe центры.[1] Хотя FeBr продается недорого,3 могут быть получены обработкой металлического железа бром:
- 2 Fe + 3 Br2 → 2 FeBr3
Выше 200 ° C, FeBr3 разлагается на бромид железа:
- 2Фебр3 → 2FeBr2 + Br2
Хлорид железа (III) значительно более стабилен, отражая большую окислительную способность хлор. FeI3 не является стабильным, так как железо (III) окисляет ионы йодида.
Использует
Бромид железа иногда используется в качестве окислителя в органическая химия, например для преобразования спирты к кетонам. Он используется как Льюис кислый катализатор бромирования ароматических соединений. Для последних приложений он часто создается на месте.[2]
Смотрите также
- Бромид железа (II), низший бромид железа
Рекомендации
- ^ Холлеман, А. Ф .; Виберг, Э. "Неорганическая химия" Academic Press: Сан-Диего, 2001. ISBN 0-12-352651-5.
- ^ Drapeau, Мартин Пичетт; Lafantaisie, Mathieu; Оллевье, Тьерри (2013). «Бромид железа (III)». Энциклопедия реагентов для органического синтеза E-EROS. Дои:10.1002 / 047084289X.rn01568. ISBN 978-0471936237.CS1 maint: использует параметр авторов (связь)
