WikiDer > Оксид родия (IV)
 | |
| Идентификаторы | |
|---|---|
3D модель (JSmol) | |
| ChemSpider | |
| ECHA InfoCard | 100.032.021 |
| Номер ЕС |
|
PubChem CID | |
| |
| |
| Характеристики | |
| RhO2 | |
| Молярная масса | 134,904 г / моль |
| Внешность | черное кристаллическое твердое вещество |
| Плотность | 7,2 г / см3 |
| Температура плавления | 1050 ° С (1,920 ° F, 1320 К) (разлагается) |
| Растворимость | не растворим в царская водка |
| Структура | |
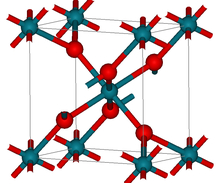
| четырехугольный (рутил) | |
| Опасности | |
Классификация ЕС (DSD) (устарело) | нет в списке |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Оксид родия (IV) (или же диоксид родия) это химическое соединение с формулой RhО2.
Химические свойства
RhO2 очень нерастворим даже в горячих царская водка.[1]
Структура
RhO2 имеет четырехугольный рутил структура.[2]
Физические свойства
RhO2 имеет металлическое удельное сопротивление со значениями <10−4 Ом · см. Он превращается в воздухе в Rh2О3 при 850 ° C, а затем на металл и кислород при 1050 ° C.[2]
Смотрите также
Рекомендации
- ^ О. Мюллер и Р. Рой (1968). «Образование и стабильность оксидов платины и родия при высоких давлениях кислорода и структуры Pt.3О4, β-PtO2 и RhO2". Журнал менее распространенных металлов. 16 (2): 129–146. Дои:10.1016/0022-5088(68)90070-2.
- ^ а б Р. Д. Шеннон (1968). «Синтез и свойства двух новых членов семейства рутиловых RhO.2 и PtO2". Твердотельные коммуникации. 6 (3): 139–143. Дои:10.1016/0038-1098(68)90019-7.
| Этот неорганический сложный–Связанная статья является заглушка. Вы можете помочь Википедии расширяя это. |