WikiDer > Цирконий
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Цирконий | ||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | /zərˈkoʊпяəм/ | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешность | серебристо-белый | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Стандартный атомный вес Аг, стд(Zr) | 91.224(2)[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Цирконий в периодическая таблица | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомный номер (Z) | 40 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Группа | группа 4 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Период | период 5 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Блокировать | d-блок | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Категория элемента | Переходный металл | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Электронная конфигурация | [Kr] 4d2 5 с2 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Электронов на оболочку | 2, 8, 18, 10, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Физические свойства | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фаза вSTP | твердый | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Температура плавления | 2128 K (1855 ° С, 3371 ° F) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Точка кипения | 4650 К (4377 ° С, 7911 ° F) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Плотность (возлеr.t.) | 6,52 г / см3 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| в жидком состоянии (приm.p.) | 5,8 г / см3 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота плавления | 14 кДж / моль | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота испарения | 591 кДж / моль | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярная теплоемкость | 25,36 Дж / (моль · К) | |||||||||||||||||||||||||||||||||||||||||||||||||||
Давление газа
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомные свойства | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Состояния окисления | −2, 0, +1,[2] +2, +3, +4 (анамфотерный окись) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 1,33 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Энергии ионизации |
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Радиус атома | эмпирические: 160вечера | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Ковалентный радиус | 175 ± 19 часов | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Спектральные линии циркония | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Другие свойства | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Естественное явление | изначальный | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Кристальная структура | шестиугольный плотно упакованный (ГПУ) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Скорость звука тонкий стержень | 3800 м / с (при 20 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Тепловое расширение | 5,7 мкм / (м · К) (при 25 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплопроводность | 22,6 Вт / (м · К) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Удельное электрическое сопротивление | 421 нОм · м (при 20 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Магнитный заказ | парамагнитный[3] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Модуль для младших | 88 ГПа | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Модуль сдвига | 33 ГПа | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Объемный модуль | 91,1 ГПа | |||||||||||||||||||||||||||||||||||||||||||||||||||
| коэффициент Пуассона | 0.34 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по Моосу | 5.0 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по Виккерсу | 820–1800 МПа | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Твердость по Бринеллю | 638–1880 МПа | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Количество CAS | 7440-67-7 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| История | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Именование | после циркон, заргун زرگون означает «золотой». | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Открытие | Мартин Генрих Клапрот (1789) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Первая изоляция | Йенс Якоб Берцелиус (1824) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Главный изотопы циркония | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
Цирконий это химический элемент с символ Zr и атомный номер 40. Имя цирконий взято из названия минерала циркон (слово связано с Персидский заргун (циркон; зар-пушка, «подобный золоту» или «как золото»)), важнейший источник циркония.[5] Блестящий, серо-белый, прочный переходный металл это очень похоже гафний и, в меньшей степени, титан. Цирконий в основном используется как огнеупорный и глушитель, хотя небольшие количества используются в качестве легирующего агента из-за его высокой устойчивости к коррозии. Цирконий образует множество неорганический и металлоорганические соединения Такие как диоксид циркония и дихлорид цирконоцена, соответственно. Пять изотопы происходят естественно, три из которых стабильны. Соединения циркония не имеют известной биологической роли.
Характеристики
Цирконий - это блестящий, серо-белый, мягкий, пластичный, податливый металл, твердый при комнатной температуре, но твердый и хрупкий при меньшей чистоте.[6][7] В виде порошка цирконий легко воспламеняется, но в твердой форме он гораздо менее склонен к возгоранию. Цирконий обладает высокой устойчивостью к коррозии под действием щелочей, кислот, соленой воды и других агентов.[8] Однако он растворится в соляной и серная кислота, особенно когда фтор настоящее.[9] Сплавы с цинк находятся магнитный при температуре менее 35 К.[8]
В температура плавления циркония составляет 1855 ° C (3371 ° F), а точка кипения составляет 4371 ° C (7900 ° F).[8] Цирконий имеет электроотрицательность 1,33 по шкале Полинга. Из элементов внутри d-блок с известной электроотрицательностью цирконий занимает пятое место по самой низкой электроотрицательности после гафний, иттрий, лантан, и актиний.[10]
При комнатной температуре цирконий демонстрирует гексагонально плотноупакованную кристаллическую структуру α-Zr, которая при 863 ° C превращается в β-Zr, объемно-центрированную кубическую кристаллическую структуру. Цирконий существует в β-фазе до точки плавления.[11]
Изотопы
Встречающийся в природе цирконий состоит из пяти изотопов. 90Zr, 91Zr, 92Zr и 94Zr стабильны, хотя 94Прогнозируется, что Zr подвергнется двойной бета-распад (экспериментально не наблюдается) с период полураспада более 1,10 × 1017 годы. 96Zr имеет период полураспада 2,4 × 1019 лет, и является самым долгоживущим радиоизотопом циркония. Из этих природных изотопов 90Zr является наиболее распространенным, составляя 51,45% от всего циркония. 96Zr является наименее распространенным, он составляет всего 2,80% циркония.[12]
Было синтезировано 28 искусственных изотопов циркония с атомной массой от 78 до 110. 93Zr является самым долгоживущим искусственным изотопом с периодом полураспада 1,53 × 106 годы. 110Zr, самый тяжелый изотоп циркония, является наиболее радиоактивным с предполагаемым периодом полураспада 30 миллисекунд. Радиоактивные изотопы с массовым числом 93 или выше распадаются на электронная эмиссия, тогда как те, у кого 89 или ниже, распадаются на позитронное излучение. Единственное исключение - 88Zr, распадающийся на захват электронов.[12]
Пять изотопов циркония также существуют в виде метастабильные изомеры: 83мZr, 85 мZr, 89мZr, 90 млZr, 90м2Zr и 91 мZr. Из этих, 90м2Zr имеет самый короткий период полураспада - 131 наносекунду. 89мZr является самым долгоживущим с периодом полураспада 4,161 минуты.[12]
Вхождение
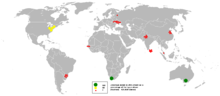
Цирконий имеет концентрацию около 130 мг / кг в земной коры и около 0,026 мкг / л в морская вода.[13] В природе не встречается как самородный металл, отражая его внутреннюю нестабильность по отношению к воде. Основным коммерческим источником циркония является циркон (ZrSiO4), а силикатный минерал,[6] который находится в основном в Австралии, Бразилии, Индии, России, Южной Африке и США, а также на более мелких месторождениях по всему миру.[7] По состоянию на 2013 год две трети добычи циркона приходится на Австралию и Южную Африку.[14] Ресурсы циркона превышают 60 млн. тонны Мировой[15] Ежегодное мировое производство циркония составляет около 900 000 тонн.[13] Цирконий также встречается более чем в 140 других минералах, включая коммерчески полезные руды. бадделеит и коснарит.[16]
Цирконий относительно богат Звезды S-типа, и он был обнаружен на Солнце и в метеоритах. Образцы лунных пород, привезенные из нескольких Аполлон миссии на Луну имеют высокое содержание оксида циркония по сравнению с земными породами.[8]
ЭПР-спектроскопия использовалась для исследования необычного 3+ валентного состояния циркония. Спектр ЭПР Zr3 +, который первоначально наблюдался как паразитный сигнал в монокристаллах ScPO4, легированных Fe, был окончательно идентифицирован при получении монокристаллов ScPO4, легированных изотопно обогащенным (94,6%) 91Zr. Также были выращены и исследованы монокристаллы LuPO4 и YPO4, легированные как естественным, так и изотопно обогащенным Zr.[17]
Производство
Цирконий является побочным продуктом добычи и переработки титан минералы ильменит и рутил, а также банка добыча полезных ископаемых.[18] С 2003 по 2007 год, в то время как цены на минеральный циркон постоянно росли с 360 до 840 долларов за тонну, цена на необработанный металлический цирконий снизилась с 39 900 долларов до 22 700 долларов за тонну. Металлический цирконий намного дороже, чем циркон, потому что процессы восстановления дороги.[15]
Цирконсодержащий песок, собранный из прибрежных вод, очищается спиральные концентраторы для удаления более легких материалов, которые затем возвращаются в воду, поскольку они являются естественными компонентами пляжного песка. С помощью магнитная сепарация, титановые руды ильменит и рутил удалены.
Большая часть циркона используется непосредственно в коммерческих целях, но небольшой процент превращается в металл. Большая часть металлического Zr производится путем восстановления хлорид циркония (IV) с магний металл в Кролл процесс.[8] Полученный металл спеченный пока не станет достаточно пластичным для обработки металлов.[7]
Разделение циркония и гафния
Коммерческий металлический цирконий обычно содержит 1–3% гафний,[19] что обычно не вызывает проблем, поскольку химические свойства гафния и циркония очень похожи. Однако их нейтронопоглощающие свойства сильно различаются, что требует отделения гафния от циркония для ядерных реакторов.[20] Используются несколько схем разделения.[19] В жидкость-жидкостная экстракция из тиоцианат-оксидные производные используют тот факт, что производное гафния немного лучше растворяется в метилизобутилкетон чем в воде. Этот метод используется в основном в США.
Zr и Hf также можно разделить фракционная кристаллизация гексафторцирконата калия (K2ZrF6), который менее растворим в воде, чем аналогичное производное гафния.
Фракционная перегонка тетрахлоридов, также называемых экстрактивная перегонка, используется в основном в Европе.
Продукт четырехкратного процесса VAM (вакуумно-дуговая плавка) в сочетании с горячей экструзией и различными вариантами прокатки отверждается с использованием газа под высоким давлением и высокой температурой. автоклавирование. В результате получается цирконий реакторного качества, который примерно в 10 раз дороже, чем промышленный цирконий, загрязненный гафнием.
Гафний необходимо удалить из циркония для ядерных применений, потому что гафний имеет поперечное сечение поглощения нейтронов в 600 раз больше, чем цирконий.[21] Отделенный гафний можно использовать для реактора. стержни управления.[22]
Соединения
Как и другие переходные металлы, цирконий образует широкий спектр неорганические соединения и координационные комплексы.[23] Как правило, эти соединения представляют собой бесцветные диамагнитные твердые вещества, в которых цирконий имеет степень окисления +4. Известно гораздо меньше соединений Zr (III), а Zr (II) встречается очень редко.
Оксиды, нитриды и карбиды
Самый распространенный оксид - это диоксид циркония, ZrO2, также известный как цирконий. Это твердое вещество от прозрачного до белого имеет исключительные вязкость разрушения (для керамики) и химической стойкости, особенно в ее кубический форма.[24] Эти свойства делают диоксид циркония полезным в качестве термобарьерного покрытия,[25] хотя это тоже распространенный алмаз заменять.[24] Моноксид циркония, ZrO, также известен и Звезды S-типа распознаются по его эмиссионным линиям в видимом спектре.[26]
Вольфрамат циркония обладает необычным свойством сжиматься во всех размерах при нагревании, тогда как большинство других веществ расширяются при нагревании.[8] Цирконил хлорид представляет собой редкий водорастворимый комплекс циркония с относительно сложной формулой [Zr4(ОЙ)12(ЧАС2O)16] Cl8.
Карбид циркония и нитрид циркония тугоплавкие твердые тела. Твердый сплав используется для сверления инструментов и режущих кромок. Также известны фазы гидрида циркония.
Цирконат титанат свинца (PZT) - это наиболее часто используемый пьезоэлектрический материал с такими приложениями, как ультразвуковые преобразователи, гидрофоны, инжекторы Common Rail, пьезоэлектрические преобразователи и микроприводы.
Галогениды и псевдогалогениды
Известны все четыре обычных галогенида, ZrF4, ZrCl4, ZrBr4, и ZrI4. Все они имеют полимерную структуру и намного менее летучие, чем соответствующие мономерные тетрагалогениды титана. Все стремятся гидролизовать дать так называемые оксигалогениды и диоксиды.
Соответствующая тетраалкоксиды также известны. В отличие от галогенидов алкоксиды растворяются в неполярных растворителях. Дигидрогексафторцирконат используется в металлообрабатывающей промышленности в качестве травителя для улучшения адгезии краски.[27]
Органические производные

Цирконийорганическая химия изучение соединений, содержащих углерод-циркониевая связка. Первым таким соединением был дибромид цирконоцена ((C5ЧАС5)2ZrBr2), о котором в 1952 г. сообщили Бирмингем и Уилкинсон.[28] Реактив Шварца, подготовленный в 1970 году П. К. Уэйлсом и Х. Вейгольдом,[29] это металлоцен используется в органический синтез для преобразования алкены и алкины.[30]
Цирконий также входит в состав некоторых Катализаторы Циглера – Натта, используется для производства полипропилен. В этом приложении используется способность циркония обратимо образовывать связи с углеродом. Большинство комплексов Zr (II) являются производными цирконоцена, одним из примеров является (C5Мне5)2Zr (CO)2.
История
Цирконийсодержащий минерал циркон и родственные ему минералы (жаргун, гиацинт, гиацинт, ligure) упоминаются в библейских писаниях.[8][20] Минерал не содержал нового элемента до 1789 г.[31] когда Клапрот проанализировал жаргуна с острова Цейлон (ныне Шри-Ланка). Он назвал новый элемент Zirkonerde (диоксид циркония).[8] Хэмфри Дэви пытались выделить этот новый элемент в 1808 году с помощью электролиза, но безуспешно.[6] Металлический цирконий был впервые получен в нечистой форме в 1824 г. Берцелиус путем нагревания смеси калия и фторида циркония калия в железной трубке.[8]
В процесс кристалла (также известный как Йодидный процесс), открытый Антон Эдуард ван Аркель и Ян Хендрик де Бур в 1925 г. был осуществлен первый промышленный процесс промышленного производства металлического циркония. Он включает образование и последующее термическое разложение тетрайодид циркония, и в 1945 году был заменен гораздо более дешевым Кролл процесс разработан Уильям Джастин Кролл, в котором тетрахлорид циркония восстановлен магнием:[7][32]
- ZrCl4 + 2 Mg → Zr + 2 MgCl2
Приложения
В 1995 году было добыто около 900 000 тонн циркониевой руды, в основном в виде циркона.[19]
Соединения
Большая часть циркона используется непосредственно при высоких температурах. Этот материал тугоплавкий, твердый и устойчивый к химическому воздействию. Благодаря этим свойствам циркон находит множество применений, некоторые из которых широко освещаются. В основном он используется в качестве глушителя, придавая керамическим материалам белый непрозрачный вид. Из-за своей химической стойкости циркон также используется в агрессивных средах, таких как формы для расплавленных металлов.
Диоксид циркония (ZrO2) используется в лабораторных тиглях, в металлургических печах и как огнеупорный материал.[8] Поскольку он механически прочный и гибкий, его можно спеченный в керамические ножи и другие лезвия.[33] Циркон (ZrSiO4) и кубический цирконий (ZrO2) огранены на драгоценные камни для использования в ювелирных изделиях.
Цирконий входит в состав некоторых абразивы, например, шлифовальные круги и наждачная бумага.[31]
Металл
Небольшая часть циркона превращается в металл, который находит различные нишевые применения. Из-за превосходной устойчивости циркония к коррозии, он часто используется в качестве легирующего агента в материалах, которые подвергаются воздействию агрессивных сред, таких как хирургические инструменты, световые нити и корпуса часов. Высокая реакционная способность циркония с кислородом при высоких температурах используется в некоторых специализированных приложениях, таких как взрывные праймеры и геттеры в вакуумные трубки. Это же свойство (вероятно) является целью включения наночастиц Zr в качестве пирофорный материал во взрывном оружии, таком как Бомба комбинированного действия BLU-97 / B. Горящий цирконий использовался в качестве источника света в некоторых фотографические фотовспышки. Порошок циркония с размером ячеек от 10 до 80 иногда используется в пиротехнических композициях для получения искры. Высокая реакционная способность циркония приводит к появлению ярких белых искр.[34]
Ядерные приложения
Облицовка топлива ядерных реакторов потребляет около 1% циркония.[19] в основном в виде циркалои. Желаемые свойства этих сплавов - низкий захват нейтронов. поперечное сечение и устойчивость к коррозии при нормальных условиях эксплуатации.[7][8] Для этой цели были разработаны эффективные методы удаления примесей гафния.
Одним из недостатков циркониевых сплавов является то, что цирконий реагирует с водой при высоких температурах, образуя водород газ и ускоренная деградация оболочка твэлов:
- Zr + 2 H2O → ZrO2 + 2 часа2
Этот экзотермический реакция идет очень медленно ниже 100 ° C, но при температуре выше 900 ° C реакция идет быстро. Большинство металлов подвергаются аналогичным реакциям. Редокс-реакция связана с нестабильностью тепловыделяющие сборки при высоких температурах.[35] Эта реакция была ответственна за небольшой взрыв водорода, впервые наблюдаемый в здании реактора Три Майл Айленд АЭС в 1979 году, но на тот момент здание защитной оболочки не пострадало. Такая же реакция произошла в реакторах 1, 2 и 3 реактора. Атомная электростанция Фукусима I (Япония) после того, как охлаждение реактора было прервано из-за землетрясение и цунами катастрофа 11 марта 2011 г., приведшая к Ядерные аварии на фукусиме I. После выпуска водорода в ремонтном цехе этих трех реакторов смесь водорода с атмосферным кислород взорвались, серьезно повредив установки и, по крайней мере, одно из зданий защитной оболочки. Во избежание взрыва предпочтительным вариантом проектирования был бы прямой выпуск водорода в открытую атмосферу. Теперь, чтобы предотвратить опасность взрыва во многих реактор с водой под давлением (PWR) защитные сооружения, a катализатор-основан рекомбинатор установлен, который преобразует водород и кислород в воду комнатной температуры до возникновения опасности.[36] На некоторых коммерческих атомных станциях установлены водородные воспламенители для сжигания водорода по мере его образования, прежде чем он достигнет такой концентрации и объема, которые могут вызвать опасный взрыв.[37]
Цирконий входит в состав гидрид циркония урана (UZrH) ядерное топливо, используемое в TRIGA реакторы.
Космическая и авиационная промышленность
Материалы, изготовленные из металлического циркония и ZrO22 используются в космических аппаратах, где требуется термостойкость.[20]
Высокотемпературные детали, такие как камеры сгорания, лопатки и лопатки в реактивные двигатели и стационарный газовые турбины все больше защищены тонкими керамика слои, обычно состоящие из смеси диоксида циркония и иттрия.[38]
Камеры для позитронно-эмиссионной томографии
Изотоп 89Zr применялся для отслеживания и количественного определения молекулярных антител с позитронно-эмиссионная томография (ПЭТ) камеры (метод, называемый «иммуно-ПЭТ»). Иммуно-ПЭТ достигла зрелости в своей технической разработке и сейчас вступает в фазу широкомасштабного клинического применения.[39][40][41] До недавнего времени радиоактивная маркировка 89Zr был сложной процедурой, требующей нескольких этапов. В 2001–2003 годах была разработана улучшенная многоступенчатая процедура с использованием сукцинилированного производного десфериоксамин B (N-SucDf) как бифункциональный хелат,[42] и лучший способ привязки 89В 2009 году сообщалось о превращении Zr в mAb. Новый метод является быстрым, состоит всего из двух этапов и использует два широко доступных ингредиента: 89Zr и соответствующий хелат.[43] Текущие разработки также включают использование производных сидерофоров для связывания 89Zr (IV).[44][45]
Медицинское использование
Цирконийсодержащие соединения используются во многих биомедицинских приложениях, включая дентальные имплантаты и короны, замены коленного и бедренного суставов, среднего уха слуховой проход цепная реконструкция и другие восстановительные и протез устройств.[46]
Цирконий связывает мочевина, свойство, которое широко используется на благо пациентов с хроническая болезнь почек.[46] Например, цирконий является основным компонентом сорбент колонно-зависимая система регенерации и рециркуляции диализата, известная как система REDY, которая была впервые представлена в 1973 году. Более 2 000 000 диализ обработки проводились с использованием сорбционной колонки в системе REDY.[47] Хотя система REDY была заменена в 1990-х годах менее дорогостоящими альтернативами, новые системы диализа на основе сорбентов проходят оценку и одобряются в США. Управление по контролю за продуктами и лекарствами (FDA). Компания Renal Solutions разработала технологию DIALISORB, портативную систему диализа с низким содержанием воды. Кроме того, разрабатываемые версии носимой искусственной почки включают технологии на основе сорбентов.[нужна цитата]
Циклосиликат циркония натрия используется перорально при лечении гиперкалиемия. Это селективный сорбент, предназначенный для улавливания калий ионы предпочтительнее других ионы по всему желудочно-кишечному тракту.[48]
Смесь мономерного и полимерного Zr4+ и Al3+ комплексы с гидроксид, хлористый и глицин, называется Алюминий цирконий тетрахлоргидрекс гли или AZG, используется в препарате как антиперспирант во многих дезодорантах. Он выбран из-за его способности закрывать поры на коже и предотвращать выход пота из тела.
Несуществующие приложения
Карбонат циркония (3ZrO2· CO2·ЧАС2O) использовался в лосьонах для лечения Ядовитый плющ но было прекращено, поскольку иногда вызывали кожные реакции.[6]
Безопасность
| Опасности | |
|---|---|
| NFPA 704 (огненный алмаз) | |
Хотя цирконий не имеет известной биологической роли, человеческое тело содержит в среднем 250 миллиграммов циркония, а суточное потребление составляет примерно 4,15 миллиграмма (3,5 миллиграмма с пищей и 0,65 миллиграмма с водой), в зависимости от диетических привычек.[49] Цирконий широко распространен в природе и присутствует во всех биологических системах, например: 2,86 мкг / г в цельной пшенице, 3,09 мкг / г в коричневом рисе, 0,55 мкг / г в шпинат, 1,23 мкг / г в яйцах и 0,86 мкг / г в говяжьем фарше.[49] Кроме того, цирконий обычно используется в коммерческих продуктах (например, дезодорант палочки, аэрозоль антиперспиранты), а также при очистке воды (например, контроль фосфор загрязненная вода, загрязненная бактериями и пирогенами).[46]
Кратковременное воздействие порошка циркония может вызвать раздражение, но только попадание в глаза требует медицинской помощи.[50] Постоянное воздействие тетрахлорид циркония приводит к увеличению смертности крыс и морских свинок и уменьшению количества крови гемоглобин и красные кровяные тельца у собак. Однако в исследовании с участием 20 крыс, получавших стандартную диету, содержащую ~ 4% оксида циркония, не было выявлено неблагоприятных эффектов на скорость роста, параметры крови и мочи или смертность.[51] Соединенные штаты. Управление по охране труда (OSHA) законный предел (допустимый предел воздействия) для циркония составляет 5 мг / м3 за 8-часовой рабочий день. В Национальный институт охраны труда и здоровья (NIOSH) рекомендуемый предел воздействия (REL) составляет 5 мг / м3 более 8-часовой рабочий день и краткосрочный предел 10 мг / м33. На уровне 25 мг / м3, цирконий сразу опасно для жизни и здоровья.[52] Однако цирконий не считается опасным для здоровья на производстве.[46] Кроме того, сообщения о побочных реакциях, связанных с цирконием, редки, и, как правило, строгих причинно-следственных связей не установлено.[46] Нет подтвержденных доказательств канцерогенности или генотоксичности циркония.[53]
Среди многочисленных радиоактивных изотопов циркония 93Zr - один из самых распространенных. Он выпущен как продукт ядерного деления из 235U и 239Pu, главным образом на атомных электростанциях и во время испытаний ядерного оружия в 1950-х и 1960-х годах. Он имеет очень длительный период полураспада (1,53 миллиона лет), его распад вызывает только низкоэнергетическое излучение, и он не считается особо опасным.[54]
Смотрите также
Рекомендации
- ^ Мейя, Юрис; и другие. (2016). «Атомный вес элементов 2013 (Технический отчет IUPAC)». Чистая и прикладная химия. 88 (3): 265–91. Дои:10.1515 / pac-2015-0305.
- ^ «Цирконий: данные фторидного соединения циркония (I)». OpenMOPAC.net. Получено 2007-12-10.
- ^ Лиде, Д. Р., изд. (2005). «Магнитная восприимчивость элементов и неорганических соединений». CRC Справочник по химии и физике (PDF) (86-е изд.). Бока-Ратон (Флорида): CRC Press. ISBN 0-8493-0486-5.
- ^ Притыченко, Борис; Третьяк, В. "Принятые данные о двойном бета-распаде". Национальный центр ядерных данных. Получено 2008-02-11.
- ^ Харпер, Дуглас. "циркон". Интернет-словарь этимологии.
- ^ а б c d Эмсли, Джон (2001). Строительные блоки природы. Оксфорд: Издательство Оксфордского университета. С. 506–510. ISBN 978-0-19-850341-5.
- ^ а б c d е "Цирконий". Как производятся продукты. Advameg Inc. 2007. Получено 2008-03-26.
- ^ а б c d е ж грамм час я j k Лиде, Дэвид Р., изд. (2007–2008). "Цирконий". CRC Справочник по химии и физике. 4. Нью-Йорк: CRC Press. п. 42. ISBN 978-0-8493-0488-0.
- ^ Консидайн, Гленн Д., изд. (2005). "Цирконий". Энциклопедия химии Ван Ностранда. Нью-Йорк: Wylie-Interscience. С. 1778–1779. ISBN 978-0-471-61525-5.
- ^ Зима, Марк (2007). "Электроотрицательность (Полинг)". Университет Шеффилда. Получено 2008-03-05.
- ^ Schnell I & Albers RC (январь 2006 г.). «Цирконий под давлением: фазовые переходы и термодинамика».. Журнал физики: конденсированное вещество. 18 (5): 16. Bibcode:2006JPCM ... 18.1483S. Дои:10.1088/0953-8984/18/5/001.
- ^ а б c Ауди, Жорж; Берсильон, Оливье; Blachot, Жан; Вапстра, Алдерт Хендрик (2003), "ТогдаUBASE оценка ядерных и распадных свойств », Ядерная физика A, 729: 3–128, Bibcode:2003НуФА.729 .... 3А, Дои:10.1016 / j.nuclphysa.2003.11.001
- ^ а б Петерсон, Джон; Макдонелл, Маргарет (2007). "Цирконий". Информационные бюллетени по радиологическим и химическим веществам в поддержку анализа рисков для здоровья в загрязненных районах (PDF). Аргоннская национальная лаборатория. С. 64–65. Архивировано из оригинал (PDF) на 2008-05-28. Получено 2008-02-26.
- ^ «Цирконий и гафний - минеральные ресурсы» (PDF). 2014.
- ^ а б «Цирконий и гафний» (PDF). Обзоры минерального сырья: 192–193. Январь 2008 г.. Получено 2008-02-24.
- ^ Ральф, Джолион и Ральф, Ида (2008). «Минералы, содержащие Zr». Mindat.org. Получено 2008-02-23.
- ^ Abraham, M. M .; Ботнер, Л. А .; Ramey, J. O .; Раппаз, М. (1984-12-20). «Наличие и стабильность трехвалентного циркония в монокристаллах ортофосфатов». Журнал химической физики. 81 (12): 5362–5366. Дои:10.1063/1.447678. ISSN 0021-9606.
- ^ Каллаган, Р. (21 февраля 2008 г.). «Статистика и информация по цирконию и гафнию». Геологическая служба США. Получено 2008-02-24.
- ^ а б c d Нильсен, Ральф (2005) «Цирконий и соединения циркония» в Энциклопедии промышленной химии Ульмана, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a28_543
- ^ а б c Ствертка, Альберт (1996). Путеводитель по элементам. Издательство Оксфордского университета. С. 117–119. ISBN 978-0-19-508083-4.
- ^ Брэди, Джордж Стюарт; Клаузер, Генри Р. и Ваккари, Джон А. (24 июля 2002 г.). Справочник по материалам: энциклопедия для менеджеров, технических специалистов, менеджеров по закупкам и производству, технических специалистов и руководителей. McGraw-Hill Professional. С. 1063–. ISBN 978-0-07-136076-0. Получено 2011-03-18.
- ^ Zardiackas, Lyle D .; Краай, Мэтью Дж. И Фриз, Ховард Л. (1 января 2006 г.). Титан, ниобий, цирконий и тантал для медицинского и хирургического применения. ASTM International. С. 21–. ISBN 978-0-8031-3497-3. Получено 2011-03-18.
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ а б «Цирконий». AZoM.com. 2008 г.. Получено 2008-03-17.
- ^ Gauthier, V .; Dettenwanger, F .; Шютце, М. (2002-04-10). «Окислительное поведение γ-TiAl, покрытого термическими барьерами из диоксида циркония». Интерметаллиды. 10 (7): 667–674. Дои:10.1016 / S0966-9795 (02) 00036-5.
- ^ Кинан, П. К. (1954). «Классификация звезд S-типа». Астрофизический журнал. 120: 484–505. Bibcode:1954ApJ ... 120..484K. Дои:10.1086/145937.
- ^ Паспорт безопасности материалов для Duratec 400, DuBois Chemicals, Inc.
- ^ Уилкинсон, Г.; Бирмингем, Дж. М. (1954). «Бис-циклопентадиенильные соединения Ti, Zr, V, Nb и Ta». Журнал Американского химического общества. 76 (17): 4281–4284. Дои:10.1021 / ja01646a008.; Рухи, А. Морин (2004-04-19). "Прибытие органоциркониевой химии". Новости химии и машиностроения. 82 (16): 36–39. Дои:10.1021 / cen-v082n016.p036. ISSN 0009-2347. Получено 2008-03-17.
- ^ Уэйлс, П. К. и Вейголд, Х. (1970). «Гидридокомплексы циркония I. Получение». Журнал металлоорганической химии. 24 (2): 405–411. Дои:10.1016 / S0022-328X (00) 80281-8.
- ^ Харт, Д. В. и Шварц, Дж. (1974). «Гидроциркония. Органический синтез с использованием циркониевых промежуточных соединений. Синтез и перегруппировка комплексов алкилциркония (IV) и их реакция с электрофилами». Журнал Американского химического общества. 96 (26): 8115–8116. Дои:10.1021 / ja00833a048.
- ^ а б Кребс, Роберт Э. (1998). История и использование химических элементов нашей Земли. Вестпорт, Коннектикут: Greenwood Press. стр.98–100. ISBN 978-0-313-30123-0.
- ^ Хедрик, Джеймс Б. (1998). "Цирконий". Цены на металлы в США до 1998 г. (PDF). Геологическая служба США. С. 175–178. Получено 2008-02-26.
- ^ «Изысканная керамика - цирконий». Kyocera Inc.
- ^ Kosanke, Kenneth L .; Косанке, Бонни Дж. (1999), «Генерация пиротехнической искры», Журнал пиротехники: 49–62, ISBN 978-1-889526-12-6
- ^ Гиллон, Люк (1979). Le nucléaire en question, Gembloux Duculot, французское издание.
- ^ Arnould, F .; Bachellerie, E .; Auglaire, M .; Boeck, D .; Braillard, O .; Eckardt, B .; Ferroni, F .; Moffett, R .; Ван Гетем, Г. (2001). "Современное состояние пассивного автокаталитического рекомбинатора водорода" (PDF). 9-я Международная конференция по ядерной инженерии, Ницца, Франция, 8–12 апреля 2001 г.. Получено 4 марта 2018.
- ^ Лейз, Марк (март 2014 г.). «Предотвращение водородных взрывов при тяжелых ядерных авариях: нерешенные вопросы безопасности, связанные с производством водорода и смягчением их последствий» (PDF). NRDC. Получено 30 апреля 2020.
- ^ Meier, S.M .; Гупта, Д. К. (1994). «Эволюция термобарьерных покрытий в газотурбинных двигателях». Журнал инженерии газовых турбин и энергетики. 116: 250–257. Дои:10.1115/1.2906801.
- ^ Heuveling, Дерек А .; Visser, Gerard W. M .; Баклайон, Мэриан; Roos, Wouter H .; Wuite, Gijs J. L .; Hoekstra, Otto S .; Лиманс, К. Рене; де Бри, Ремко; ван Донген, Гус А.М.С. (2011). "89ПЭТ / КТ-лимфосцинтиграфия на основе Zr-наноколлоидного альбумина для обнаружения сторожевых узлов при раке головы и шеи: доклинические результаты » (PDF). Журнал ядерной медицины. 52 (10): 1580–1584. Дои:10.2967 / jnumed.111.089557. PMID 21890880.
- ^ van Rij, Catharina M .; Шарки, Роберт М .; Гольденберг, Дэвид М .; Frielink, Cathelijne; Molkenboer, Janneke D.M .; Franssen, Gerben M .; van Weerden, Wietske M .; Oyen, Wim J. G .; Боерман, Отто К. (2011). «Визуализация рака простаты с помощью иммуно-ПЭТ и иммуно-ОФЭКТ с использованием радиоактивно меченного моноклонального антитела против EGP-1». Журнал ядерной медицины. 52 (10): 1601–1607. Дои:10.2967 / jnumed.110.086520. PMID 21865288.
- ^ Ruggiero, A .; Holland, J. P .; Худолин, Т .; Шенкер, Л .; Кулова, А .; Bander, N.H .; Lewis, J. S .; Гримм, Дж. (2011). «Нацеливание на внутренний эпитоп простатоспецифического мембранного антигена с помощью иммуно-ПЭТ 89Zr-7E11». Журнал ядерной медицины. 52 (10): 1608–15. Дои:10.2967 / jnumed.111.092098. ЧВК 3537833. PMID 21908391.
- ^ Верель, И .; Visser, G.W .; Boellaard, R .; Stigter-Van Walsum, M .; Сноу, Г. Б .; Ван Донген, Г. А. (2003). «89Zr иммуно-ПЭТ: Комплексные процедуры производства 89Zr-меченные моноклональные антитела » (PDF). J Nucl Med. 44 (8): 1271–81. PMID 12902418.
- ^ Перк, L, «Будущее иммуно-ПЭТ в разработке лекарств. Цирконий-89 и йод-124 как ключевые факторы в молекулярной визуализации» В архиве 25 апреля 2012 г. Wayback Machine, Амстердам, Циклотрон, 2009.
- ^ Дери, Мелисса А .; Поннала, Шашикант; Зеглис, Брайан М .; Поль, Габор; Dannenberg, J. J .; Льюис, Джейсон С .; Франческони, Линн С. (12.06.2014). «Альтернативный хелатор для радиофармпрепаратов 89Zr: радиоактивная мечение и оценка 3,4,3- (LI-1,2-HOPO)». Журнал медицинской химии. 57 (11): 4849–4860. Дои:10.1021 / jm500389b. ISSN 0022-2623. ЧВК 4059252. PMID 24814511.
- ^ Капитан Илья; Deblonde, Gauthier J.-P .; Руперт, Питер Б.; An, Dahlia D .; Или, Мари-Клэр; Ростан, Эмелин; Ralston, Corie Y .; Сильный, Роланд К .; Абергель, Ребекка Дж. (21 ноября 2016 г.). «Инженерное распознавание четырехвалентного циркония и тория с помощью хелаторно-белковых систем: на пути к гибким платформам лучевой терапии и визуализации». Неорганическая химия. 55 (22): 11930–11936. Дои:10.1021 / acs.inorgchem.6b02041. ISSN 0020-1669. PMID 27802058.
- ^ а б c d е Ли ДБН, Робертс М., Блючел К.Г., Оделл Р.А. (2010) Цирконий: биомедицинские и нефрологические приложения. ASAIO J 56 (6): 550-556.
- ^ Ясень SR. Сорбенты в лечении уремии: краткая история и большое будущее. 2009 Семин Набери 22: 615-622
- ^ Ингельфингер, Джули Р. (2015). «Новая эра лечения гиперкалиемии?». Медицинский журнал Новой Англии. 372 (3): 275–7. Дои:10.1056 / NEJMe1414112. PMID 25415806.
- ^ а б Шредер, Генри А .; Баласса, Джозеф Дж. (Май 1966 г.). «Аномальные следы металлов в человеке: цирконий». Журнал хронических болезней. 19 (5): 573–586. Дои:10.1016/0021-9681(66)90095-6. PMID 5338082.
- ^ "Цирконий". Международные карты химической безопасности. Международная организация труда. Октябрь 2004 г.. Получено 2008-03-30.
- ^ Цирконий и его соединения 1999. Сборник МАК по охране труда. 224–236
- ^ «CDC - Карманный справочник NIOSH по химическим опасностям - соединения циркония (как Zr)». www.cdc.gov. Получено 2015-11-27.
- ^ toxnet.nlm.nih.gov/cgi-bin/sis/search/f?./temp/~EHRbeW:2
- ^ «Информационный бюллетень ANL о здоровье человека: цирконий (октябрь 2001 г.)» (PDF). Аргоннская национальная лаборатория. Получено 15 июля 2020.
внешняя ссылка
- Подкаст "Химия в ее стихии" (MP3) из Королевское химическое обществос Мир химии: Цирконий
- Цирконий в Периодическая таблица видео (Ноттингемский университет)