WikiDer > S-аденозил-L-гомоцистеин
 | |
| Имена | |
|---|---|
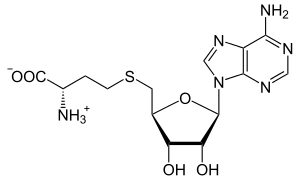
| Название ИЮПАК S- (5′-дезоксиаденоз-5′-ил) -л-гомоцистеин | |
| Другие имена AdoHcy, 2-S-аденозил-л-гомоцистеин, 5′-S- (3-Амино-3-карбоксипропил) -5'-тиоаденозинS-аденозилгомоцистеин, SAH | |
| Идентификаторы | |
3D модель (JSmol) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.012.328 |
| КЕГГ | |
| MeSH | S-аденозилгомоцистеин |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C14ЧАС20N6О5S | |
| Молярная масса | 384.412 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
S-Аденозил-л-гомоцистеин (SAH) это биосинтетический предшественник гомоцистеин.[1] SAH формируется деметилирование из S-аденозил-л-метионин.[2][3] Аденозилгомоцистеиназа превращает SAH в гомоцистеин и аденозин.
Рекомендации
- ^ Финкельштейн, Дж. Д. (2000). «Пути и регуляция метаболизма гомоцистеина у млекопитающих». Семин. Тромб. Хемост. 26: 219–225. Дои:10.1055 / с-2000-8466. PMID 11011839.
- ^ Ribbe, M. W .; Hu, Y .; Hodgson, K. O .; Хедман, Б. (2014). «Биосинтез металлокластеров нитрогеназ». Chem. Rev. 114 (8): 4063–4080. Дои:10.1021 / cr400463x. ЧВК 3999185. PMID 24328215.
- ^ Джеймс, С. Джилл; Мельник, Степан; Погрибна, Марта; Погрибный, Игорь П; Кодилл, Мари А (2002). «Повышение уровня S-аденозилгомоцистеина и гипометилирования ДНК: потенциальный эпигенетический механизм патологии, связанной с гомоцистеином». Журнал питания. 132 (8): 2361S – 2366S. Дои:10.1093 / jn / 132.8.2361S. PMID 12163693.
внешняя ссылка
| Этот биохимия статья - это заглушка. Вы можете помочь Википедии расширяя это. |