WikiDer > Метионин
 Каноническая форма метионина | |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Метионин | |||
| Другие имена 2-амино-4- (метилтио) бутановая кислота | |||
| Идентификаторы | |||
3D модель (JSmol) | |||
| Сокращения | Met, M | ||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.393 | ||
| Номер ЕС |
| ||
| КЕГГ | |||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Свойства[2] | |||
| C5ЧАС11NО2S | |||
| Молярная масса | 149.21 г · моль−1 | ||
| Внешность | Белый кристаллический порошок | ||
| Плотность | 1,340 г / см3 | ||
| Температура плавления | 281 ° С (538 ° F, 554 К) разлагается | ||
| Растворимый | |||
| Кислотность (пKа) | 2,28 (карбоксил), 9,21 (амино)[1] | ||
| Фармакология | |||
| V03AB26 (КТО) QA05BA90 (КТО), QG04BA90 (КТО) | |||
| Страница дополнительных данных | |||
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее. | |||
Термодинамический данные | Фазовое поведение твердое тело – жидкость – газ | ||
| УФ, ИК, ЯМР, РС | |||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Метионин (символ Встретил или M)[3] (/мɪˈθаɪəпяп/)[4] является незаменимая аминокислота в людях. В качестве субстрата для других аминокислот, таких как цистеин и таурин, универсальные соединения, такие как Такой же, и важный антиоксидант глутатион, метионин играет решающую роль в метаболизме и здоровье многих видов, включая человека. это закодированный посредством кодон АВГ.
Метионин также является важной частью ангиогенез, рост новых кровеносных сосудов. Добавка может принести пользу людям, страдающим от отравления медью.[5] Чрезмерное потребление метионина, метильная группа донор в Метилирование ДНК, связан с ростом рака в ряде исследований.[6][7] Метионин был впервые выделен в 1921 г. Джон Ховард Мюллер.[8]
Биохимические детали
Метионин (сокращенно Встретил или M; кодируется кодоном AUG) является α-аминокислота что используется в биосинтез из белки. Он содержит α-аминогруппу (которая находится в протонированный −NH3+ форма в биологических условиях), карбоксильная группа (который находится в депротонированном -COO− форма в биологических условиях) и S-метил тиоэфир боковая цепь, классифицируя ее как неполярный, алифатический аминокислота.
В ядерных генах эукариоты И в Археи, метионин кодируется стартовый кодон, то есть указывает на начало кодирующая область и является первой аминокислотой, производимой в зарождающемся полипептид в течение мРНК перевод.[9]
Протеиногенная аминокислота
Вместе с цистеин, метионин - один из двух сера-содержащий протеиногенные аминокислоты. За исключением нескольких исключений, когда метионин может действовать как датчик окислительно-восстановительного потенциала (например.,[10]), остатки метионина не играют каталитической роли.[11] Это контрастирует с остатками цистеина, где тиоловая группа играет каталитическую роль во многих белках.[11] Однако тиоэфир играет незначительную структурную роль из-за эффекта стабильности S / π взаимодействия между атомом серы боковой цепи и ароматическими аминокислотами в одной трети всех известных белковых структур.[11] Это отсутствие сильной роли отражено в экспериментах, где небольшой эффект наблюдается у белков, в которых метионин заменен на норлейцинаминокислота с прямой углеводородной боковой цепью, в которой отсутствует тиоэфир.[12]Было высказано предположение, что норлейцин присутствовал в ранних версиях генетического кода, но метионин вторгся в окончательную версию генетического кода из-за того, что он используется в кофакторе. S-аденозилметионин (СЭМ).[13] Эта ситуация не уникальна и могла произойти с орнитином и аргинином.[14]
Кодирование
Метионин - одна из двух аминокислот, кодируемых одним кодон (AUG) в стандарте генетический код (триптофан, закодированный UGG, является другим). Отражая эволюционное происхождение его кодона, другие кодоны AUN кодируют изолейцин, который также является гидрофобной аминокислотой. В митохондриальном геноме нескольких организмов, в том числе метазоа и дрожжикодон AUA также кодирует метионин. В стандартном генетическом коде AUA кодирует изолейцин и соответствующую тРНК (ileX в кишечная палочка) использует необычную базу лизидин (бактерии) или агматидин (археи), чтобы дискриминировать AUG.[15][16]
Кодон метионина AUG также является наиболее распространенным стартовым кодоном. Кодон «Старт» - это сообщение для рибосома что сигнализирует об инициации белка перевод из мРНК, когда кодон AUG находится в Консенсусная последовательность Козака. Как следствие, метионин часто включается в N-концевое положение белки в эукариоты и археи во время перевода, хотя его можно удалить посттрансляционная модификация. В бактерии, производная N-формилметионин используется в качестве исходной аминокислоты.
Производные
S-аденозил-метионин
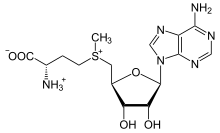
Производное метионина S-аденозилметионин (SAM) - кофактор, который служит главным образом метил донор. SAM состоит из молекулы аденозила (через 5 'углерод), присоединенной к сере метионина, что делает его сульфоний катион (т.е. три заместителя и положительный заряд). Сера действует как мягкая кислота Льюиса (т.е. донор / электрофил), что позволяет S-метильная группа для переноса в кислородную, азотную или ароматическую систему, часто с помощью других кофакторов, таких как кобаламин (витамин B12 в организме человека). Некоторые ферменты используют SAM для инициирования радикальной реакции; они называются радикальный SAM Ферменты.В результате переноса метильной группы получается S-аденозил-гомоцистеин. У бактерий он либо регенерируется путем метилирования, либо восстанавливается путем удаления аденина и гомоцистеина, в результате чего соединение дигидроксипентандион спонтанно превращается в автоиндуктор-2, который выводится как побочный продукт / сигнал кворума.
Биосинтез
Как незаменимая аминокислота метионин не синтезируется. de novo у людей и других животных, которые должны принимать метионин или метионинсодержащие белки. У растений и микроорганизмов биосинтез метионина относится к аспартат семья, наряду с треонином и лизин (через диаминопимелат, но не через α-аминоадипат). Основная магистраль происходит от аспарагиновая кислота, а сера может поступать из цистеин, метантиол, или сероводород.[11]
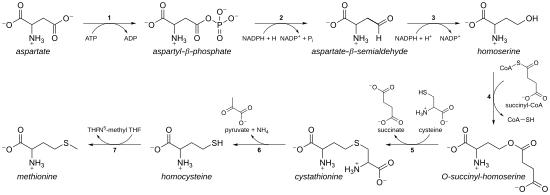
- Сначала аспарагиновая кислота превращается через β-аспартил-полуальдегид в гомосерин двумя стадиями восстановления концевой карбоксильной группы (гомосерин, следовательно, имеет γ-гидроксил, следовательно, гомо- серии). Промежуточный аспартат-полуальдегид является точкой разветвления пути биосинтеза лизина, где он вместо этого находится конденсированный с пируватом. Гомосерин является точкой разветвления треонинового пути, где вместо этого он изомеризуется после активации концевого гидроксила фосфатом (также используется для биосинтеза метионина в растениях).[11]
- Затем гомосерин активируется фосфатной, сукцинильной или ацетильной группой гидроксила.
- У растений и, возможно, у некоторых бактерий,[11] фосфат используется. Этот этап используется совместно с биосинтезом треонина.[11]
- У большинства организмов ацетильная группа используется для активации гомосерина. В бактериях это может быть катализатором с помощью фермента, кодируемого metX или мета (не гомологи).[11]
- В энтеробактерии и в ограниченном количестве других организмов используется сукцинат. Фермент, который катализирует реакцию, - это MetA, а специфичность к ацетил-КоА и сукцинил-КоА определяется одним резидентом.[11] Физиологическая основа предпочтения ацетил-КоА или сукцинил-КоА неизвестна, но такие альтернативные пути присутствуют в некоторых других путях (например биосинтез лизина и биосинтез аргинина).
- Затем активирующую гидроксил группу заменяют цистеином, метантиолом или сероводородом. Реакция замещения технически представляет собой γ-устранение за которым следует вариант Майкл дополнение. Все задействованные ферменты являются гомологами и членами Метаболизм Cys / Met Семейство PLP-зависимых ферментов, которая является подмножеством PLP-зависимой клады типа I. Они используют кофактор PLP (пиридоксальфосфат), который функционирует, стабилизируя карбанионные промежуточные соединения.[11]
- Если он реагирует с цистеином, он производит цистатионин, который раскалывается, чтобы дать гомоцистеин. Участвующие ферменты: цистатионин-γ-синтаза (закодировано metB в бактериях) и цистатионин-β-лиаза (metC). Цистатионин по-разному связывается двумя ферментами, позволяя протекать β- или γ-реакциям.[11]
- Если он реагирует со свободным сероводородом, он производит гомоцистеин. Это катализируется О-ацетилгомосерин-аминокарбоксипропилтрансфераза (ранее известный как О-ацетилгомосерин (тиол) -лиаза. Он кодируется либо встретил или metZ в бактериях.[11]
- Если он вступает в реакцию с метантиолом, он производит непосредственно метионин. Метантиол является побочным продуктом катаболического пути некоторых соединений, поэтому этот путь более редок.[11]
- Если гомоцистеин продуцируется, тиоловая группа метилируется с образованием метионина. Два метионинсинтазы известны; один кобаламин (витамин B12) зависимый и один независимый.[11]
Путь с использованием цистеина называется "путь транссульфурации", тогда как путь с использованием сероводорода (или метантиола) называется" путем прямого сульфурирования ".
Цистеин продуцируется аналогичным образом, а именно, он может быть получен из активированного серина и либо из гомоцистеина («путь обратного транс-сульфурилирования»), либо из сероводорода («путь прямого сульфурирования»); активированный серин обычно О-ацетил-серин (через CysK или CysM в Кишечная палочка), но в Аэропирум перникс и некоторые другие археи О-фосфосерин используется.[17] CysK и CysM являются гомологами, но принадлежат к кладе типа III складки PLP.
Путь транс-сульфулирования
Ферменты, участвующие в Кишечная палочка путь транс-сульфулирования биосинтеза метионина:
- Аспартокиназа
- Аспартат-полуальдегиддегидрогеназа
- Гомосериндегидрогеназа
- Гомосерин-О-транссукцинилаза
- Цистатионин-γ-синтаза
- Цистатионин-β-лиаза
- Метионинсинтаза (у млекопитающих этот шаг выполняется гомоцистеинметилтрансфераза или бетаин-гомоцистеин-S-метилтрансфераза.)
Другие биохимические пути
Хотя млекопитающие не могут синтезировать метионин, они все же могут использовать его в различных биохимических путях:
Катаболизм
Метионин превращается в S-аденозилметионин (SAM) пользователем (1) метионин аденозилтрансфераза.
SAM служит донором метила во многих (2) метилтрансфераза реакции, и преобразуется в S-аденозилгомоцистеин (САХ).
(3) Аденозилгомоцистеиназацистеин.
Регенерация
Метионин можно регенерировать из гомоцистеина через (4) метионинсинтаза в реакции, которая требует витамин B12 как кофактор.
Гомоцистеин также можно реметилировать с помощью глицин бетаин (NNN-триметилглицин, TMG) в метионин через фермент бетаин-гомоцистеин-метилтрансфераза (E.C.2.1.1.5, BHMT). BHMT составляет до 1,5% от всего растворимого белка печени, и недавние данные свидетельствуют о том, что он может иметь большее влияние на гомеостаз метионина и гомоцистеина, чем метионинсинтаза.
Путь обратного трансульфурилирования: превращение в цистеин
Гомоцистеин можно превратить в цистеин.
- (5) Цистатионин-β-синтаза (фермент, который требует активной формы витамин B6, пиридоксальфосфат) объединяет гомоцистеин и серин для производства цистатионин. Вместо того, чтобы унижать цистатионин через цистатионин-β-лиаза, как и в биосинтетическом пути, цистатионин расщепляется на цистеин и α-кетобутират через (6) цистатионин-γ-лиаза.
- (7) Фермент α-кетокислота дегидрогеназа превращает α-кетобутират в пропионил-КоА, который метаболизируется до сукцинил-КоА в трехэтапном процессе (см. пропионил-КоА для пути).
Синтез этилена
Эта аминокислота также используется растения для синтеза этилен. Этот процесс известен как Ян цикл или цикл метионина.
Химический синтез
Промышленный синтез объединяет акролеин, метантиол, и цианид, который дает гидантоин.[18]Рацемический метионин также может быть синтезирован из фталимидомалоната диэтилнатрия путем алкилирования хлорэтилметилсульфидом (ClCH2CH2SCH3) с последующим гидролизом и декарбоксилированием.[19]
Питание человека
Требования
Совет по пищевым продуктам и питанию Института медицины США установил рекомендуемые диетические нормы (RDA) для незаменимые аминокислоты в 2002 г. Для метионина в сочетании с цистеином, для взрослых от 19 лет и старше, 19 мг / кг массы тела / день.[20]
Диетические источники
| Еда | г / 100г |
|---|---|
| Яйцо, белый, сушеный, порошок, с пониженным содержанием глюкозы | 3.204 |
| семена кунжута мука (нежирная) | 1.656 |
| бразильский орех | 1.124 |
| Сыр, Пармезан, тертый | 1.114 |
| семена конопли, лущеный | 0.933 |
| Концентрат соевого белка | 0.814 |
| Курица, бройлеры или фритюрницы, жареные | 0.801 |
| Рыбы, тунец, светлый, консервированный в воде, сушеные твердые вещества | 0.755 |
| Говядина, вяленый, сушеный | 0.749 |
| Бекон | 0.593 |
| Семена чиа | 0.588 |
| Говядина, фарш, 95% нежирного мяса / 5% жира, сырое | 0.565 |
| Свинина, молотый, 96% постное / 4% жирное, сырое | 0.564 |
| Зародыши пшеницы | 0.456 |
| Яйцо, целиком, вареные, сваренные вкрутую | 0.392 |
| Овсяный | 0.312 |
| Арахис | 0.309 |
| Нута | 0.253 |
| Кукуруза, желтый | 0.197 |
| Миндаль | 0.151 |
| Фасоль, пинто, приготовленная | 0.117 |
| Чечевица, приготовленный | 0.077 |
| Рис, коричневый, среднезернистый, приготовленный | 0.052 |
Высокий уровень метионина содержится в яйцах, мясе и рыбе; семена кунжута, бразильские орехи и некоторые другие семена растений; и крупа зерна. Большинство фруктов и овощей содержат очень мало. Наиболее бобовыехотя и плотный, но с низким содержанием метионина. Белки без адекватного количества метионина не считаются полные белки.[22] По этой причине рацемический метионин иногда добавляют в качестве ингредиента к корма для домашних животных.[23]
Ограничение
Некоторые научные данные показывают, что ограничение потребления метионина может увеличить продолжительность жизни плодовых мух.[24]
Исследование 2005 года показало, что ограничение метионина без ограничения энергии увеличивает продолжительность жизни мышей.[25] Это удлинение требует интактной передачи сигналов гормона роста, поскольку животные без интактной передачи сигналов гормона роста не имеют дальнейшего увеличения продолжительности жизни при ограничении метионина.[26] Метаболический ответ на ограничение метионина также изменяется у сигнальных мутантов гормона роста мышей.[27]
Исследование, опубликованное в Природа показали добавление только незаменимой аминокислоты метионина в рацион плодовые мошки при диетических ограничениях, включая ограничение незаменимые аминокислоты (EAAs), восстановлено плодородие без сокращения продолжительности жизни, типичной для ограничений в питании, что привело исследователей к выводу, что метионин «действует в сочетании с одним или несколькими другими EAA, сокращая продолжительность жизни».[24][28][29] Восстановление метионина в рационе мышей, соблюдающих режим ограничения диеты, блокирует многие преимущества ограничения в питании, процесс, который может быть опосредован увеличением производства сероводорода.[30]
Несколько исследований показали, что ограничение метионина также подавляет связанные со старением болезненные процессы у мышей.[31][32] и подавляет канцерогенез толстой кишки у крыс.[33] У людей ограничение метионина путем модификации диеты может быть достигнуто с помощью растительной диеты.[34]
Ограничение диетического метионина снижает уровень его катаболита. S-аденозилметионин (SAM), что приводит к последующей потере метилирование гистонов.[35] Активный процесс, опосредованный конкретным, сохраненным метилирование H3K9 сохраняет память об исходном профиле метилирования, позволяя эпигеном восстанавливается при восстановлении уровня метионина в рационе.[35]
Исследование на крысах, проведенное в 2009 году, показало, что «добавление метионина в рацион специально увеличивает митохондриальную активность. ROS производство и митохондрии ДНК окислительное повреждение в печени крысы митохондрии предлагая правдоподобный механизм для гепатотоксичность".[36]
Однако, поскольку метионин является незаменимая аминокислота, его нельзя полностью исключить из рациона животных без болезни или смерти со временем.[нужна цитата] Например, у крыс, получавших диету без метионина и холина, развилась стеатогепатит (жирная печень) и анемия, и потеряли две трети своего веса за 5 недель. Прием метионина улучшил патологические последствия метиониновой депривации.[37] Кратковременное исключение из рациона только метионина может обратить вспять вызванное диетой ожирение и повысить чувствительность к инсулину у мышей.[38] и ограничение метионина также защищает мышиную модель спонтанного полигенного ожирения и диабета.[39]
Здоровье
Потеря метионина связана с старческим поседением волос. Его недостаток приводит к накоплению перекиси водорода в волосяных фолликулах, снижению эффективности тирозиназы и постепенной потере цвета волос.[40]Метионин повышает внутриклеточную концентрацию GSH, тем самым способствуя антиоксидантной защите клеток и окислительно-восстановительной регуляции. Он также защищает клетки от потери нигральных клеток, вызванной допамином, путем связывания окислительных метаболитов.[41]
Метионин является промежуточным звеном в биосинтезе цистеин, карнитин, таурин, лецитин, фосфатидилхолин, и другие фосфолипиды. Неправильная конверсия метионина может привести к атеросклероз[42] из-за накопления гомоцистеин.
Метионин также может иметь важное значение для обращения вспять повреждающего метилирования глюкокортикоидных рецепторов, вызванного повторяющимся стрессовым воздействием, с последствиями для депрессии.[43]
Другое использование
DL-Метионин иногда назначают собакам в качестве добавки; Это помогает снизить вероятность образования камней в почках у собак. Также известно, что метионин увеличивает выведение хинидина с мочой за счет подкисления мочи. Аминогликозидные антибиотики, используемые для лечения инфекций мочевыводящих путей, лучше всего работают в щелочных условиях, а закисление мочи при использовании метионина может снизить его эффективность. Если собака сидит на диете, которая подкисляет мочу, использовать метионин не следует.[44]
Метионин разрешен в качестве добавки к органическому корму для птицы в рамках сертифицированной органической программы США.[45]
Метионин можно использовать в качестве нетоксичного пестицида против гигантский ласточкин хвост гусеницы, являющиеся серьезным вредителем апельсиновых культур.[46]
Смотрите также
- Аллантоин
- Формилметионин
- Окисление метионина
- Отравление парацетамолом
- Фотореактивный метионин
- S-метилцистеин
использованная литература
- ^ Доусон Р.М., Эллиотт, округ Колумбия, Эллиотт WH, Джонс К.М. (1959). Данные для биохимических исследований. Оксфорд: Clarendon Press.
- ^ Weast, Роберт С., изд. (1981). CRC Справочник по химии и физике (62-е изд.). Бока-Ратон, Флорида: CRC Press. п. С-374. ISBN 0-8493-0462-8..
- ^ «Номенклатура и символика аминокислот и пептидов». Совместная комиссия IUPAC-IUB по биохимической номенклатуре. 1983. Архивировано с оригинал 9 октября 2008 г.. Получено 5 марта 2018.
- ^ «Метионин». Издательство Оксфордского университета.
- ^ «Метионин». WebMD.
- ^ Кавуото П., Фенек М.Ф. (2012). «Обзор зависимости от метионина и роли ограничения метионина в контроле над ростом рака и продлении жизни». Отзывы о лечении рака. 38 (6): 726–36. Дои:10.1016 / j.ctrv.2012.01.004. PMID 22342103.
- ^ Cellarier E, Durando X, Vasson MP, Farges MC, Demiden A, Maurizis JC, Madelmont JC, Chollet P (2003). «Метиониновая зависимость и лечение рака». Отзывы о лечении рака. 29 (6): 489–99. Дои:10.1016 / S0305-7372 (03) 00118-X. PMID 14585259.
- ^ Паппенгеймер AM (1987). "Биографические воспоминания Джона Ховарда Мюллера" (PDF). Вашингтон, округ Колумбия: Национальная академия наук.
- ^ Гедес Р.Л., Просдокими Ф., Фернандес Г.Р., Моура Л.К., Рибейро Х.А., Ортега Дж.М. (декабрь 2011 г.). «Пути биосинтеза аминокислот и ассимиляции азота: большая делеция генома в процессе эволюции эукариот». BMC Genomics. 12 Дополнение 4: S2. Дои:10.1186 / 1471-2164-12-S4-S2. ЧВК 3287585. PMID 22369087.
- ^ Bigelow DJ, Squier TC (январь 2005 г.). «Редокс-модуляция клеточной передачи сигналов и метаболизма посредством обратимого окисления сенсоров метионина в белках, регулирующих кальций». Biochimica et Biophysica Acta (BBA) - Белки и протеомика (Представлена рукопись). 1703 (2): 121–34. Дои:10.1016 / j.bbapap.2004.09.012. PMID 15680220.
- ^ а б c d е ж г час я j k л м п Ферла MP, Патрик WM (август 2014 г.). «Бактериальный биосинтез метионина». Микробиология. 160 (Pt 8): 1571–84. Дои:10.1099 / мик ..0.077826-0. PMID 24939187.
- ^ Чирино П.С., Тан И, Такахаши К., Тиррелл Д.А., Арнольд Ф.Х. (сентябрь 2003 г.). «Глобальное включение норлейцина вместо метионина в гем-домен цитохрома P450 BM-3 увеличивает активность пероксигеназы». Биотехнологии и биоинженерия. 83 (6): 729–34. Дои:10.1002 / бит.10718. PMID 12889037.
- ^ Альварес-Карреньо C, Бесерра A, Ласкано A (октябрь 2013 г.). «Норвалин и норлейцин, возможно, были более распространенными белковыми компонентами на ранних этапах эволюции клеток». Истоки жизни и эволюция биосферы. 43 (4–5): 363–75. Bibcode:2013ОЛЕБ ... 43..363А. Дои:10.1007 / s11084-013-9344-3. PMID 24013929.
- ^ Jukes TH (август 1973 г.). «Аргинин как эволюционный нарушитель синтеза белка». Сообщения о биохимических и биофизических исследованиях. 53 (3): 709–14. Дои:10.1016 / 0006-291x (73) 90151-4. PMID 4731949.
- ^ Икеучи Й, Кимура С., Нумата Т, Накамура Д., Йокогава Т, Огата Т, Вада Т, Сузуки Т, Сузуки Т (апрель 2010 г.). «Агматин-конъюгированный цитидин в антикодоне тРНК необходим для декодирования AUA у архей». Природа Химическая Биология. 6 (4): 277–82. Дои:10.1038 / nchembio.323. PMID 20139989.
- ^ Мурамацу Т., Нисикава К., Немото Ф., Кучино Ю., Нисимура С., Миядзава Т., Йокояма С. (ноябрь 1988 г.). «Кодоновая и аминокислотная специфичности транспортной РНК преобразуются с помощью одной посттранскрипционной модификации». Природа. 336 (6195): 179–81. Bibcode:1988Натура.336..179М. Дои:10.1038 / 336179a0. PMID 3054566.
- ^ Мино К., Исикава К. (сентябрь 2003 г.). «Новая реакция сульфгидрилирования O-фосфо-L-серина, катализируемая O-ацетилсеринсульфгидрилазой из Aeropyrum pernix K1». Письма FEBS. 551 (1–3): 133–8. Дои:10.1016 / S0014-5793 (03) 00913-X. PMID 12965218.
- ^ Карлхайнц Драуз, Ян Грейсон, Аксель Клеманн, Ханс-Петер Криммер, Вольфганг Лойхтенбергер, Кристоф Векбеккер (2006). Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a02_057.pub2.CS1 maint: несколько имен: список авторов (ссылка на сайт)
- ^ Баргер G, Weichselbaum TE (1934). "дл-Метионин ». Органический синтез. 14: 58.; Коллективный объем, 2, п. 384
- ^ Институт медицины (2002). «Белок и аминокислоты». Нормы потребления энергии, углеводов, клетчатки, жиров, жирных кислот, холестерина, белков и аминокислот с пищей. Вашингтон, округ Колумбия: The National Academies Press. С. 589–768.
- ^ «Национальная база данных по питательным веществам для справки». Министерство сельского хозяйства США. Архивировано из оригинал на 2015-03-03. Получено 2009-09-07. Цитировать журнал требует
| журнал =(Помогите) - ^ Финкельштейн JD (май 1990 г.). «Метиониновый метаболизм у млекопитающих». Журнал пищевой биохимии. 1 (5): 228–37. Дои:10.1016/0955-2863(90)90070-2. PMID 15539209.
- ^ Палика Л. (1996). Руководство для потребителей по корму для собак: что входит в состав корма для собак, почему он там и как выбрать лучший корм для вашей собаки. Нью-Йорк: Дом книги Хауэлл. ISBN 978-0-87605-467-3.
- ^ а б Грандисон Р.С., Пайпер, доктор медицины, Партридж Л. (декабрь 2009 г.). «Аминокислотный дисбаланс у дрозофилы объясняет увеличение продолжительности жизни ограничением диеты». Природа. 462 (7276): 1061–4. Bibcode:2009 Натур.462.1061G. Дои:10.1038 / nature08619. ЧВК 2798000. PMID 19956092. Сложить резюме.
- ^ Миллер Р.А., Бюнер Дж., Чанг Й., Харпер Дж. М., Сиглер Р., Смит-Уилок М. (июнь 2005 г.). «Диета с дефицитом метионина продлевает продолжительность жизни мышей, замедляет старение иммунной системы и хрусталика, изменяет уровни глюкозы, Т4, IGF-I и инсулина, а также увеличивает уровни MIF гепатоцитов и устойчивость к стрессу». Ячейка старения. 4 (3): 119–25. Дои:10.1111 / j.1474-9726.2005.00152.x. ЧВК 7159399. PMID 15924568..
- ^ Brown-Borg HM, Rakoczy SG, Wonderlich JA, Rojanathammanee L, Kopchick JJ, Armstrong V, Raasakka D (декабрь 2014 г.). «Передача сигналов гормона роста необходима для увеличения продолжительности жизни с помощью диетического метионина». Ячейка старения. 13 (6): 1019–27. Дои:10.1111 / acel.12269. ЧВК 4244257. PMID 25234161.
- ^ Brown-Borg HM, Rakoczy S, Wonderlich JA, Borg KE, Rojanathammanee L (апрель 2018 г.). «Метаболическая адаптация короткоживущих трансгенных мышей с гормоном роста к ограничению и добавлению метионина». Летопись Нью-Йоркской академии наук. 1418 (1): 118–136. Bibcode:2018НЯСА1418..118Б. Дои:10.1111 / nyas.13687. ЧВК 7025433. PMID 29722030.
- ^ Грандисон Р.К., Пайпер, доктор медицины, Партридж Л. (декабрь 2009 г.). «Аминокислотный дисбаланс у дрозофилы объясняет увеличение продолжительности жизни ограничением диеты». Природа. 462 (7276): 1061–4. Bibcode:2009 Натур.462.1061G. Дои:10.1038 / nature08619. ЧВК 2798000. PMID 19956092.
- ^ «Рецепт аминокислот может быть верным для долгой жизни». Новости науки. 2 декабря 2009 г.
- ^ Hine C, Harputlugil E, Zhang Y, Ruckenstuhl C, Lee BC, Brace L, Longchamp A, Treviño-Villarreal JH, Mejia P, Ozaki CK, Wang R, Gladyshev VN, Madeo F, Mair WB, Mitchell JR (январь 2015 г.) . «Производство эндогенного сероводорода имеет важное значение для улучшения диетических ограничений». Ячейка. 160 (1–2): 132–44. Дои:10.1016 / j.cell.2014.11.048. ЧВК 4297538. PMID 25542313.
- ^ Richie JP, Leutzinger Y, Parthasarathy S, Malloy V, Orentreich N, Zimmerman JA (декабрь 1994). «Ограничение метионина увеличивает глутатион в крови и увеличивает продолжительность жизни у крыс F344». Журнал FASEB. 8 (15): 1302–7. Дои:10.1096 / fasebj.8.15.8001743. PMID 8001743.
- ^ Сан Л., Садыги Аха А.А., Миллер Р.А., Харпер Дж.М. (июль 2009 г.). «Увеличение продолжительности жизни мышей за счет ограничения пищи перед отъемом и ограничения метионина в среднем возрасте». Журналы геронтологии. Серия A, Биологические и медицинские науки. 64 (7): 711–22. Дои:10.1093 / gerona / glp051. ЧВК 2691799. PMID 19414512.
- ^ Komninou D, Leutzinger Y, Reddy BS, Richie JP (2006). «Ограничение метионина подавляет канцерогенез толстой кишки». Питание и рак. 54 (2): 202–8. Дои:10.1207 / s15327914nc5402_6. PMID 16898864.
- ^ Кавуото П., Фенек М.Ф. (октябрь 2012 г.). «Обзор зависимости от метионина и роли ограничения метионина в контроле над ростом рака и продлении жизни». Отзывы о лечении рака. 38 (6): 726–36. Дои:10.1016 / j.ctrv.2012.01.004. PMID 22342103.
- ^ а б Haws, Spencer A .; Ю, Дэян; Е, Цуньци; Вилле, Корал К .; Nguyen, Long C .; Krautkramer, Kimberly A .; Tomasiewicz, Jay L .; Ян, Шани Э .; Миллер, Блейк Р .; Лю, Уоллес H .; Игараси, Кадзухико (13 марта 2020 г.). «Истощение метилметаболита вызывает адаптивные ответы для поддержки стабильности и эпигенетической устойчивости гетерохроматина». Молекулярная клетка. 78 (2): 210–223.e8. Дои:10.1016 / j.molcel.2020.03.004. ISSN 1097-4164. ЧВК 7191556. PMID 32208170.
- ^ Гомес Дж., Каро П., Санчес И., Науди А., Джов М., Портеро-Отин М., Лопес-Торрес М., Памплона Р., Барха Дж. (Июнь 2009 г.).«Влияние диетических добавок метионина на образование митохондриальных радикалов кислорода и окислительное повреждение ДНК в печени и сердце крыс». Журнал биоэнергетики и биомембран. 41 (3): 309–21. Дои:10.1007 / s10863-009-9229-3. PMID 19633937.
- ^ Оз Х.С., Чен Т.С., Нойман М. (март 2008 г.). «Дефицит метионина и повреждение печени на модели диетического стеатогепатита». Пищеварительные заболевания и науки. 53 (3): 767–76. Дои:10.1007 / s10620-007-9900-7. ЧВК 2271115. PMID 17710550.
- ^ Ю. Д., Ян С. Е., Миллер Б. Р., Висински Дж. А., Шерман Д. С., Бринкман Дж. А., Томашевич Дж. Л., Каммингс Н. Э., Кимпл М. Е., Кринс В. Л., Ламминг Д. В. (январь 2018 г.). «Кратковременное лишение метионина улучшает метаболическое здоровье посредством сексуально диморфных, независимых от mTORC1 механизмов». Журнал FASEB. 32 (6): 3471–3482. Дои:10.1096 / fj.201701211R. ЧВК 5956241. PMID 29401631.
- ^ Кастаньо-Мартинес, Тереза; Шумахер, Фабиан; Шумахер, Силке; Кочлик, Бастиан; Вебер, Даниэла; Грун, Тилман; Биманн, Рональд; Макканн, Адриан; Авраам, Клаус (06.03.2019). «Ограничение метионина предотвращает развитие диабета 2 типа у мышей NZO». Журнал FASEB. 33 (6): 7092–7102. Дои:10.1096 / fj.201900150R. ISSN 1530-6860. ЧВК 6529347. PMID 30841758.
- ^ Вуд Дж. М., Деккер Х., Хартманн Х., Чаван Б., Рокос Х., Спенсер Дж. Д. и др. (Июль 2009 г.). «Старческое поседение волос: окислительный стресс, опосредованный H2O2, влияет на цвет волос человека, притупляя восстановление сульфоксида метионина». Журнал FASEB. 23 (7): 2065–75. arXiv:0706.4406. Дои:10.1096 / fj.08-125435. HDL:10454/6241. PMID 19237503.
- ^ Пиннен Ф. и др. (2009). «Совместные препараты, связывающие L-допа и серосодержащие антиоксиданты: новые фармакологические средства против болезни Паркинсона». Журнал медицинской химии. 52 (2): 559–63. Дои:10.1021 / jm801266x. PMID 19093882.
- ^ Refsum H, Ueland PM, Nygård O, Vollset SE (1998). «Гомоцистеин и сердечно-сосудистые заболевания». Ежегодный обзор медицины. 49 (1): 31–62. Дои:10.1146 / annurev.med.49.1.31. PMID 9509248.
- ^ Weaver IC, Champagne FA, Brown SE, Dymov S, Sharma S, Meaney MJ, Szyf M (ноябрь 2005 г.). «Отмена материнского программирования стрессовых реакций у взрослых потомков с помощью метиловых добавок: изменение эпигенетической маркировки в более позднем возрасте». Журнал неврологии. 25 (47): 11045–54. Дои:10.1523 / JNEUROSCI.3652-05.2005. ЧВК 6725868. PMID 16306417.
- ^ Гримшоу, Джейн (25 июля 2011 г.) Метионин для собак и побочные эффекты. cristers360.com
- ^ «Правила и положения». Федеральный регистр. 76 (49): 13501–13504. 14 марта 2011 г.
- ^ Льюис Д.С., Cuda JP, Стивенс Б.Р. (декабрь 2011 г.). «Новый биорациональный пестицид: эффективность метионина против Heraclides (Papilio) cresphontes, суррогата инвазивного Princeps (Papilio) demoleus (Lepidoptera: Papilionidae)». Журнал экономической энтомологии. 104 (6): 1986–90. Дои:10.1603 / ec11132. PMID 22299361.
внешние ссылки
- Рудра М.Н., Чоудхури Л.М. (30 сентября 1950 г.). «Содержание метионина в зерновых и бобовых культурах». Природа. 166 (568): 568. Bibcode:1950Натура.166..568р. Дои:10.1038 / 166568a0. PMID 14780151.