WikiDer > Репинотан
 | |
| Клинические данные | |
|---|---|
| Маршруты администрация | Устный |
| Легальное положение | |
| Легальное положение |
|
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| ChemSpider | |
| UNII | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| Химические и физические данные | |
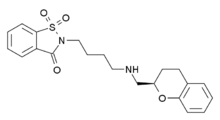
| Формула | C21ЧАС24N2О4S |
| Молярная масса | 400.49 г · моль−1 |
| 3D модель (JSmol) | |
| |
| |
| | |
Репинотан (BAYx3702), производное аминометилхромана, представляет собой селективный 5-HT1А рецептор полный агонист с высокой активностью и эффективностью.[1][2] Она имеет нейропротекторный эффекты в исследованиях на животных,[3][4][5] и был испытан на людях для уменьшения травм головного мозга после травм головы.[6] Впоследствии он был испытан до фазы II для лечения Инсульт, но хотя побочные эффекты были умеренными и заключались в основном в тошноте, репинотан не продемонстрировал достаточной эффективности, чтобы оправдать дальнейшие клинические испытания.[7][8][9] Тем не менее, репинотан продолжает изучаться для других применений, и было обнаружено, что он эффективен для противодействия угнетение дыхания произведено морфий, хотя и с небольшим уменьшением анальгетического эффекта.[10]
История
Компания Bayer Healthcare AG (Вупперталь, Германия) впервые синтезировала репинотан в начале 2000-х годов. В 2004 году ожидалось, что оно будет подано NDA. Исследования фазы III как в отношении ишемического инсульта, так и травматическое повреждение мозга были запущены в марте 2002 года.[11] Однако эти испытания показали, что препарат неэффективен для лечения (ноябрь 2009 г.).[12]
В октябре 2010 года дальнейшие исследования показали, что репинотан способен противодействовать угнетению дыхания, вызванному морфином. Репинотан продолжает изучаться, но пока не выпущен в продажу.[10]
Химические и физические свойства
Репинотан представляет собой энантиомерно чистое производное аминометилхромана с сахаринилбутильным заместителем.[13] Он классифицируется как синтетический органический продукт и имеет пять акцепторов водородных связей и один донор водородных связей. Его топологическая полярная площадь поверхности равна 84,09, и он имеет семь вращающихся связей. Кроме того, его молекулярная масса составляет 400,15 г / моль. Репинотан имеет формальный заряд, равный нулю, и количество ковалентно связанных единиц, равное единице. По химическим и физическим свойствам он похож на лиганды кветиапина, PAT5A и пиоглитазона.[14]
Синтез
Компания Bayer Healthcare AG синтезировала репинотан в трех основных последовательностях реакций. Форма с метаболически стабильным 14углеродная этикетка была необходима для фармакокинетических исследований. Гидрохлорид гидроксилировали в положении 6 хроманового фрагмента.[13]
Схема первой реакции
Для первой последовательности реакций [14C] -фенол использовали в качестве исходного соединения. Затем образование аддукта Михаэля использовали для получения хромановых колец с [14C] -фенолом.[13]
Схема второй реакции
Во второй последовательности реакций первым использовали [карбонил-14C] -2-гидроксиацетофенон. Соединение XII образовалось в результате конденсации [карбонил-14C -] - 2-гидроксиацетофенона с диметилоксилатом и замыканием цикла. Конечный продукт был получен гидрогенолитическим дебензилированием и соляной кислотой.[13]
Схема третьей реакции
Третья реакция включает ацилирование промежуточного соединения XVII с использованием ацетилхлорида. Затем проводили деацетилирование и дебензилирование с помощью HCl. Pd / C использовали на стадии деацетилирования, а Pd / C использовали на стадии дебензилирования.[13]
Механизм действия
Репинотан HCI (BAYx3702) действует как высокоселективный полный агонист рецептора 5-HT1A. Он блокируется специфическим антагонистом рецептора 5-HT1A, WAY 100135. [10] и его основным метаболизатором является CYP2D6. Известно, что этнические различия влияют на CYP2D6. Считается, что репинотан действует за счет гиперполяризации нейронов.[15]
Когда репинотан впервые связывается как с пре-, так и с постсинаптическими рецепторами 5-HT1A, активируются связанные с G-белком внутренне выпрямляющие каналы K +. Это вызывает гиперполяризацию. Поскольку гиперполяризация вызывает подавление возбуждения нейронов и меньшее высвобождение глутамата, нейроны защищены от перевозбуждения. Это может объяснить нейрозащитные свойства репинотана.[8]
Кроме того, репинотан влияет на белок Bcl-2, серотонинергический фактор роста глии S-100beta и фактор роста нервов.[8] Репинотан способен подавлять каспазу-3 через MAPK и PKCalpha.[16] Апоптоз в результате аноксии / реоксигенации и обработки H (2) O (2) также может подавляться.[17]
Было обнаружено, что репинотан связывается с высоким или умеренным сродством с рецепторами альфа-1 и альфа-2 адренергических, 5-HT7- и 5-HT1D, дофаминовыми D2 и D4, сигма-сайтами и 5-HT2C. Он способен увеличивать активность дофаминергических нейронов VTA и высвобождение дофамина медиальной префронтальной корой.[18]
Фармакология
Фармакодинамика
Репинотан действует как селективный высокоаффинный полный агонист рецептора подтипа рецептора 5-HT1A.[12] Он увеличивает активность дофаминовых (DA) нейронов в вентральной тегментальной области, а также высвобождение DA в медиальной префронтальной коре.[19]
Кроме того, это чрезвычайно мощный препарат, способный преодолевать гематоэнцефалический барьер. После инфузии почти мгновенно достигается равновесие распределения между плазмой и мозгом.[20]
Эффективность репинотана в основном зависит от таких факторов, как промежуток времени между началом симптомов инсульта и приемом препарата. Возраст и артериальное давление пациента также играют роль. Обычно наблюдается снижение реакции с увеличением возраста, а также уменьшение реакции по мере повышения артериального давления.[21] Наиболее эффективная доза составляет примерно 1,25 мг в день.[22]
Фармакокинетика
Первичный путь введения Репинотана - внутривенная инъекция,[12] что указывает на то, что он попадает прямо в кровоток. Он способен преодолевать гематоэнцефалический барьер - высокоселективный барьер, отделяющий циркулирующую кровь от внеклеточной жидкости мозга. Диффузия действует как движущая сила, которая позволяет репинотану пересекаться в обоих направлениях. Кроме того, препарат не заряжен, что согласуется с тем фактом, что он способен преодолевать липофильный и неполярный гематоэнцефалический барьер.[20]
Период полувыведения репинотана составляет примерно 1 час. Выведение происходит параллельно из плазмы и мозга. Кроме того, объем распределения репинотана в равновесном состоянии и плазменный клиренс не зависят от дозы. Это свидетельствует о линейной фармакокинетике в диапазоне 0,1–3,0 мкг репинотана / кг / ч.[23]
Скорость инфузии до 150 мкг / ч хорошо воспринимается.[24] Оптимальная доза Репинотана - 1,25 мг / сут.[22]
Возможное влияние пола и возраста на прием репинотана
Пол и возраст не влияют на фармакокинетику репинотана. Собственный вес тоже не играет большой роли.[24]
Уход
Острый ишемический инсульт
Репинотан был первоначально разработан компанией Bayer Healthcare AG (Вупперталь, Германия) в качестве перорального средства для лечения депрессии.[11] Однако вместо этого он был испытан как кандидат для уменьшения травм головного мозга после травмы головы. Затем препарат был исследован в качестве средства профилактики вторичного повреждения головного мозга у жертв ишемического инсульта. Ранние испытания показали способность репинотана снижать потерю нейронов СА1 и СА3 в гиппокампе. Также уменьшилось повреждение корковой ткани. Кроме того, было показано, что репинотан смягчает дефицит пространственного обучения.[25] Однако испытания были прекращены из-за недостаточной эффективности репинотана.[12]
Респираторная депрессия
В настоящее время было обнаружено, что репинотан эффективен при остановке угнетения дыхания, вызванного морфином. Кроме того, он подавляет ноцицепцию в высоких дозах, но усиливает ноцицепцию в малых дозах (0,2 мкг / кг).[10] Репинотан может применяться при болезни Паркинсона, так как он способен снижать эксайтотоксичность, вызванную глутаматом, и, следовательно, некоторую гибель клеток.[26]
Дополнительные лекарства Триалед
Еще одно лекарство от инсульта, испытанное в то же время, пикозотан, похоже на репинотан в том, что он также является агонистом серотонина. Другие препараты включали зонампанел, который действует как антагонист рецептора AMPA вместо агониста рецептора 5-HT1A, и DP-b99. DP-b99 - хелатор металла с железом.[27]
Побочные эффекты
Побочные эффекты репинотана во время испытаний в качестве лечения ишемического инсульта состояли в основном из серотонинергических побочных эффектов, включая тошноту и рвоту. Наиболее частым побочным эффектом была головная боль. Наиболее частыми тяжелыми последствиями были неврологическое ухудшение, кровоизлияние в мозг и отек мозга. Однако в целом было доказано, что репинотан безопасен.[22]
Его текущее исследование как антагониста угнетения дыхания, вызываемого морфином, показало, что он не вызывает серьезных побочных эффектов со стороны сердечно-сосудистой системы. Однако небольшое снижение артериального давления было более незначительным эффектом.[10] Репинотан связан с уменьшением диаметра зрачка.[28]
Исходные прогнозы и текущая доступность
В настоящее время репинотан коммерчески недоступен в США. Первоначально Lehman Brothers ожидала, что продажи в США составят 1000 миллионов долларов, а дата запуска - 2006 год. Оборот банка Vontobel и Bayer оценивается в 450 миллионов евро. Тем не менее, лекарство продолжает исследоваться на предмет лечения, отличного от его первоначального назначения.[11]
Смотрите также
Рекомендации
- ^ De Vry, J .; Schohe-Loop, R .; Heine, H.G .; Greuel, J.M .; Mauler, F .; Schmidt, B .; Sommermeyer, H .; Глейзер, Т. (1998). «Характеристика производного аминометилхромана BAY x 3702 как сильнодействующего агониста рецептора 5-гидрокситриптамина1А». Журнал фармакологии и экспериментальной терапии. 284 (3): 1082–1094. PMID 9495870.
- ^ Dong, J .; De Montigny, C .; Блиер, П. (1998). «Полные агонистические свойства BAY x 3702 при электрофизиологических исследованиях пресинаптических и постсинаптических 5-HT1A рецепторов в гиппокампе и спинном шве крыс». Журнал фармакологии и экспериментальной терапии. 286 (3): 1239–1247. PMID 9732384.
- ^ Алессандри, Б.; Tsuchida, E .; Баллок, Р. М. (1999). «Нейрозащитный эффект нового агониста серотониновых рецепторов, BAY X3702, на очаговое ишемическое повреждение головного мозга, вызванное острой субдуральной гематомой у крысы». Исследование мозга. 845 (2): 232–235. Дои:10.1016 / S0006-8993 (99) 01948-4. PMID 10536203.
- ^ Kline, A.E .; Yu, J .; Horváth, E .; Marion, D.W .; Диксон, К. Э. (2001). «Селективный агонист рецептора 5-HT (1A) репинотан HCl снижает гистопатологию и дефицит пространственного обучения после черепно-мозговой травмы у крыс». Неврология. 106 (3): 547–555. Дои:10.1016 / S0306-4522 (01) 00300-1. PMID 11591455.
- ^ Mauler, F .; Хорват, Э. (2005). «Нейропротекторная эффективность репинотана HCl, агониста рецептора 5-HT1A, на животных моделях инсульта и черепно-мозговой травмы». Журнал церебрального кровотока и метаболизма. 25 (4): 451–459. Дои:10.1038 / sj.jcbfm.9600038. PMID 15674237.
- ^ Ohman, J .; Браакман, Р .; Legout, V .; Группа по изучению травм головного мозга (2001). «Репинотан (BAY x 3702): агонист 5HT1A у пациентов с черепно-мозговой травмой». Журнал нейротравмы. 18 (12): 1313–1321. Дои:10.1089/08977150152725614. PMID 11780862.
- ^ Луцеп, Х. Л. (2005). «Репинотан, агонист 5-HT1A, в лечении острого ишемического инсульта». Текущие целевые показатели по лекарствам. ЦНС и неврологические расстройства. 4 (2): 119–120. Дои:10.2174/1568007053544165. PMID 15857296.
- ^ а б c Берендс А.С., Луитен П.Г., Ньякас С. (2005). «Обзор нейропротективных свойств агониста рецептора 5-HT1A репинотана HCl (BAYx3702) при ишемическом инсульте». Препарат для ЦНС. 11 (4): 379–402. Дои:10.1111 / j.1527-3458.2005.tb00055.x. ЧВК 6741728. PMID 16614737.
- ^ Teal, P .; Davis, S .; Hacke, W .; Kaste, M .; Lyden, P .; Исследователи модифицированного рандомизированного контролируемого исследования воздействия; Fierus, M .; Bayer Healthcare, A. (2009). «Рандомизированное двойное слепое плацебо-контролируемое исследование для оценки эффективности, безопасности, переносимости и фармакокинетических / фармакодинамических эффектов целевого воздействия репинотана внутривенно у пациентов с острым ишемическим инсультом: модифицированное рандомизированное исследование с контролируемым воздействием (mRECT)». Инсульт: журнал церебрального кровообращения. 40 (11): 3518–3525. Дои:10.1161 / STROKEAHA.109.551382. PMID 19745176.
- ^ а б c d е Guenther U, Wrigge H, Theuerkauf N, Boettcher MF, Wensing G, Zinserling J, Putensen C, Hoeft A (октябрь 2010 г.). «Репинотан, селективный агонист 5-HT1A-R, противодействует угнетению дыхания, вызванному морфином, у анестезированных крыс». Анест. Анальг. 111 (4): 901–7. Дои:10.1213 / ANE.0b013e3181eac011. PMID 20802053.
- ^ а б c Луцеп, Х.Л. (июнь 2002 г.). «Репинотан Байер». Текущее мнение об исследуемых лекарствах. 3 (6): 924–7. PMID 12137415.
- ^ а б c d Бирюзовый, P; Дэвис, S; Хаке, Вт; Kaste, M; Lyden, PD; Модифицированное исследование рандомизированного контролируемого воздействия, исследователи; Фиерус, М; Bayer HealthCare, AG (ноябрь 2009 г.). «Рандомизированное двойное слепое плацебо-контролируемое исследование для оценки эффективности, безопасности, переносимости и фармакокинетических / фармакодинамических эффектов целевого воздействия репинотана внутривенно у пациентов с острым ишемическим инсультом: модифицированное рандомизированное исследование с контролируемым воздействием (mRECT)». Инсульт: журнал церебрального кровообращения. 40 (11): 3518–25. Дои:10.1161 / strokeaha.109.551382. PMID 19745176.
- ^ а б c d е Зайдель, Д .; Конрад, М .; Schoof, Y .; Шохе-Луп Р. (ноябрь 2002 г.). «Синтез меченного [14C] гидрохлорида репинотана и его основного метаболита М-6». Журнал меченых соединений и радиофармпрепаратов. 45 (13): 1115–1132. Дои:10.1002 / jlcr.629.
- ^ «ПабХим-Репинотан». Pubchem. Национальный центр биотехнологической информации, Национальная медицинская библиотека США. Получено 10 ноября 2014.
- ^ Танигава, Т; Heinig, R; Куроки, Й; Хигучи, S (февраль 2006 г.). «Оценка межэтнических различий в фармакокинетике репинотана с использованием популяционного подхода» (PDF). Метаболизм и фармакокинетика лекарств. 21 (1): 61–69. Дои:10.2133 / dmpk.21.61. PMID 16547395.
- ^ Де Ври, Дж; Schohe-Loop, R; Гейне, HG; Greuel, JM; Маулер, Ф; Шмидт, В; Sommermeyer, H; Глейзер, Т. (март 1998 г.). «Характеристика производного аминометилхромана BAY x 3702 как сильнодействующего агониста рецептора 5-гидрокситриптамина1А». Журнал фармакологии и экспериментальной терапии. 284 (3): 1082–94. PMID 9495870.
- ^ Адаев, Т; Рэй, я; Sondhi, R; Собоцкий, Т; Банерджи, П. (7 апреля 2003 г.). «Рецептор 5-HT1A, связанный с G-белком, вызывает подавление каспазы-3 через MAPK и протеинкиназу Calpha». Biochimica et Biophysica Acta (BBA) - Исследование молекулярных клеток. 1640 (1): 85–96. Дои:10.1016 / s0167-4889 (03) 00023-5. PMID 12676358.
- ^ Díaz-Mataix, L; Артигас, Ф; Селада, П. (май 2006 г.). «Активация пирамидных клеток в медиальной префронтальной коре головного мозга крысы, проецируемых в вентральную область покрышки агонистом рецептора 5-HT1A». Европейская нейропсихофармакология. 16 (4): 288–96. Дои:10.1016 / j.euroneuro.2005.10.003. HDL:10261/34586. PMID 16290106.
- ^ Díaz-Mataix, L; Скорца, MC; Бортолоцци, А; Тот, М; Celada, P; Артигас, Ф (23 ноября 2005 г.). «Участие рецепторов 5-HT1A в префронтальной коре в модуляции дофаминергической активности: роль в атипичном антипсихотическом действии» (PDF). Журнал неврологии. 25 (47): 10831–43. Дои:10.1523 / jneurosci.2999-05.2005. ЧВК 6725886. PMID 16306396.
- ^ а б Шварц, Т; Беккерманн, Б; Бюнер, К; Маулер, Ф; Schuhmacher, J; Зайдель, Д; Стейнке, Вт; Вайнц, К; Циммерд, Д. (сентябрь 2005 г.). «Фармакокинетика репинотана у здоровых животных и животных с поражением головного мозга». Биофармацевтика и утилизация лекарств. 26 (6): 259–68. Дои:10.1002 / bdd.458. PMID 15966026.
- ^ Teal, P .; Davis, S .; Hacke, W .; Kaste, M .; Lyden, P.D .; Фиерус, М. (10 сентября 2009 г.). «Рандомизированное двойное слепое плацебо-контролируемое испытание для оценки эффективности, безопасности, переносимости и фармакокинетических / фармакодинамических эффектов целевого воздействия репинотана внутривенно у пациентов с острым ишемическим инсультом: модифицированное рандомизированное контролируемое испытание (mRECT)». Гладить. 40 (11): 3518–3525. Дои:10.1161 / STROKEAHA.109.551382. PMID 19745176.
- ^ а б c Бирюзовый, P; Серебро, Флорида; Симард, Д. (февраль 2005 г.). «Исследование BRAINS: безопасность, переносимость и определение дозы репинотана при остром инсульте». Канадский журнал неврологических наук. 32 (1): 61–7. Дои:10,1017 / с0317167100016899. PMID 15825548.
- ^ Heinig, R; Sundaresan, P; Шах, А; Бетчер, М. (2005). «Влияние пола и возраста на фармакокинетику репинотана». Клинические исследования лекарств. 25 (2): 125–34. Дои:10.2165/00044011-200525020-00005. PMID 17523762.
- ^ а б Heinig, R; Бёттчер, MF (2005). «Фармакокинетика возрастающих доз внутривенного репинотана у здоровых добровольцев мужского пола». Клинические исследования лекарств. 25 (2): 115–23. Дои:10.2165/00044011-200525020-00004. PMID 17523761.
- ^ Kline, AE; Ю, Дж; Хорват, Э; Марион, DW; Диксон, CE (2001). «Селективный агонист рецептора 5-HT (1A) репинотан HCl снижает гистопатологию и дефицит пространственного обучения после черепно-мозговой травмы у крыс». Неврология. 106 (3): 547–55. Дои:10.1016 / s0306-4522 (01) 00300-1. PMID 11591455.
- ^ Bezard, E; Герлах, I; Moratalla, R; Брутто, CE; Йорк, Р. (июль 2006 г.). «Опосредованная агонистом рецептора 5-HT1A защита от токсичности МРТР на моделях болезни Паркинсона у мышей и макак». Нейробиология болезней. 23 (1): 77–86. Дои:10.1016 / j.nbd.2006.02.003. HDL:10261/59551. PMID 16545572.
- ^ Ферро, JM; Давалос, А (2006). «Другие нейропротективные методы лечения острого инсульта, проходящие испытания». Цереброваскулярные заболевания. 21 Дополнение 2 (2): 127–30. Дои:10.1159/000091712. PMID 16651823.
- ^ Boettcher, M; Heinig, R; Венсинг, G; Kuhlmann, J (март 2005 г.). «Реакция зрачка: действительный чувствительный клинический биомаркер для соединений 5-HT». Фундаментальная и клиническая фармакология и токсикология. 96 (3): 246. Дои:10.1111 / j.1742-7843.2005.pto960317.x. PMID 15733223.

