WikiDer > Буспирон
 | |
| Клинические данные | |
|---|---|
| Произношение | /ˈбjuːsпɪрoʊп/ (BEW-спи-рон) |
| Торговые наименования | Буспар, Наманспин |
| Другие имена | MJ 9022-1[1] |
| AHFS/Drugs.com | Монография |
| MedlinePlus | a688005 |
| Беременность категория |
|
| Маршруты администрация | Устно |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Биодоступность | 3.9%[2] |
| Связывание с белками | 86–95%[3] |
| Метаболизм | Печень (через CYP3A4)[7][8] |
| Метаболиты | 5-ОН-Буспирон; 6-ОН-Буспирон; 8-ОН-Буспирон; 1-ПП[4][5][6] |
| Устранение период полураспада | 2,5 часа[7] |
| Экскреция | Моча: 29–63%[3] Кал: 18–38%[3] |
| Идентификаторы | |
| |
| Количество CAS |
|
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.048.232 |
| Химические и физические данные | |
| Формула | C21ЧАС31N5О2 |
| Молярная масса | 385.512 г · моль−1 |
| 3D модель (JSmol) | |
| |
| |
| (проверять) | |
Буспирон, продается под торговой маркой Буспарсреди прочего, это лекарство, которое в основном используется для лечения тревожные расстройства, особенно генерализованное тревожное расстройство.[9][10] Преимущества поддерживают его краткосрочное использование.[11] Не было обнаружено, что он эффективен при лечении психоз.[9] Его принимают внутрь, и для достижения эффекта может потребоваться до четырех недель.[9][10]
Общие побочные эффекты буспирона включают тошноту, головные боли, головокружение и трудности с концентрацией внимания.[9][11] Серьезные побочные эффекты могут включать: галлюцинации, серотониновый синдром, и припадки.[11] Его использование в беременность кажется безопасным, но не был хорошо изучен, хотя использование во время кормление грудью не рекомендуется.[11][12] Это серотонин 5-HT1А рецептор агонист.[2]
Буспирон был впервые произведен в 1968 году и разрешен для медицинского применения в США в 1986 году.[9][10] Он доступен как дженерик.[11] В 2017 году это было 80-е место среди наиболее часто назначаемых лекарств в Соединенных Штатах, на него было выписано более десяти миллионов рецептов.[13][14]
Медицинское использование
Беспокойство
Буспирон используется для краткосрочного лечения тревожные расстройства или симптомы беспокойства.[15][16][17][18][19] Обычно это менее предпочтительно, чем селективные ингибиторы обратного захвата серотонина (СИОЗС).[10]
Буспирон не оказывает немедленного анксиолитического действия и, следовательно, имеет отсроченный начало действия; его полная клиническая эффективность может проявиться через 2–4 недели.[20] Было показано, что препарат одинаково эффективен при лечении генерализованного тревожного расстройства (ГТР). бензодиазепины включая диазепам, алпразолам, лоразепам, и клоразепат.[2] Неизвестно, что буспирон эффективен при лечении других тревожные расстройства помимо GAD,[21] хотя есть некоторые ограниченные доказательства того, что он может быть полезен при лечении боязнь общества как дополнение к селективные ингибиторы обратного захвата серотонина (СИОЗС).[2][22]
Другое использование
Сексуальная дисфункция
Есть некоторые свидетельства того, что буспирон сам по себе может быть полезен при лечении гипоактивное расстройство полового влечения (HSDD) у женщин.[23]
Разное
Буспирон неэффективен для лечения отмена бензодиазепинов, отмена барбитуратов, или же отмена алкоголя/Белая горячка.[24]
Антидепрессанты SSRI и SNRI, такие как пароксетин и венлафаксин может вызвать обратимый синдром боли в челюсти / спазма челюсти (хотя это не часто), и буспирон, по-видимому, эффективен в лечении бруксизм на сжатие челюсти, вызванное СИОЗС / СИОЗСН.[25][26]
Противопоказания
Буспирон имеет следующие противопоказания:[27][28]
- Повышенная чувствительность к буспирону.
- Метаболический ацидоз, как в сахарный диабет
- Не следует использовать с Ингибиторы МАО
- Сильно скомпрометировано печень и / или почка функция
Побочные эффекты
Известен побочные эффекты связанные с буспироном включают головокружение, головные боли, тошнота, нервозность, и парестезия.[2] Буспирон относительно хорошо переносится, и не связан с седация, познавательный и психомоторное нарушение, расслабление мышц, физическая зависимость, или же противосудорожное средство последствия.[2] Кроме того, буспирон не производит эйфория[20] и не наркотик злоупотребления.[16]
Неясно, существует ли риск поздняя дискинезия или другие двигательные расстройства с буспироном.[9]
Передозировка
Буспирон, по-видимому, относительно безвреден в случаях приема одного препарата. передозировка, хотя окончательных данных по этому поводу, похоже, нет.[29] В одной клиническое испытание, буспирон вводили здоровым добровольцам мужского пола в дозе 375 мг / день, и он вызывал побочные эффекты, включая тошнота, рвота, головокружение, сонливость, миоз, и желудочное расстройство.[15][16][18] В ранних клинических испытаниях буспирон давали в дозах даже 2400 мг / день, при этом акатизия, тремор, и жесткость мышц наблюдаемый.[30] Преднамеренная передозировка буспирона 250 мг и до 300 мг приводит к сонливости примерно у 50% людей.[30] Сообщалось об одной смерти в связи с приемом 450 мг буспирона вместе с алпразолам, дилтиазем, алкоголь, кокаин.[30]
Взаимодействия
Буспирон показан in vitro быть метаболизируется посредством фермент CYP3A4.[8] Этот вывод согласуется с in vivo взаимодействия, наблюдаемые между буспироном и этими ингибиторами или индукторами цитохром P450 3A4 (CYP3A4) и другие:[27]
- Итраконазол: Повышенный уровень буспирона в плазме.
- Рифампицин: Снижает уровень буспирона в плазме.
- Нефазодон: Повышенный уровень буспирона в плазме.
- Галоперидол: Повышенный уровень галоперидола в плазме.
- Карбамазепин: Снижает уровень буспирона в плазме.
- Грейпфрут: значительно увеличивает уровень буспирона в плазме.[31] Видеть грейпфрут – лекарственные взаимодействия.
- Флувоксамин: Умеренно повысить уровень буспирона в плазме.[32]
Повышенное артериальное давление сообщалось, когда буспирон вводили пациентам, принимающим ингибиторы моноаминоксидазы (ИМАО).[27]
Фармакология
Фармакодинамика
| Сайт | Kя (нМ) | Разновидность | Ссылка |
|---|---|---|---|
| 5-HT1А | 3.98–214 21 (медиана) | Человек | [33][34] |
| 5-HT1B | >100,000 | Крыса | [35] |
| 5-HT1D | 22,000–42,700 | Человек | [36][37] |
| 5-HT2А | 138 759–1,300 | Человек Крыса | [38] [35][38] |
| 5-HT2B | 214 | Человек | [38] |
| 5-HT2C | 490 1,100–6,026 | Человек Крыса / свинья | [38] [35][38] |
| 5-HT3 | >10,000 | Крыса | [39][40] |
| 5-HT4 | >10,000 | Крыса | [40] |
| 5-HT6 | 398 | Мышь | [41] |
| 5-HT7 | 375–381 | Крыса | [42][43] |
| α1 | 1,000 | Крыса | [35] |
| α2 | 6,000 | Крыса | [44] |
| α2А | 7.3 (1-ПП) | Человек | [35] |
| β | 8,800 | Крыса | [35] |
| D1 | 33,000 | Крыса | [35] |
| D2 | 484 240 | Человек Крыса | [45] [35] |
| D3 | 98 | Человек | [45] |
| D4 | 29 | Человек | [45] |
| МАЧ | 38,000 | Крыса | [35] |
| ГАМКА (БДЗ) | >100,000 | Крыса | [35] |
| Значения Kя (нМ). Чем меньше значение, тем сильнее лекарство связывается с участком. | |||
Буспирон действует как агонист из серотонин 5-HT1А рецептор с высоким близость.[2][35] Это частичный агонист обоих пресинаптический 5-HT1А рецепторы, которые тормозят ауторецепторы, и постсинаптический 5-HT1А рецепторы.[2] Считается, что основные эффекты буспирона опосредуются его взаимодействием с пресинаптическим 5-HT.1А рецептора, тем самым уменьшая возбуждение нейронов, продуцирующих серотонин.[2] Буспирон также имеет более низкое сродство к серотонину. 5-HT2А, 5-HT2B, 5-HT2C, 5-HT6, и 5-HT7 рецепторы.[33]
Помимо связывания с рецепторами серотонина, буспирон является антагонистом дофамин D2 рецептор со слабым сродством.[2][35] Он преимущественно блокирует тормозные пресинаптические D2 ауторецепторы и противодействуют постсинаптическому D2 рецепторы только в более высоких дозах.[2] Соответственно, было обнаружено, что буспирон увеличивает дофаминергический нейротрансмиссия в нигростриальный путь в низких дозах, тогда как в более высоких дозах постсинаптический D2 рецепторы заблокированы и антидофаминергический эффекты, такие как гипоактивность и уменьшил стереотипияхотя, в частности, не каталепсия, наблюдаются у животных.[2] Также было обнаружено, что буспирон связывается с дофамином с гораздо более высоким сродством. D3 и D4 рецепторы, где он аналогично антагонист.[45]
Главный метаболит буспирона, 1- (2-пиримидинил) пиперазин (1-PP), встречается на более высоких уровнях циркуляции, чем сам буспирон, и, как известно, действует как мощный α2-адренергический рецептор антагонист.[44][46][47] Этот метаболит может быть ответственным за увеличение норадренергический и дофаминергический активность, наблюдаемая с буспироном у животных.[46][48] Кроме того, 1-PP может играть важную роль в антидепрессивном действии буспирона.[48] Буспирон также имеет очень слабое и, вероятно, клинически несущественное сродство к α1-адренергический рецептор.[35][49] Однако сообщалось, что буспирон продемонстрировал «значительную и избирательную внутреннюю эффективность» в отношении α1-адренергический рецептор экспрессируется «тканевым и видовым образом».[49]
В отличие от бензодиазепинов, буспирон не взаимодействует с ГАМКА рецептор сложный.[2][50]
Фармакокинетика
Буспирон имеет низкий устный биодоступность 3,9% относительно внутривенная инъекция из-за обширного метаболизм первого прохождения.[2] В время до пикового уровня в плазме после приема внутрь - от 0,9 до 1,5 часов.[2] Сообщается, что период полувыведения 2,8 часа,[2] хотя обзор 14 исследований показал, что средний конечный период полувыведения колебался от 2 до 11 часов, а в одном исследовании даже сообщалось о конечном периоде полувыведения 33 часа.[4] Буспирон метаболизируется в первую очередь CYP3A4, и видный лекарственные взаимодействия с ингибиторы и индукторы этого фермент наблюдались.[7][8] Основной метаболиты Буспирона включают 5-гидроксибуспирон, 6-гидроксибуспирон, 8-гидроксибуспирон и 1-PP.[4][5][6] 6-гидроксибуспирон был идентифицирован как преобладающий печеночный метаболит буспирона, уровень которого в плазме в 40 раз выше, чем у буспирона, после перорального введения буспирона людям.[5] Метаболит является частичным агонистом 5-HT с высоким сродством.1А рецептор (Kя = 25 нМ), как и буспирон, и продемонстрировал занятость 5-HT1А рецептор in vivo.[5] Таким образом, он, вероятно, играет важную роль в терапевтических эффектах буспирона.[5] Также было обнаружено, что 1-PP циркулирует на более высоких уровнях, чем сам буспирон, и аналогичным образом может играть значительную роль в клинических эффектах буспирона.[46][48]
Химия
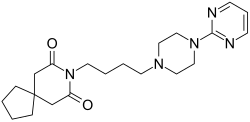
Буспирон является членом азапирон химический класс, и состоит из азаспиродекандион и пиримидинилпиперазин компоненты, связанные вместе бутил цепь.
Аналоги
Структурные аналоги буспирона включают другие азапироны, такие как гепирон, ипсапирон, пероспирон, и тандоспирон.[53]
Синтез
Алкилирование 1- (2-пиримидил) пиперазина (1) с 3-хлор-1-цианопропаном (2, 4-хлорбутиронитрил) дает 3, который уменьшается либо на гидрирование над Никель Ренея катализатор, или с LAH. Полученный 1 ° амин (4) с предыдущей стадии затем подвергают взаимодействию с 3,3-тетраметиленглутаровым ангидридом (5, 8-оксаспиро [4.5] декан-7,9-дион) с получением буспирона (6).
История
Буспирон был первым синтезированный, командой в Мид Джонсон, в 1968 г.,[21] но не был запатентован до 1975 года.[54][55][требуется дополнительная ссылка (и)] Первоначально он разрабатывался как антипсихотик препарат, средство, медикамент действующий на D2 рецептора, но оказалось неэффективным при лечении психоз и был перепрофилирован как анксиолитик.[2] В 1986 г. Бристоль-Майерс Сквибб получил одобрение FDA на применение буспирона для лечения ГТР.[21][56] В патент срок действия буспирона истек в 2001 году, и теперь он доступен как общий препарат.
Общество и культура
Родовые имена
Буспирон это ГОСТИНИЦА, БАН, DCF, и DCIT буспирона, а буспирона гидрохлорид это его USAN, БАНМ, и ЯНВАРЬ.[1][57][58][59]
Имя бренда
Буспирон в основном продавался под торговой маркой Буспар.[57][59] Буспар в настоящее время внесен в список прекращенных Федеральным управлением по лекарственным средствам США.[60] В 2010 году в ответ на петицию граждан FDA США определило, что Buspar не был снят с продажи по соображениям безопасности или эффективности.[61]
Дефицит 2019
В связи с остановкой производства на Mylan Pharmaceuticals посадить в Моргантаун, Западная Вирджиния, Соединенные Штаты испытали нехватку буспирона в 2019 году.[62]
Исследование
Некоторые предварительные исследования подтверждают другие применения, такие как лечение депрессия и поведенческие проблемы после повреждения мозга.[2]
Рекомендации
- ^ а б Elks J (14 ноября 2014 г.). Словарь лекарственных средств: химические данные: химические данные, структуры и библиографии. Springer. С. 192–. ISBN 978-1-4757-2085-3.
- ^ а б c d е ж грамм час я j k л м п о п q р Ссуда C, Politis M (июнь 2012 г.). «Буспирон: что это такое?». Исследование мозга. 1461: 111–8. Дои:10.1016 / j.brainres.2012.04.032. PMID 22608068. S2CID 11734819.
- ^ а б c «Буспирон (Rx) - Буспар, Буспирекс, другие». Ссылка на Medscape. WebMD. Получено 14 ноября 2013.
- ^ а б c Гамманс Р.Э., Майоль РФ, ЛаБудд Ж.А. (март 1986 г.). «Метаболизм и диспозиция буспирона». Американский журнал медицины. 80 (3B): 41–51. Дои:10.1016/0002-9343(86)90331-1. PMID 3515929.
- ^ а б c d е Schatzberg AF, Nemeroff CB (2009). Американский психиатрический учебник по психофармакологии. Американский психиатрический паб. С. 490–. ISBN 978-1-58562-309-9.
- ^ а б Вонг Х., Докенс Р.С., Паджор Л., Йола С., Грейс Дж. Э., Старк А.Д. и др. (Август 2007 г.). «6-гидроксибуспирон является основным активным метаболитом буспирона: оценка фармакокинетики и занятости рецептора 5-гидрокситриптамина1А у крыс». Метаболизм и утилизация лекарств. 35 (8): 1387–92. Дои:10.1124 / dmd.107.015768. PMID 17494642. S2CID 25558546.
- ^ а б c Махмуд И., Сахаджвалла С. (апрель 1999 г.). «Клиническая фармакокинетика и фармакодинамика анксиолитического препарата буспирона». Клиническая фармакокинетика. 36 (4): 277–87. Дои:10.2165/00003088-199936040-00003. PMID 10320950. S2CID 1102318.
- ^ а б c d Чжу М., Чжао В., Хименез Х, Чжан Д., Йола С., Дай Р. и др. (Апрель 2005 г.). «Цитохром P450 3A-опосредованный метаболизм буспирона в микросомах печени человека». Метаболизм и утилизация лекарств. 33 (4): 500–7. Дои:10.1124 / дмд.104.000836. PMID 15640381. S2CID 10142905.
- ^ а б c d е ж «Монография буспирона гидрохлорида для профессионалов». Drugs.com. Американское общество фармацевтов систем здравоохранения. Получено 3 марта 2019.
- ^ а б c d Wilson, T. K .; Трипп, Дж. (Январь 2018 г.). «Буспирон». StatPearls. PMID 30285372.
- ^ а б c d е Британский национальный формуляр: BNF 76 (76 изд.). Фармацевтическая пресса. 2018. с. 338. ISBN 9780857113382.
- ^ «Предупреждения о беременности и кормлении грудью с буспироном». Drugs.com. Получено 3 марта 2019.
- ^ «ТОП-300 2020». ClinCalc. Получено 11 апреля 2020.
- ^ «Буспирон - Статистика употребления наркотиков». ClinCalc. Получено 11 апреля 2020.
- ^ а б «Таблетка буспирона гидрохлорида (буспирона гидрохлорида) [Watson Laboratories, Inc.]». DailyMed. Watson Laboratories, Inc. Июль 2013 г.. Получено 14 ноября 2013.
- ^ а б c "БУСПАР® (гидрохлорид буспирона) таблетки 5 мг и 10 мг ИНФОРМАЦИЯ О ПРОДУКТЕ" (PDF). Услуги электронного бизнеса TGA. Aspen Pharma Pty Ltd. Январь 2010 г.. Получено 14 ноября 2013.
- ^ Росси С., изд. (2013). Австралийский справочник по лекарствам (Изд., 2013). Аделаида: Австралийский фонд руководства по лекарствам. ISBN 978-0-9805790-9-3.
- ^ а б «Буспирон 10 мг таблетки». электронный сборник лекарств. Actavis UK Ltd. 10 сентября 2012 г.. Получено 14 ноября 2013.
- ^ Объединенный формулярный комитет. Британский национальный формуляр (BNF). Фармацевтическая пресса. п. 224.
- ^ а б Садок Б.Дж., Садок В.А., Руис П. (22 сентября 2014 г.). Краткий обзор психиатрии Каплана и Садока: поведенческие науки / клиническая психиатрия. Wolters Kluwer Health. С. 3211–. ISBN 978-1-4698-8375-5.
- ^ а б c Хауленд Р.Х. (ноябрь 2015 г.). «Буспирон: назад в будущее». Журнал психосоциального ухода и служб психического здоровья. 53 (11): 21–4. Дои:10.3928/02793695-20151022-01. PMID 26535760.
- ^ Масдракис В.Г., Турик Д., Болдуин Д.С. (2013). «Фармакологическое лечение социального тревожного расстройства». Тревожные расстройства. Современные тенденции в фармакопсихиатрии. 29. С. 144–53. Дои:10.1159/000351960. ISBN 978-3-318-02463-0. PMID 25225024.
- ^ Гольдштейн I, Ким Н.Н., Клейтон А.Х., ДеРогатис Л.Р., Джиральди А., Пэриш С.Дж. и др. (Январь 2017 г.). «Гипоактивное расстройство сексуального влечения: обзор экспертной группы Международного общества по изучению сексуального здоровья женщин (ISSWSH)». Труды клиники Мэйо. 92 (1): 114–128. Дои:10.1016 / j.mayocp.2016.09.018. PMID 27916394.
- ^ Sontheimer DL, Ables AZ (март 2001 г.). «Эффективно ли лечение имипрамином или буспироном у пациентов, желающих прекратить длительное применение бензодиазепинов?». Журнал семейной практики. 50 (3): 203. PMID 11252203.
- ^ Гарретт А.Р., Хоули Дж.С. (апрель 2018 г.). «Бруксизм, связанный с приемом СИОЗС: систематический обзор опубликованных отчетов о случаях». Неврология. Клиническая практика. 8 (2): 135–141. Дои:10.1212 / CPJ.0000000000000433. ЧВК 5914744. PMID 29708207.
- ^ Приско В., Ианнакконе Т., Ди Грезия Дж. (2017-04-01). «Использование буспирона в селективном бруксизме, вызванном ингибитором обратного захвата серотонина». Европейская психиатрия. Резюме 25-го Европейского конгресса психиатрии. 41: S855. Дои:10.1016 / j.eurpsy.2017.01.1701.
- ^ а б c «Монография Буспирона». Drugs.com. Получено 2011-08-27.
- ^ Геддес Дж, Гельдер М.Г., Маю Р. (2005). Психиатрия. Оксфорд [Оксфордшир]: Издательство Оксфордского университета. п.237. ISBN 978-0-19-852863-0.
- ^ Фултон Б., Брогден Р. Н. (1997). «Буспирон». Препараты ЦНС. 7 (1): 68–88. Дои:10.2165/00023210-199707010-00007. ISSN 1172-7047.
- ^ а б c Дарт RC (2004). Медицинская токсикология. Липпинкотт Уильямс и Уилкинс. С. 886–. ISBN 978-0-7817-2845-4.
- ^ Лилья Дж. Дж., Кивисто К. Т., Бакман Дж. Т., Ламберг Т. С., Неувонен П. Дж. (Декабрь 1998 г.). «Грейпфрутовый сок существенно увеличивает плазменную концентрацию буспирона». Клиническая фармакология и терапия. 64 (6): 655–60. Дои:10.1016 / S0009-9236 (98) 90056-X. PMID 9871430. S2CID 22009095.
- ^ Lamberg TS, Kivistö KT, Laitila J, Mårtensson K, Neuvonen PJ (1998). «Влияние флувоксамина на фармакокинетику и фармакодинамику буспирона». Европейский журнал клинической фармакологии. 54 (9–10): 761–6. Дои:10.1007 / s002280050548. PMID 9923581. S2CID 21939719.
- ^ а б c Рот Б.Л., Дрискол Дж. «ПДСП Кя База данных". Программа скрининга психоактивных веществ (PDSP). Университет Северной Каролины в Чапел-Хилл и Национальный институт психического здоровья США. Получено 14 августа 2017.
- ^ Бесс Ф.Г., Мартин ИЛ (1994). «Молекулярная биология 5-HT рецепторов». Нейрофармакология. 33 (3–4): 275–317. Дои:10.1016/0028-3908(94)90059-0. PMID 7984267. S2CID 35553281.
- ^ а б c d е ж грамм час я j k л м Хамик А., Оксенберг Д., Фишетт С., Перутка С.Дж. (июль 1990 г.). «Анализ взаимодействия тандоспирона (SM-3997) с сайтами связывания рецепторов нейромедиаторов». Биологическая психиатрия. 28 (2): 99–109. Дои:10.1016 / 0006-3223 (90) 90627-э. PMID 1974152. S2CID 25608914.
- ^ Peroutka SJ, Switzer JA, Hamik A (1989). «Идентификация сайтов связывания 5-гидрокситриптамина1D в мембранах головного мозга человека». Синапс. 3 (1): 61–6. Дои:10.1002 / син. 890030109. PMID 2521959.
- ^ Waeber C, Schoeffter P, Palacios JM, Hoyer D (июнь 1988 г.). «Молекулярная фармакология сайтов узнавания 5-HT1D: исследования связывания радиолиганда в мембранах мозга человека, свиньи и теленка». Архив фармакологии Наунин-Шмидеберг. 337 (6): 595–601. Дои:10.1007 / bf00175783. PMID 2975354. S2CID 21344978.
- ^ а б c d е Bonhaus DW, Weinhardt KK, Taylor M, DeSouza A, McNeeley PM, Szczepanski K и др. (1997). «RS-102221: новый высокоаффинный и селективный антагонист рецептора 5-HT2C». Нейрофармакология. 36 (4–5): 621–9. Дои:10.1016 / с0028-3908 (97) 00049-х. PMID 9225287. S2CID 24930608.
- ^ Нельсон Д.Р., Томас Д.Р. (май 1989 г.). «[3H] -BRL 43694 (гранисетрон), специфический лиганд для сайтов связывания 5-HT3 в корковых мембранах мозга крыс». Биохимическая фармакология. 38 (10): 1693–5. Дои:10.1016/0006-2952(89)90319-5. PMID 2543418.
- ^ а б Borsini F, Giraldo E, Monferini E, Antonini G, Parenti M, Bietti G, Donetti A (сентябрь 1995 г.). «BIMT 17, антагонист рецептора 5-HT2A и полный агонист рецептора 5-HT1A в коре головного мозга крысы». Архив фармакологии Наунин-Шмидеберг. 352 (3): 276–82. Дои:10.1007 / bf00168557. PMID 8584042. S2CID 19340842.
- ^ Плассат Дж. Л., Амлайки Н., Хен Р. (август 1993 г.). «Молекулярное клонирование рецептора серотонина млекопитающих, который активирует аденилатциклазу». Молекулярная фармакология. 44 (2): 229–36. PMID 8394987.
- ^ Ловенберг Т.В., Барон Б.М., де Лесеа Л., Миллер Д.Д., Проссер Р.А., Реа М.А. и др. (Сентябрь 1993 г.). «Новый рецептор серотонина, активирующий аденилатциклазу (5-HT7), участвующий в регуляции циркадных ритмов млекопитающих». Нейрон. 11 (3): 449–58. Дои:10.1016 / 0896-6273 (93) 90149-л. PMID 8398139. S2CID 28729004.
- ^ Руат М., Трайффорт Э., Лерс Р., Тардивель-Лакомб Дж., Диас Дж., Аранг Дж. М., Шварц Дж. К. (сентябрь 1993 г.). «Молекулярное клонирование, характеристика и локализация высокоаффинного рецептора серотонина (5-HT7), активирующего образование цАМФ». Труды Национальной академии наук Соединенных Штатов Америки. 90 (18): 8547–51. Bibcode:1993ПНАС ... 90.8547R. Дои:10.1073 / пнас.90.18.8547. ЧВК 47394. PMID 8397408.
- ^ а б Блиер П., Кюре О, Шапут И, де Монтиньи С. (июль 1991 г.). «Тандоспирон и его метаболит, 1- (2-пиримидинил) -пиперазин - II. Влияние острого введения 1-PP и длительного приема тандоспирона на норадренергическую нейротрансмиссию». Нейрофармакология. 30 (7): 691–701. Дои:10.1016 / 0028-3908 (91) 90176-в. PMID 1681447. S2CID 44297577.
- ^ а б c d Бергман Дж., Крыша Р.А., Фурман К.А., Конрой Дж.Л., Мелло Н.К., Сибли Д.Р., Сколник П. (март 2013 г.). «Модификация самостоятельного введения кокаина буспироном (буспар®): потенциальное участие дофаминовых рецепторов D3 и D4». Международный журнал нейропсихофармакологии. 16 (2): 445–58. Дои:10.1017 / S1461145712000661. ЧВК 5100812. PMID 22827916.
- ^ а б c Tunnicliff G (сентябрь 1991 г.). «Молекулярные основы анксиолитического действия буспирона». Фармакология и токсикология. 69 (3): 149–56. Дои:10.1111 / j.1600-0773.1991.tb01289.x. PMID 1796057.
- ^ Зудевельд К.П., Русич-Павлетич Дж., Маас Х.Д., Пелетье Л.А., Ван дер Грааф PH, Данхоф М. (декабрь 2002 г.). «Фармакокинетико-фармакодинамическое моделирование буспирона и его метаболита 1- (2-пиримидинил) пиперазина у крыс». Журнал фармакологии и экспериментальной терапии. 303 (3): 1130–7. Дои:10.1124 / jpet.102.036798. PMID 12438536. S2CID 14139919.
- ^ а б c Фава М (2007). «Комбинация буспирона и бупропиона в лечении депрессии». Психотерапия и психосоматика. 76 (5): 311–2. Дои:10.1159/000104708. PMID 17700052. S2CID 46284917.
- ^ а б Стерн Т.А., Фава М., Виленс Т.Э., Розенбаум Дж.Ф. (27 апреля 2015 г.). Электронная книга по психофармакологии и нейротерапии Массачусетской больницы общего профиля. Elsevier Health Sciences. С. 29–. ISBN 978-0-323-41323-7.
- ^ Nutt DJ, Ballenger JC (15 апреля 2008 г.). Тревожные расстройства. Джон Вили и сыновья. С. 395–. ISBN 978-0-470-98683-7.
- ^ Доккенс Р.К., Салазар Д.Е., Фулмор И.Е., Велинг М., Арнольд М.Э., Круп Р. (ноябрь 2006 г.). «Фармакокинетика недавно идентифицированного активного метаболита буспирона после введения буспирона в диапазоне терапевтических доз». Журнал клинической фармакологии. 46 (11): 1308–12. Дои:10.1177/0091270006292250. PMID 17050795.
- ^ Джаджу HK, Mayol RF, LaBudde JA, Blair IA (1989). «Метаболизм успокаивающего препарата буспирона у людей». Метаболизм и утилизация лекарств. 17 (6): 634–40. PMID 2575499.
- ^ Тейлор Д. П., Moon SL (июль 1991 г.). «Буспирон и родственные ему соединения в качестве альтернативных анксиолитиков». Нейропептиды. 19 Дополнение: 15–9. Дои:10.1016 / 0143-4179 (91) 90078-в.. PMID 1679210. S2CID 13730683.
- ^ а б Аллен Л. Е., Фергюсон ХК, Киссель Дж. У. (май 1972 г.). «Психоседативные агенты. 2. 8- (4-Замещенный 1-пиперазинилалкил) -8-азаспиро (4.5) декан-7,9-дионы». Журнал медицинской химии. 15 (5): 477–9. Дои:10.1021 / jm00275a009. PMID 5035267.
- ^ Патент США 3907801 N- (8 (4-пиридилпиперазино) алкил (9-заспироалкандионы)
- ^ Федеральное управление по лекарственным средствам США (9 сентября 1986 г.). Одобрение типа 1 для новых молекулярных продуктов. https://www.accessdata.fda.gov/drugsatfda_docs/nda/pre96/018731Orig1s000rev.pdf
- ^ а б Index Nominum 2000: Международный справочник лекарственных средств. Тейлор и Фрэнсис. Январь 2000. С. 149–. ISBN 978-3-88763-075-1.
- ^ Мортон И.К., Холл Дж. М. (6 декабря 2012 г.). Краткий словарь фармакологических агентов: свойства и синонимы. Springer Science & Business Media. С. 57–. ISBN 978-94-011-4439-1.
- ^ а б «Буспирон».
- ^ "Drugs @ FDA: одобренные FDA лекарственные препараты". www.accessdata.fda.gov. Получено 2019-09-20.
- ^ «Определение того, что таблетки BUSPAR (буспирона гидрохлорид), 10 миллиграммов, 15 миллиграммов и 30 миллиграммов не были изъяты из продажи по причинам безопасности или эффективности». Федеральный регистр. 2010-10-19. Получено 2019-09-20.
- ^ Рабин RC (01.02.2019). «Нехватка лекарств от тревожных состояний заставляет пациентов нервничать». Нью-Йорк Таймс. ISSN 0362-4331. Получено 2019-09-20.
внешняя ссылка
 СМИ, связанные с Буспирон в Wikimedia Commons
СМИ, связанные с Буспирон в Wikimedia Commons- «Буспирон». Портал информации о наркотиках. Национальная медицинская библиотека США.


